Emilio Maseda Garrido
Hospital Universitario“ La Paz“
Referencia completa
Terragni PP, Del Sorbo L, Mascia L, Urbino R, Martin EL, Birocco A, Faggiano C, Quintel M, Gattinoni L, Ranieri VM. Tidal volume lower than 6 ml/kg enhances lung protection. Role of extracorporeal carbon dioxide removal. Anesthesiology 2009; 111:826-35. (Pubmed) (Pdf)
Introducción
En el año 2000 se publicó un artículo del ARDS Network que cambió la forma de ventilar a los pacientes con SDRA1. De forma tradicional, los pacientes con SDRA eran ventilados con volúmenes cercanos a los 10-15 ml/kg para poder mantener la PaCO2 dentro de los límites normales. Sin embargo, la utilización de volúmenes corrientes más pequeños demostró mejorar la supervivencia de los pacientes con SDRA, y en el momento actual los valores estándares de ventilación para los pacientes con lesión
No obstante, incluso utilizando valores como éstos de volumen corriente y de presión en la vía aérea, la ventilación mecánica puede a su vez dañar el pulmón ya lesionado. Ésto es debido a la heterogeneidad anatómica de las lesiones que subyacen en el pulmón con SDRA, lo cual genera una respuesta inflamatoria difusa2. De hecho, cualquier volumen corriente, por muy pequeño que sea, puede dañar el pulmón con SDRA debido a una sobredistensión de los alvéolos no lesionados y al colapso cíclico de la vía aérea más distal llena de líquido.
Uno de los problemas que limita la utilización de un volumen corriente pequeño en el paciente con SDRA es el aumento en la PaCO2 y la aparición de una acidosis respiratoria progresiva, mayor cuanto mayor es la disminución en el volumen corriente.
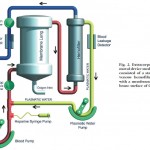
Resumen
El estudio fue realizado en un único centro de Italia desde Julio de 2006 a Septiembre de 2007 en todos los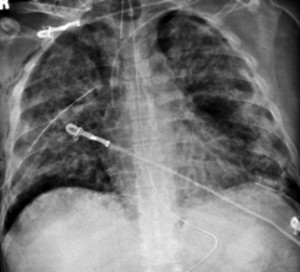
En aquellos pacientes que presentaban una presión meseta de 26-27 cmH2O, se mantuvo la misma estrategia ventilatoria al menos durante 72 h. Sin embargo, en los pacientes con una presión meseta entre 28-30 cmH2O se modificó la forma de ventilación durante al menos las siguientes 72 h de la siguiente manera:
1) el volumen corriente se disminuyó progresivamente (1 ml/kg del peso ideal cada 4 h) hasta conseguir una presión meseta de 26-27 cmH2O;
2) se trató de evitar la aparición de atelectasias por reabsorción en aquellos pacientes con un volumen corriente muy pequeño utilizando la relación PEEP-FiO2 utilizada en el brazo de la“ PEEP más elevada“ en el estudio ALVEOLI3;
3) la frecuencia respiratoria fue aumentada hasta 40 respiraciones/min, y se administró bicarbonato hasta 20 mEq/h;
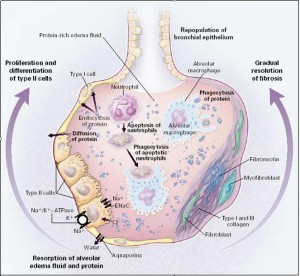
Después de 72 h con esta estrategia de ventilación, una vez al día se programaba el flujo de hemofiltración en su valor mínimo (50 ml/ min) , el volumen corriente se aumentaba a 6 ml/kg del peso ideal, y la relación PEEP-FiO2 se establecía según la pauta convencional seguida en el estudio ARDSNet1; si la presión meseta permanecía < 28 cmH2O durante 3 h, la eliminación extracorpórea de CO2 se interrumpía.
De los 32 pacientes que fueron incluidos en el estudio, 22 tuvieron una presión meseta de 26-27 cmH2O, y 10 pacientes entre 28-30 cmH2O. No hubo diferencias significativas en cuanto a la gravedad entre ambos grupos de pacientes evaluados mediante el SAPSII.
Los resultados más significativos del estudio fueron que en el grupo de pacientes sometidos a bypass veno-venoso se produjo una normalización progresiva de la PaCO2 y del pH, cuyos valores tras 69 minutos de procedimiento fueron 50,4 ± 8,2 mmHg y 7,32 ± 0,03, respectivamente (p<0,001), permitiendo disminuir el volumen corriente a menos de 6 ml/kg durante 144 h de media. Asimismo, después de 72 h de ventilación con un volumen corriente menor de 6 ml/kg se observó una mejoría en los marcadores morfológicos de protección pulmonar en la TC pulmonar y una disminución de la concentración de citoquinas pulmonares en el lavado broncoalveolar (p<0,01). No hubo ninguna complicación relacionada con la técnica en aquellos pacientes en los que se utilizó la eliminación extracorpórea de CO2.
Comentario
Los resultados de este estudio sugieren que una disminución en el volumen corriente condiciona una disminución en la hiperinsuflación pulmonar y en la producción de mediadores de la inflamación en los pacientes con SDRA que tienen una presión meseta entre 28 y 30 cmH2O, cuando ventilamos según la estrategia ARDSNet1.
Además, los resultados apoyan la eliminación extracorpórea de CO2 para tratar de forma segura y eficaz la acidosis respiratoria ocasionada por la disminución del volumen corriente y, por lo tanto, restablecer la normalidad en el pH arterial.
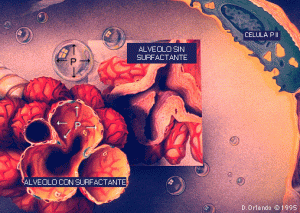
Diferentes estudios sugieren que la acidosis hipercápnica se tolera bien (hipercapnia permisiva)4, e incluso puede ser beneficiosa. Un análisis post hoc del estudio ARDSNet1 sugiere que la acidosis hipercápnica se asocia con una mayor superviviencia en los pacientes ventilados con un volumen corriente de 12 ml/kg (presión media en la vía aérea de 33 cmH2O), pero no en aquellos ventilados con un volumen corriente de 6 ml/kg (presión media en la vía aérea de 25 cmH2O)5.
En el momento actual no está claro la importancia relativa de la acidosis frente a la hipercapnia per se, y asimismo, de la protección pulmonar con volúmenes corrientes pequeños frente a la hipercapnia per se. Necesitaríamos un ensayo clínico que separase el volumen corriente de la acidosis hipercápnica, utilizando la eliminación extracorpórea del CO2, como en el artículo que estamos comentando.
A pesar de las limitaciones del estudio, creo que este trabajo nos abre una puerta hacia un futuro en el que los pacientes con SDRA puedan ser tratados con un circuito extracorpóreo mínimamente invasivo para eliminar CO2, y con una presión positiva continua no invasiva en la vía aérea para mantener la oxigenación, lo que estaría en consonancia con la filosofía actual de la ventilación mecánica: evitar la intubación traqueal, la lesión pulmonar inducida por la ventilación mecánica y la infección nosocomial.
Bibliografía
1. ARDS Network: Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. N Engl J Med 2000; 342:1301-8. (Pubmed) (Pdf)
2. Bellani G, Messa C, Gerra L, Spagnolli E, Foti G, Patroniti N, Fumagalli R, Musch G, Fazio, Pesenti A. Lungs of patients with acute respiratory distress syndrome show diffuse inflammation in normally aerated regions: A [18F]-Fluoro-2-deoxy-D-glucose PET/CT study. Crit Care Med 2009; 37:2216-22. (Pubmed)
3. Brower RG, Lanken PN, MacIntyre N, Matthay MA, Morris A, Ancukiewicz M, Schoenfeld D, Thompson BT. Higher versus lowerpositive end-expiratory pressures in patients with the acute respiratory distress syndrome. N Engl J Med 2004; 351:327-36. (Pubmed) (Pdf)
4. Hickling KG, Henderson SG, Jackson R. Low mortality associatted with low volume pressure limited ventilation with permissive hypercapnia in severe adult respiratory distress syndrome. Intensive Care Med 1990; 16:372-7. (Pubmed)
5. Kregenow DA, Rubenfeld GD, Hudson LD, Swenson ER. Hypercapnic acidosis and mortality in acute lung injury. Crit Care Med 2006; 34:1-7. (Pubmed)
Emilio Maseda Garrido Servicio de Anestesiología y Reanimación Hospital Universitario“ La Paz“



Muy bueno el articulo
Muy buena y real la visión del anestesiologo