 Rafael Gonzalez. Anestesia y Reanimación. H.U. de León.
Rafael Gonzalez. Anestesia y Reanimación. H.U. de León.
En AnestesiaR hemos publicado varias entradas comentando guías nacionales y americanas, sobre el tratamiento de las infecciones intraabdominales. Es sorprendente descubrir las diferencias entre ellas, no sólo debidas al contexto. Y es que en este tema las dudas son numerosas, y a pesar de la importancia y frecuencia de la patología los estudios en pacientes graves no son abundantes. De ahí el interés de la revisión que comentamos hoy, con un enfoque diferente y muy pegado a la práctica clínica.
Original: Essentials for selecting antimicrobial therapy for intra-abdominal infections. S. Blot, J.J De Waele and D. Vogelaers. Drugs 2012; 72 (6): e17-e32 (PubMed) (pdf) (epub)
Resumen
La introducción de este artículo ya presenta como conceptos interesantes que la infección intraabdominal (IIA) tiene unas características propias: la posibilidad de control quirúrgico de la fuente (ya sea por laparotomía, laparoscopia o drenaje percutáneo), su carácter polimicrobiano, y la frecuente asociación de estas infecciones con los cuadros de fracaso renal agudo y shock séptico.
Los autores recalcan que, conceptualmente, se ha distinguido entre peritonitis primaria o con integridad del tracto digestivo; secundaria o con disrupción del mismo en algún punto; y terciaria, refiriéndose a aquella que no se ha resuelto tras varias intervenciones y/o ciclos de tratamiento antibiótico) e infección intra-abdominal (diferenciando aquí entre complicada y no complicada, en función de la presencia o no de peritonitis, ya sea esta localizada o extensa). Respecto a este tema se hace una interesante reflexión sobre la falta de consenso que ha podido existir en los diferentes estudios entre el concepto teórico de IIA complicada (el mencionado en el párrafo anterior) y el concepto“ clínico“ (aquella con características de gravedad, de extensión anatómica o de presencia de patógenos resistentes).
Por ello proponen una clasificación alternativa en la que se van a desechar los términos“ complicada“,“ no complicada“, y“ peritonitis terciaria“ porque han podido conducir a error bien por la falta de precisión, bien por la falta de acuerdo en el concepto expresado.
En esta nueva propuesta se relacionan 3 aspectos:
a) Integridad anatómica.
b) Gravedad de la expresión clínica.
c) Presencia de factores de riesgo para el hallazgo de patógenos resistentes (MDR).
Como estos últimos factores se limitan básicamente a la presencia o no de tratamiento antimicrobiano previo y/o a la hospitalización previa durante un periodo lo suficientemente prolongado (que se establece en torno a 5-7 días), la clasificación propuesta queda así de manera que cada número se corresponda con un régimen antibiótico determinado (tabla 1)
Comentario
Algunos de los puntos más destacables de esta revisión, son los siguientes:
– La utilidad de los cultivos de líquido abdominal están en debate en la IIA comunitaria: suelen mostrar una flora polimicrobiana en la que es difícil distinguir entre patógenos y contaminantes. Además suelen modificar poco el régimen standard en presencia de peritonitis. Tampoco se recomiendan hemocultivos.
– En cambio, en IIA nosocomial, estos cultivos de líquido abdominal se convierten en obligados al poder dar información sobre a) gérmenes no habitualmente cubiertos en IIA comunitaria y b) presencia de gérmenes que ya se hayan convertido en resistentes a los tratamientos recomendados 8 hasta el 79% de los aislamientos en algunas series). Además, en los casos de presentación como sepsis grave y shock séptico, los hemocultivos pueden ser útiles tanto en la detección de gérmenes como en la definición del pronóstico subsiguiente cuando son positivos.
– La exposición a más de 2 días de tratamiento antibiótico previo, se reconoce como el factor más importante para la presencia de patógenos resistentes, independientemente del momento y lugar de aparición (y así se expresa en la tabla de clasificación).
– La discutida relevancia de los aislamientos de Candida spp. y, por tanto, la dudosa recomendación de incluir antifúngicos en el tratamiento empírico de estos pacientes, excepto en dos grupos de riesgo definidos: pacientes neutropénicos y pacientes con fuga anastomótica.
– La recomendación de no cubrir Enterococci en la mayoría de las IIA comunitarias, y sí en la nosocomial. Es razonable su tratamiento en casos de shock séptico, tratamientos prolongados con cefalosporinas, inmunosupresión, presencia de prótesis valvulares y recurrencia de IIA con manifestación de sepsis grave.
– En cuanto a los patrones de resistencia locales, avisa de la necesidad de monitorizar resultados propios y en la infección mencionada ya que muchos datos pueden ser extrapolados de otros focos (por ejemplo, E. Coli resistente a fluorquinolonas en infección urinaria) y no reflejar la realidad de la IIA.
– Reflexión interesante sobre las alergias a betalactámicos, recomendando actitudes diferentes según sean reacciones mediadas o no por IgE, postulando aquí el uso de Tigeciclina y Aztreonam.
– Finalmente, recomendaciones sobre la duración del tratamiento de 5 a 7 días (recordando que, incluso regímenes de 3 días en peritonitis leves-moderadas tienen resultados similares a pautas de 5-10 días).
Bibliografía
1.- Guidelines for the empirical antibiotic treatment of intra-abdominal infections.Guirao X, Arias J, Badía JM, García-Rodríguez JA, Mensa J, Alvarez-Lerma F, Borges M, Barberán J, Maseda E, Salavert M, Llinares P,Gobernado M, García Rey C. Rev Esp Anestesiol Reanim. 2010 Jan;57(1):41-60. (PubMed)
2.- Diagnosis and management of complicated intra-abdominal infection in adults and children: guidelines by the Surgical Infection Society and the Infectious Diseases Society of America. Clinical Infectious Diseases 2010, 50: 133-164. (PubMed) (pdf)

 Rafael Gonzalez. Anestesia y Reanimación. H.U. de León.
Rafael Gonzalez. Anestesia y Reanimación. H.U. de León.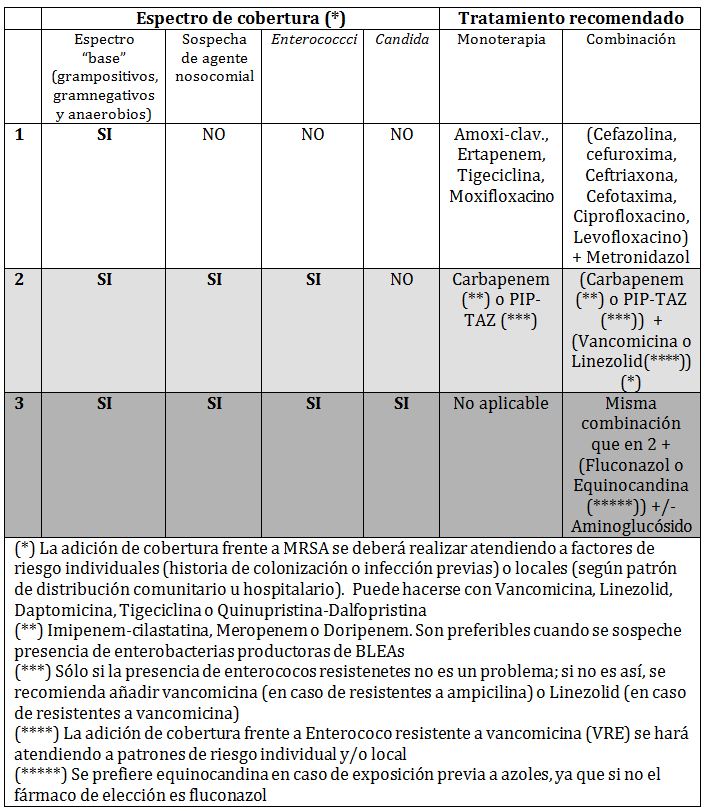


Hola Rafael,
Lo primero agradecer tu revision sobre este artículo y este tema tan recurrente en nuestras Reanimaciones pero tras leerlo hay algunos puntos sobre los que no estoy de acuerdo.
La división en el tratamiento de la infección abdominal habitualmente se hace entre infección abdominal leve-moderada (que se correspondería con el primer apartado de la tabla) e infección abdominal grave (que uniría los dos segundos). El manejo y antibioterpia a efectos prácticos de la sepsis grave y del shock séptico es muy similar y cuanto mas sencillo y claros sean los algoritmos mejor.
Siguiendo la tabla al tener tantas divisiones se podría plantear el caso de una infección nosocomial tardía con una sepsis grave, peritonitis localizada y que solo recibiera pipe-tazo como antibiótico inicial. Podría ser suficiente pero es incongruente con lo que el propio artículo defiende después de cubrir gérmenes nosocomiales (pseudomonas, enterobacterias BLEE, enterococos resistentes a vancomicina…)
Echo de menos que se valore la comorbilidad del paciente.Tiene el paciente factores de riesgo de mala evolución? No es lo mismo tratar una infección comunitaria grave en un joven de 25 años sano que en un paciente cirrótico, diabético, malnutrido, con IRC que acude al hospital cada tres días a dializarse, etc
No estoy de acuerdo en que no se deban tomar hemocultivos en las infecciones de origen comunitario. La toma de cultivos es la base para poder ajustar después la antibioterapia y no perpetuar antibióticos potentes demasiados días.
Estoy en cambio absolutamente de acuerdo con que cada hospital debe estudiar su epidemiología y adaptar las guias de consenso a su entorno. En nuestra Reanimación lo hicimos pero tomamos como base el algoritmo de consenso que se publicó hace tres años en la revista española de quimioterapia (Rev Esp Quimiter 2009;22(3)151-77)
Un saludo!
Marta Bernardino
H.U. Fundación Alcorcón (Madrid)
Hola Marta:
ante todo disculpa la tardanza en escribirte. Creo que tus comentarios son extremadamente interesantes y que serán muchas las personas que estarán de acuerdo con ellos.
Cuando decidí revisar este artículo para la página, reconozco que lo que más me llamó la atención es la revista en la que se publicó (no es una de nuestras «habituales»). Y que, como ya comenté entonces, me pareció muy interesante que nos hiciera reflexionar sobre el significado de los términos «complicada» y «no complicada» en función de quien los use (puede referirse a la extensión o no del proceso a nivel abdominal si son utilizados en términos estrictamente microbiológicos y anatomopatológicos, mientras que en términos clínicos puede haberse aplicado a diferencias en la gravedad del cuadro o dificultades en el tratamiento antibiótico por, por ejemplo, presencia de multirresistentes).
Más allá de esto, el acuerdo o no con lo allí expuesto está servido. Por ejemplo, y respecto al tema de no realizar hemocultivos en IIA comunitaria, la IDSA en sus guías del 2010 así lo dice (bien es verdad que son recomendaciones B-III y que su utilidad para acortar-guiar tratamientos la limita a inmunocomprometidos y pacientes «tóxicos», en los cuales espero que estén incluidos los que tú y yo tratamos)
Otro punto es la posible complicación que tiene la tabla para su interpretación que puede ser algo «arbitraria». Te digo esto porque yo, en el mismo caso que tú planteas, y que por tanto entraría en el grupo 2 de tratamiento, nunca trataría sólo con PIP-TAZ, debido al aumento progresivo tanto de productores de BLEAs como de Enterococo resistente a Vancomicina (y esta sería la actitud que se comenta en los asteriscos de la tabla). De todas formas, me sigue pareciendo que la tabla transmite la misma filosofía que todas las demás (incluido por supuesto las recomendaciones a la que tú haces referencia de la Rev Esp Quimioter 2009) y que és: «no trates al paciente inicialmente con PIP-TAZ si la evolución es inferior a 7 días y no está grave, ya que es un arma que podemos tener para cuando lo esté (que tiene papeletas)». El tratamiento «anticipado» (y por desgracia, casi nunca precoz) con este antipseudomónico parece claro que es una mala política y obliga al uso de más carbapenémicos como «siguiente escalón» en lugares donde la prevalencia de BLEAs se dispara (aunque este fenómeno esté relacionado directamente con el consumo de cefalosporinas de tercera generación), perdiendo también entonces su utilidad como antipseudomónico.
Creo que tu último párrafo es la mejor máxima de tratamiento, resume en muy pocas palabras lo que hay que hacer y que no se nos debería olvidar nunca (aunque eso implica tener un conocimiento extenso que no siempre es posible)
Te agradezco mucho el interés, Marta (al fin y al cabo esto lleva un «tiempito») y espero que saludes de mi parte a todos tus compañeros por allí (de los que, por cierto, siempre tendré un cariñoso recuerdo por lo bien que me acogieron hace años)
Rafa