Dra. Raquel Fernández-García.
Artículo Original:
Jean-Louis Vincent y Daniel De Backer. ICU nephrology: the implications of cardiovascular alterations in the acutely ill. Kidney Int. 2011. (PubMed)
Introducción
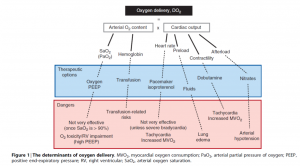
En este artículo se revisa la fisiología básica del gasto cardíaco y sus componentes para entender mejor los efectos de las alteraciones cardiovasculares en el paciente crítico y la mejor manera de tratarlo. El aporte de oxígeno (oxygen delivery, DO2) se determina por el gasto cardiaco y por el contenido arterial de oxígeno, que a su vez está determinado por la concentración de hemoglobina y por la saturación arterial de oxígeno (Figura 1).
Entendiendo el Gasto Cardíaco
El gasto cardíaco tiene cuatro determinantes: frecuencia cardíaca, contractilidad, precarga y postcarga. Para entender al paciente y el impacto combinado de estos cuatro componentes, el Dr. Vincent sugiere una simple analogía que equipara el gasto cardíaco, es decir, la cantidad de sangre bombeada por el corazón en un período de tiempo, a la velocidad de una bicicleta (Figura 2).
La frecuencia cardíaca equivale a la velocidad de pedaleo. El aumento de la frecuencia cardíaca puede afectar al llenado del ventrículo izquierdo y por tanto, reducir el volumen de eyección pudiendo ser perjudicial dado que, la frecuencia cardíaca es un determinante fundamental en la demanda de oxígeno miocárdico. La frecuencia cardiaca óptima para cada paciente es difícil de determinar ya que depende de la contractilidad intrínseca, del volumen intravascular, del estado adrenérgico y de la función diastólica.
La contractilidad depende de la fuerza muscular de la contracción. Sin embargo, la fuerza de contracción es también un determinante de las demandas miocárdicas de oxígeno y un aumento rápido puede dar lugar a fatiga, como sucede al ciclista que pedalea y tiene que reducir para finalmente detenerse.
La precarga es el grado de distensión del miocardio. Depende del volumen intravascular, de la función diastólica y del tiempo (y por tanto, de la frecuencia cardíaca).
La postcarga representa los elementos contra los cuales el ventrículo debe trabajar con el fin de extraer la sangre, y depende de la presión arterial y del tono vascular.
La Función Cardíaca en la Sepsis
En la sepsis, la presencia simultánea de taquicardia y reducción del tono vascular lleva a la reducción de la postcarga y del gasto cardíaco, y por tanto, se puede mantener o incluso aumentar. De hecho, la sepsis se asocia típicamente con un gran gasto cardiaco (estado hiperdinámico). La depresión miocárdica puede ocurrir al mismo tiempo, debido a la liberación de citoquinas y otros mediadores, algunos de los cuales están asociados con alteraciones del calcio de los miocitos cardíacos, que lleva a la reducción de la contracción miocárdica. Existe evidencia de que a mayor gravedad de la sepsis, mayor grado de vasodilatación y de depresión miocárdica. Es importante destacar que la gravedad de la depresión miocárdica está a veces oculta por la hipotensión arterial inicial (disminución de la postcarga) y se hace evidente sólo después de restaurar la presión arterial con agentes vasoconstrictores.
Distribución del Flujo Sanguíneo
En condiciones agudas, cuando el suministro de oxígeno se ve amenazado, el gasto cardiaco es redistribuido preferentemente al cerebro y al corazón. El flujo sanguíneo renal se reduce con la consiguiente disminución en la producción de orina, ayudando así a preservar el volumen sanguíneo (un efecto que se ha llamado «el éxito renal agudo»).
s esperable que en los pacientes con shock hipovolémico o cardiogénico persistente haya disminuido la perfusión esplácnica y renal, pero ocurre esto también en pacientes con shock séptico?. Varios estudios han demostrado que la perfusión hepato-esplácnica sí se encuentra alterada en los pacientes con shock séptico, y la gravedad de estas alteraciones está relacionada con el resultado. Para la perfusión renal, los datos son más escasos y los resultados están en controversia.
Alteraciones en la Microcirculación
La microcirculación desempeña un papel clave en la perfusión a nivel orgánico. Varios estudios han demostrado que la perfusión microvascular se ve alterada en la sepsis y en 4 la insuficiencia cardíaca severa, incluso cuando la circulación global se mantiene en los objetivos iniciales de la reanimación.En la sepsis, alteraciones en la perfusión microvascular renal, junto con requerimientos de oxígeno aumentados en los túbulos, puede contribuir a la insuficiencia renal, incluso cuando el total de la perfusión renal está preservada.
La Perfusión Renal: Presión versus Flujo
Para garantizar un aporte adecuado de oxígeno a los tejidos, lo primero es optimizar la presión de perfusión y posteriormente, optimizar el flujo.Restaurar o mantener una presión de perfusión suficiente debe ser, por tanto, uno de los objetivos. Restaurar un adecuado gasto urinario puede ser indicativo de un nivel de presión arterial óptima. Pero qué es un nivel óptimo? Posiblemente la respuesta esté en la variabilidad individual.
La Función Renal en la Sepsis
La sepsis es una causa común de insuficiencia renal aguda en el paciente crítico y la estabilización hemodinámica de estos pacientes a menudo no es suficiente. En contraste con las creencias anteriores de que el flujo sanguíneo renal está disminuido en la sepsis, por la vasoconstricción renal y la isquemia, la evidencia más reciente indica que el flujo sanguíneo renal suele ser mayor en modelos animales y por lo menos, normal en humanos, aunque la filtración glomerular se reduce notablemente en insuficiencia renal séptica aguda. La sepsis relacionada con la insuficiencia renal es más bien un fenómeno inmunomediado, asociado con la liberación de citoquinas, aumento en la formación de óxido nítrico, estrés oxidativo, daño mitocondrial y el aumento de apoptosis.
¿Es el Shock relacionado con la Insuficiencia Renal Aguda Protectivo?
Como el metabolismo renal es muy exigente con la necesidad de energía, algunos autores han sugerido que el cese de la función renal puede ser una adaptación para intentar mejorar el desequilibrio entre la demanda y el suministro de oxígeno de la función renal celular. De hecho, el consumo de oxígeno renal es suministrado principalmente por la reabsorción tubular de sodio, la reducción de filtración glomerular debe conducir a una reducción de la reabsorción, y por lo tanto del consumo de oxígeno renal. Este concepto es apoyado por el hecho de que la necrosis tubular aguda se observa con poca frecuencia en los pacientes con shock séptico. Sin embargo, esta idea ha sido cuestionada recientemente. En pacientes sometidos a cirugía cardíaca, el consumo de oxígeno renal resultó ser similar en los pacientes con y sin insuficiencia renal aguda, mientras que la filtración glomerular, el flujo sanguíneo renal, y la reabsorción de sodio resultaron ser inferiores en pacientes con insuficiencia renal aguda que en los pacientes con función renal normal. En pacientes con disfunción renal el consumo renal por unidad de sodio reabsorbido es el doble que en pacientes con función renal normal. Esto sugiere que la disfunción renal representa más insuficiencia renal que“ éxito renal“.
Enfoque Práctico Hemodinámico
Restauración / Mantenimiento del Volumen Sanguíneo
Lo primero es restaurar un adecuado volumen sanguíneo con la administración de líquidos. La disminución del gasto urinario es un signo de hipoperfusión renal y la restauración en la producción de orina es un objetivo importante en la insuficiencia renal aguda. La oliguria es un signo más frecuente de insuficiencia renal aguda que el aumento de creatinina. Hay pruebas concluyentes de que los diuréticos no protegen a los riñones, y alguna evidencia de que pueden tener efectos perjudiciales. Hay también evidencia de que la formación de edema, que se produce como resultado de la administración de líquidos en exceso, puede alterar la función tisular. Este concepto también se aplica a nivel renal, donde el edema puede provocar aumento de la presión intracapsular. Por tanto, es esencial evaluar cuidadosamente el estado volumétrico del paciente, a fin de evitar tanto la hipo, como la hipervolemia. Evaluar los requerimientos de líquidos no es, sin embargo, fácil. La evaluación de la frecuencia cardíaca no es sensible ni específica. En contraste con la respuesta típica de la presión arterial sobre el estado volumétrico en la insuficiencia renal crónica, la presión arterial dice muy poco sobre el estado volumétrico en el paciente crítico. Como la presión arterial está determinada por el gasto cardíaco y el tono vascular, la hipotensión arterial puede ser consecuencia de alteraciones en:
– la función cardiaca: la hipovolemia, el infarto de miocardio, arritmias severas o una obstrucción (como en la embolia pulmonar masiva o en el taponamiento cardiaco) o en – el tono vascular: la sepsis grave. Las presiones de llenado cardíaco proporcionan muy poca información en relación con el estado volumétrico del paciente. La presión venosa central puede estar elevada, incluso en presencia de hipovolemia, en pacientes con hipertensión pulmonar, como en los pacientes con enfermedad pulmonar crónica.
En última instancia, la respuesta a fluidos se caracteriza por un aumento del volumen sistólico asociado con un aumento del llenado cardíaco, que corresponde a un posicionamiento ascendente en la curva de Frank-Starling. Para los tejidos, el consiguiente aumento del gasto cardíaco incrementará el transporte de oxígeno.Se pueden utilizar varias técnicas para tratar de predecir la respuesta a fluidos. En los pacientes en ventilación mecánica, las variaciones respiratorias en el volumen sistólico o sus derivados (presión de pulso, pletismografía) se asocian con una alta probabilidad de respuesta hemodinámica a fluidos. Por desgracia, estos índices no son válidos en los pacientes con arritmias, respiración espontánea o con volumen tidal bajos, y por tanto estas técnicas sólo se pueden aplicar en determinados pacientes. Además, la perfecta coordinación con el respirador requiere sedación profunda, que es preferible evitar.La prueba de elevación pasiva de las piernas también puede ser utilizada para predecir la respuesta a fluidos, pero para ello, estos pacientes deben ser capaces de tolerar un cambio rápido en la posición del tórax (esto puede no ser el caso de algunos pacientes quirúrgicos y en pacientes con edema cerebral) y requiere el uso de una monitorización de respuesta rápida del gasto cardíaco. Aquí también, puede ser necesaria la sedación para prevenir el estrés relacionado con la estimulación simpática, lo que puede aumentar la frecuencia cardíaca y el gasto cardíaco en todas las personas, independientemente de su estado de volumen.La técnica de respuesta a fluidos detecta al paciente que responde a la administración de líquidos, y minimiza los riesgos de edema (edema pulmonar, en particular). Cuando se realiza una exposición a fluidos, deben estar definidos cuatro elementos de antemano. Se resumen mediante el acrónimo, TROL:
1- (Type of fluid)= tipo de fluido (por ejemplo, Ringer lactato).
2- (Rate of infusion) = velocidad de infusión (por ejemplo, 500 ml. en 30 min.).
3- (Objetive) = objetivo (por ejemplo, aumento de la presión arterial a 75 mmHg o la producción de orina superior a 20 ml. en 30 min.).
4- (Limits) = límites (por ejemplo, un aumento máximo de la presión venosa central de 3 mmHg sobre una basal de 12 mmHg).
Si el paciente mejora pero no se ha alcanzado el objetivo con el“ fluid challenge“ y los límites de seguridad no se rompen, puede ser repetida la administración de volumen hasta el momento en que no haya más mejoría o los límites de seguridad se excedan. Una respuesta positiva sugiere hipovolemia continua, limitando así los riesgos asociados a la sobrecarga de líquidos.
Restauración / Mantenimiento de la Presión de Perfusión
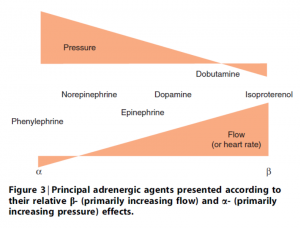
Cuando el volumen sanguíneo ha sido restaurado y la terapia de fluidos ya no es beneficiosa, son necesarios los agentes vasoactivos para restaurar /mantener la presión de perfusión. En los pacientes hipotensos, los vasopresores se deben utilizar como estrategia de primera línea. La Figura 3 se presentan los efectos de los agentes vasoactivos utilizados actualmente sobre la presión arterial y el gasto cardíaco.
Conclusión
Las alteraciones cardiovasculares en el paciente crítico son complejas y no se limitan a los estados de bajo flujo. La sepsis es una causa frecuente de insuficiencia renal en el que el flujo sanguíneo renal por lo general se conserva. En todos los casos, la optimización del volumen sanguíneo y la presión de perfusión tisular son de extrema importancia.
Bibliografía
1.- Jean-Louis Vincent y Daniel De Backer. ICU nephrology: the implications of cardiovascular alterations in the acutely ill. Kidney Int. 2011. (PubMed)