Luciano Aguilera
Jefe de Servicio de Anestesia del Hospital de Basurto. Bilbao.
Referencia Completa: Lurati Buse GA, Schumacher P, Seeberger E, Studer W, Schuman RM, Fassl J, Kasper J, Filipovic M, Bolliger D, Seeberger MD. Randomized comparison of sevoflurane versus propofol to reduce perioperative myocardial ischemia in patients undergoing noncardiac surgery. (PubMed)
Las complicaciones cardiológicas después de cirugía no cardíaca representan un importante problema en pacientes mayores de 45 años con patología arteriosclerótica o riesgo a padecerla. Se ha descrito una incidencia de infarto de miocardio en el 4% de estos pacientes, y un incremento de los niveles de troponinas en el 8% [1].
En una población de estudio con enfermedad coronaria, los autores del presente trabajo publicaron [2] un aumento significativo de las troponinas en el 16% de los enfermos y, en el 46%, hubo modificaciones electrocardiográficas compatibles con isquemia miocárdica. Diversos artículos hacen referencia a la asociación independiente de isquemia postoperatoria y efectos adversos con mortalidad a corto y a largo plazo.
Los anestésicos inhalatorios, por sus efectos de preacondicionamiento, producen en el animal de experimentación una cierta protección frente a posibles cuadros de isquemia [3]. En este sentido, trabajos clínicos preliminares sugieren un comportamiento similar [4] en lo referente a la mortalidad, aunque por el momento no pueden considerarse definitivos. Lo cual no ha impedido para que, en base a ello, se recomiende la administración de anestesia inhalatoria en pacientes hemodinámicamente estables [5] con riesgo cardiovascular para cirugía no cardiaca, a pesar de la escasez de resultados concluyentes al respecto [recomendación IIa].
Hipótesis
En base a la hipótesis que los halogenados producen el fenómeno de preacondicionamiento miocárdico, los autores diseñaron este trabajo randomizado para comparar si la incidencia de isquemia miocárdica era menor en el grupo de los enfermos anestesiados con sevoflurano frente a los que se les administraba propofol.
Incluyeron 385 pacientes, randomizándolos para recibir sevoflurano o propofol. Monitorizaron el electrocardiograma (EKG), troponinas T y péptido natriurético durante 48h. Evaluaron la presencia de delirio, y a los 6 y 12 meses contactaron para estimar efectos adversos cardiológicos.
Objetivos
El objetivo principal fue valorar, en las primeras 48 horas del postoperatorio, la incidencia de isquemia miocárdica determinada por el EKG continuo y/o elevación de las troponinas. Los objetivos secundarios (con un periodo de hasta 12 meses) consistieron en obtener las concentraciones del factor natriurético, la presencia de efectos adversos cardiológicos (isquemia miocárdica, angor inestable, insuficiencia cardíaca). Finalmente, el tercer aspecto valorado fue la presencia de delirio y la incidencia de náuseas y vómitos.
Material y métodos
No hubo diferencias en las características generales de ambos grupos (criterios de inclusión, patología previa, tratamiento, ASA, comorbilidades o tipo de cirugía). La inducción anestésica fue con etomidato, y el mantenimiento con propofol o sevoflurano. El protocolo anestésico era“ abierto“, no existían limitaciones en cuanto a la administración de opioides, bloqueantes neuromusculares, líquidos administrados, al igual que la analgesia postoperatoria.
Se monitorizó durante las primeras 48h el EKG de manera continua (la isquemia fue definida como la rectificación del ST durante más de un minuto), los niveles de troponinas T y los del factor natriurético. Para valorar los objetivos secundarios se realizó un seguimiento de hasta 12 meses.
Comentario
Comparativamente con propofol, el mantenimiento de la anestesia con sevoflurano no reducía la incidencia de isquemia perioperatoria en pacientes de alto riesgo sometidos a cirugía mayor no cardíaca (describen una incidencia de un 40%). En este sentido, encontraron una elevación de las troponinas T similar a la publicada por otros autores (26,7%). Tampoco se encontraron diferencias estadísticas en relación a una menor incidencia de efectos adversos cardiológicos, ni en las concentraciones de péptido natriurético a los 12 meses.
Trabajos recientes [6,7] tampoco han encontrado una disminución significativa de la elevación de marcadores o una reducción de los efectos adversos cardiológicos cuando se comparaban 2 grupos de enfermos anestesiados con propofol o sevoflurano. No obstante, sí se publican estudios que señalan un efecto clínicamente relevante de los inhalatorios en pacientes intervenidos de patología coronaria con circulación extracorpórea [8,9].
Los autores, en base a la ausencia de un evidencia clara desde el punto de vista clínico, cuestionan las recomendaciones [5] de la administración de inhalatorios con el fin de prevenir los efectos adversos desde el punto de vista cardiológico, máxime, considerando que no son fármacos inocuos [9].
En relación con el delirio (complicación muy poco valorada en la UCI), si bien se han descrito mecanismos de neuroprotección frente a la isquemia por parte de los halogenados [10] y la existencia de trabajos con resultados prometedores al respecto [11], en el presente trabajo no encuentran diferencias entre ambos grupos.
Los autores concluyen, pese a la descripción de una serie de limitaciones que no invalidan el trabajo (ausencia de doble ciego durante el perioperatorio, aparición de una nueva generación de troponinas T, que el tamaño de la muestra fue determinado exclusivamente para el objetivo primario, inclusión de más pacientes en el grupo del propofol) que, en su experiencia, la técnica anestésica en estos pacientes no influye en la incidencia de complicaciones cardiovasculares ni en la mortalidad después de cirugía no cardiaca.
Bibliografía
1.- Devereaux PJ, Xavier D, Pogue J, Guyatt G, Sigamani A, Garutti I, LeslieK, Rao-Melacini P, Chrolavicius S, Yang H, Macdonald C, Avezum A, Lanthier L, Hu W, Yusuf S. Characteristics and short-term prognosis of perioperative myocardial infarction in patients undergoing noncardiac surgery: a cohort study. Ann Intern Med. 2011 Apr 19;154(8):523-8. (PubMed)
2.- Filipovic M, Jeger R, Probst C, Girard T, Pfisterer M, Gurke L, SkarvanK, Seeberger MD. Heart rate variability and cardiac troponin I areincremental and independent predictors of one-year all-cause mortalityafter major noncardiac surgery in patients at risk of coronary arterydisease. J Am Coll Cardiol. 2003; 42: 1767““1776. (PubMed)
3.- Fradorf J, Huhn R, Weber NC, Ebel D, Wingert N, Preckel B, Toma O,Schlack W, Hollmann MW. Sevoflurane-induced preconditioning: impact ofprotocol and aprotinin administration on infarct size and endothelial nitric-oxide synthase phosphorylation in the rat heart in vivo. Anesthesiology. 2010; 113: 1289““1298. (PubMed) (pdf) (epub)
4. Yu CH, Beattie WS. The effects of volatile anesthetics on cardiac ischemic complications and mortality in CABG: a meta-analysis. Can JAnaesth. 2006;53:906““918. (PubMed)
5.- Fleisher LA, Beckman JA, Brown KA, Calkins H, Chaikof E,Fleischmann KE, Freeman WK, Froehlich JB, Kasper EK, Kersten JR,Riegel B, Robb JF; ACC/AHA Task Force Members, Smith SC Jr, JacobsAK, Adams CD,Anderson JL, Antman EM, Buller CE, Creager MA,Ettinger SM, Faxon DP, Fuster V, Halperin JL, Hiratzka LF, Hunt SA,Lytle BW, Nishimura R, Ornato JP, Page RL, Riegel B, Tarkington LG,Yancy CW. ACC/AHA 2007 guidelines on perioperative cardiovascularevaluation and care for noncardiac surgery: executive summary: a reportof the American College Of Cardiology/American Heart AssociationTask Force on Practice Guidelines (Writing Committee to Revise the2002 Guidelines on Perioperative Cardiovascular Evaluation for NoncardiacSurgery): developed in collaboration with the American Societyof Echocardiography, American Society of Nuclear Cardiology, HeartRhythm Society, Society of Cardiovascular Anesthesiologists, Society forCardiovascular Angiography and Interventions, Society for VascularMedicine and Biology, and Society for Vascular Surgery. Circulation. 2007;116:1971““1996. (PubMed) (pdf)
6.- De Hert SG, Longrois D, Yang H, Fleisher LA. Does the use of a volatileanesthetic regimen attenuate the incidence of cardiac events after vascularsurgery? Acta Anaesthesiol Belg. 2008; 59:19 ““25. (PubMed)
7.- Zangrillo A, Testa V, Aldrovandi V, Tuoro A, Casiraghi G, Cavenago F,Messina M, Bignami E, Landoni G. Volatile agents for cardiac protectionin noncardiac surgery: a randomized controlled study. J CardiothoracVasc Anesth. 2011; 25: 902““907. (PubMed)
8.- Bein B. Clinical application of the cardioprotective effects of volatileanaesthetics: pro-get an extra benefit from a proven anaesthetic free ofcharge. Eur J Anaesthesiol. 2011; 28: 620““622. (PubMed)
9.- Van Rompaey N, Barvais L. Clinical application of the cardioprotectiveeffects of volatile anaesthetics: con“”total intravenous anaesthesia or nottotal intravenous anaesthesia to anaesthetise a cardiac patient? Eur JAnaesthesiol. 2011; 28: 623““627. (PubMed)
10.- Yang Q, Dong H, Deng J, Wang Q, Ye R, Li X, Hu S, Dong H, XiongL. Sevoflurane preconditioning induces neuroprotection through reactiveoxygen species-mediated up-regulation of antioxidant enzymes in rats. Anesth Analg. 2011; 112: 931““937. (PubMed) (pdf)
11.- Royse CF, Andrews DT, Newman SN, Stygall J, Williams Z, Pang J,Royse AG. The influence of propofol or desflurane on postoperativecognitive dysfunction in patients undergoing coronary artery bypasssurgery. Anaesthesia. 2011;66:455““ 464. (PubMed)
Luciano Aguilera Jefe de Servicio de Anestesia del Hospital de Basurto. Bilbao. __________ Los autores declaran que el manuscrito no ha recibido financiación, no existe conflicto de intereses y no aparecen datos de pacientes. Imágenes originales propiedad de AnestesiaR, cedidas por el autor de la entrada.
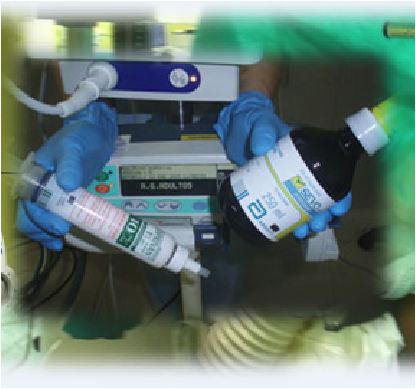
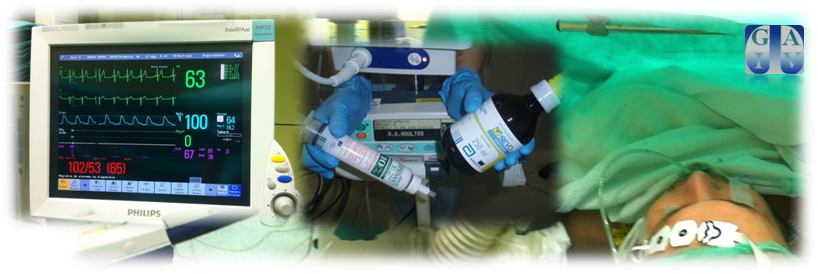

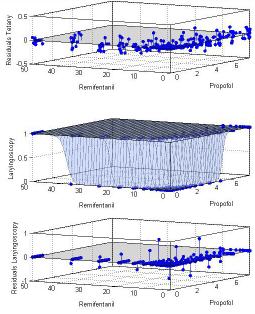

Siempre es un placer leer los artículos en AnestesiaR de GATIV. Y tan sólo por un afán constructivo en la sana discusión científica puedo exponer varios autores que no están deacuerdo con dicha afirmación.
Así mismo existen artículos y estudios a nivel clínico con humanos que parecen demostrar que el efecto de preacondicionamiento cardiaco y neuronal tiene su importancia clínica, cuando usamos halogenados .
Animo a los lectores a leerse los estudios clínicos de G D Hert sobre este tema, especialmente http://journals.lww.com/anesthesiology/Abstract/2002/07000/Sevoflurane_but_Not_Propofol_Preserves_Myocardial.7.aspx.
Puntos de vista diferentes al del artículo y que espongo para animar a los lectores a un debate sano en su medio habitual.
He leído atentamente el artículo de Lurati et al y me gustaría contribuir a la crítica del mismo, llamando la atención sobre algunos puntos del estudio.
1.- Comentarios a la población en estudio
En primer lugar, creo que los autores parten de una idea presumiblemente equivocada en cuanto a las características de los pacientes reclutados. Existen estudios que demuestran que la incidencia postoperatoria de eventos mayores adversos cardíacos (MACE) es superior en los pacientes con cardiopatía isquémica conocida que en aquellos con sólo presencia de factores de riesgo para presentarla y así, nuestro grupo , en un estudio retrospectivo de 6 años que incluyó a 526 enfermos con patología coronaria conocida o con 2 ó más factores de riesgo sometidos a cirugía mayor no cardíaca, encontró una morbilidad cardíaca postoperatoria superior en el grupo de pacientes coronarios (25,8% frente a 10.1%, p < 0,001)1, mientras que Puig-Barberá et al en un estudio prospectivo de 1.456 pacientes consecutivos sometidos a cirugía mayor programada no cardíaca encuentran también que aquellos pacientes con cardiopatía isquémica conocida tienen más riesgo de MACE postoperatorios (RR del 6.7 en pacientes con IAM, p 0.0001)2.
Por tanto, mezclar en una misma población a estudio dos subpoblaciones con diferentes riesgos sin analizarlos posteriormente por separado podría constituir un sesgo.
Por otro lado, algo similar ocurre con la edad superior a 75 años, pacientes en los que también existe un riesgo mayor de MACE1,2, por lo que también debería haberse analizado este subgrupo de forma independiente.
Además, en cuanto a la enfermedad renal crónica (ERC) de los pacientes incluidos en este estudio, sólo se ha considerado criterio de exclusión una eTFG de < 30 ml/min. El cálculo de la TFG representa un método más acertado de valoración de la función renal que la mera determinación de la creatinina3. El valor de 60 ml/min y pacientes con uno de < 30 ml/min, es decir, entre pacientes con ERC <2 y pacientes con ERC grado 3.
Por último, la cirugía vascular es la de mayor riesgo de morbimortalidad cardíaca, siendo superior a un 5%, mientras que la cirugía abdominal mayor presenta un riesgo entre 1 y 5% y la ortopédica un riesgo inferior al 1%5. De nuevo el grupo poblacional del estudio mezcla pacientes con diferentes técnicas quirúrgicas y el análisis de los resultados no determina en qué sugbrupo de tipo de cirugía se dan los MACE postoperatorios,
Quizás los resultados teniendo en cuenta estas apreciaciones con respecto a las características de los pacientes y el análisis de los subgrupos mencionados. podrían haber sido otros.
2.- Comentarios al intraoperatorio y postoperatorio
La libertad del manejo anestésico supone, a mi juicio, una gran fuente de sesgos. Del texto del artículo no se puede inferir la cantidad de fluidos administrados en un grupo y otro, así como tampoco la incidencia de eventos hemodinámicos como hipotensión, hipertensión o taquicardias (no consta, de hecho, ningún criterio definitorio de tales eventos) ni la cantidad de opiáceos utilizada en ambos grupos . Veamos a continuación la importancia de estos hechos.
La cantidad de fluidos intraoperatorios es una variable ineludible a registrar, puesto que puede ser un determinante decisivo en la aparición de complicaciones cardiovasculares postoperatorias. Y así, McArdle et al6 describen una incidencia de MACE del 40% tras cirugía abierta de reparación de aneurisma de aorta abdominal y encuentran que los pacientes con dichas complicaciones cardiovasculares presentaron un mayor balance positivo de líquidos en los días postoperatorios 0 (p < 0.01), 1 (p < 0.05), 2 (p < 0.03) y 3 (p < 0.04), teniendo además tiempos más prolongados de estancia en UCI y en el hospital. ¿Alguno de los grupos del estudio tuvo más aporte de fluidos que el otro? No podemos saberlo.
Que los episodios de inestabilidad hemodinámica, bien sea hipertensión y taquicardia (intubación endotraqueal, estimulación quirúrgica) o hipotensión (hemorragia, compresión de cava…) se asocian a eventos isquémicos intraoperatorios es un hecho ya consabido desde hace mucho tiempo y demostrado en muchos estudios, como por ejemplo el de Slogoff et al7. El trabajo que nos ocupa no hace mención a tales alteraciones hemodinámicas y es difícil imaginar grandes cirugías vasculares sin la concurrencia de las mismas. En mi opinión, cualquier estudio que se precie y trate de evaluar la incidencia de MACE postoperatorios, debería recoger estas variables e incluirlas dentro de los análisis multi o univariantes.
Por otro lado, al no conocer las dosis de opiáceos utilizadas intraoperatoriamente o como parte del régimen analgésico postoperatorio, también se desconoce si el consumo fue mayor en alguno de los grupos. Y es un hecho demostrado ya que la unión de los opioides a sus receptores (δ, κ y µ) sirve de trigger para la puesta en marcha de vías de señalización comunes con las activadas por el condicionamiento isquémico, protegiendo contra la isquemia y reperfusión miocárdica8,9.
3.- Comentarios a la discusión: «precondicionamiento y condicionamiento remoto»
Creo que este tercer punto sería el más importante. Como bien dice el profesor Berthold Bein en una magnífica revisión10, un requisito impresecindible para que se pueda registrar diferencias en el daño celular miocárdico es que la isquemia durante la cirugía sea de suficiente magnitud como para producir cantidades medibles de marcadores bioquímicos de dicho daño (troponina). Es decir, sin isquemia miocárdica intensa no hay ni posibilidad ni resultado clínico alguno de cardioprotección. Y en este sentido, la discusión que Lurati et al desarrollan en su trabajo está basada en la acción cardioprotectora de los agentes volátiles en cirugía cardíaca. Y la pregunta, cuya respuesta es obvia, sería: «¿es de igual intensidad la isquemia miocárdica que pueda producirse en cirugía no cardíaca que la ocurrida en el seno de una cirugía cardíaca?». Pues evidentemente no. Y es bueno recordar ahora los diferentes tipos de condicionamiento isquémico11:
Precondicionamiento clásico (CP): aquél realizado antes del evento isquémico y con efecto protector 2 » 3 horas después de la isquemia.
Precondicionamiento segunda ventana (SWOP): aquél realizado antes del evento isquémico y con efecto protector desde 12 » 24 horas después de la isquemia hasta 2 ó 3 días después.
Postcondicionamiento: aquél realizado tras la isquemia, desde el inicio de la reperfusión o más tardíamente.
Condicionamiento: aquél que incluye el uso tanto del precondicionamiento como el del postcondicionamiento.
Condicionamiento remoto: aquél realizado antes del evento isquémico de un órgano diferente al corazón y que puede tener efecto protector miocárdico.
No voy a entrar aquí en la discusión del efecto cardioprotector de los volátiles en cirugía cardíaca, porque el artículo de Lurati et al no versa sobre este tipo de cirugía, ni versa sobre el precondicionamiento miocárdico en cirugía no cardíaca, ya que en este tipo de cirugía, la isquemia de suficiente intensidad como para producir daño celular se produce en órganos no cardíacos (riñón, miembros inferiores, pulmón, hígado…) caso de producirse, puesto que no en toda cirugía abdominal mayor acontece por la técnica un isquemia orgánica. Es decir, de lo que debe versar la discusión del artículo de Lurati et al es del precondicionamiento remoto, condicionamiento (isquémico) que ha sido demostrado ya tras cirugía electiva de reparación de aneurisma de aorta abdominal12.
Una de las características del precondicionamiento isquémico es el fenómeno de la tolerancia cruzada, es decir, estímulos no isquémicos pueden producir tolerancia celular a una isquemia intensa subsiguiente. Esta es la base del precondicionamiento farmacológico producido por los anestésicos inhalatorios13. Igualmente el condicionamiento remoto podría presenter el fenómeno de tolerancia cruzada y de acuerdo con esta idea, se ha descrito en ratas un efecto protector del precondicionamiento y postcondicionamiento del sevoflurano sobre la lesión miocárdica inducida por la lesión por isquemia » reperfusión de la aorta infrarrenal14.
Es cierto que en clínica humana no se ha demostrado todavía la existencia de este efecto protector del precondicionamiento remoto con los agentes anestésicos inhalatorios en cirugía no cardíaca, pero en mi opinión los estudios que pretendan demostrarlo no deben tener sesgos como los comentados hasta ahora, es decir:
Deben comparar grupos de riesgo iguales, sin mezclar cirugías que conlleven isquemia visceral con aquellas que no la impliquen.
Deberían basarse en protocolos de precondicionamiento de órganos no cardíacos más estrictos siguiendo, al menos por ahora, los protocolos de precondicionamiento miocárdico que han demostrado eficacia en cirugía cardíaca (dosis altas de inhalatorio, dos ciclos con su «wash out» mejor que un ciclo de administración continua…).
Cumpliendo primero el objetivo hemodinámico de la estabilidad, registrando y analizando los episodios de taquicardia, hipertensión e hipotensión, con un protocolo también estricto anestésico y nunca abierto.
Sólo entonces, los resultados de tales estudios podrían considerarse definitivos. Indudablemente, con estas consideraciones en mente, se abre ante nosotros un mundo apasionante de investigación clínica en el campo de la anestesia inhalatoria independientemente de lo que pudiéramos encontrarnos al final del camino.
REFERENCIAS
1.- De la Cruz C, Estecha MA, Cruz J, Castillo A, Palma F. Morbimortalidad cardíaca postoperatoria en pacientes ancianos de alto riesgo intervenidos de cirugía mayor no cardíaca. Rev Esp Anestesiol Reanim 1999; 46: 4 » 8
2.- Puig-Barberá J, Márquez-Calderón S, Vila-Sánchez M. Complicaciones cardiacas en cirugía mayor programada no cardiaca: incidencia y factores de riesgo. Rev Esp Cardiol 2006; 59: 329 » 337
3.- K/DOQI clinical practice guidelines for chronic kidney disease: evaluation, classification, and stratification. Am J Kidney Dis 2002; 39 (Suppl 1): S1 – 266
4.- Kertai MD, Boersma E, Bax JJ, van den Meiracker AH, van Urk H, Roelandt JR,
Poldermans D. Comparison between serum creatinine and creatinine clearance
for the prediction of postoperative mortality in patients undergoing major vascular
surgery. Clin Nephrol 2003; 59: 17 » 23
5.- Poldermans D, Bax JJ, Boersma E et al. Guidelines for pre-operative cardiac risk assesment and perioperative cardiac management in non-cardiac surgery. The Task Force for Preoperative Cardiac Risk Assesment and Perioperative Cardiac Management in Non-cardiac Surgery of the European Society of Cardiology (ESC) and endorsed by the European Society of Anaesthesiology (ESA). Eur Heart J 2009; 30: 2769 » 2812
6.- McArdle GT, Price G, Lewis A, Hood JM, McKinley A, Blair PH et al. Positive fluid balance is associated with complications after elective open infrarenal abdominal aortic aneurysm repair. Eur J Vasc Endovasc Surg 2007; 34: 522 – 527
7.- Slogoff S, Keats AS. Does perioperative myocardial ischemia lead to perioperative myocardial infarction? Anesthesiology 1985; 62: 107 – 114
8.-Wong GT, Huang Z, Irwin MG. Remifentanil reduces the release of biochemical markers of myocardial damage after coronary artery bypass surgery: a randomized trial. J Cardio Vasc Anesth 2010; 59: 194 » 197
9.- Yellon DM, Downey JM. Preconditioning the myocardium: from cellular physiology to clinical cardiology. Physiol Rev 2003: 83: 1113 – 1151
10.- Berthold B. Clinical application of the cardioprotective effects of volatile anaesthetics: PRO » get an extra benefit from a proven anaesthetic free of charge. Eur J Anaesthesiol 2011;28:620″622
11.- Hausenloy DJ, Yellon DM. Preconditioning and postconditioning: underlying mechanisms and clinical application. Atheroesclerosis 2009; 204: 334 » 341
12.- Ali ZA, Challagan CJ, Lim E, Ali AA, Reza SA, Akthar AR et al. Remote ischemic preconditioning reduces myocardial and renal injury after elective abdominal aortic aneurysm repair. Circulation 2007; 116 (Suppl I): I-98 – I-105
13.- Minguet G, Joris J, Lamy M. Preconditioning and protection against ischaemia » reperfusion in non » cardiac organs: a place for volatile anesthetics? Eu J Anaesthesiol 2007; 24: 733 – 745
14.- China papers. The Protective Effect of Sevoflurane Preconditioning and Postconditioning on Infrarenal Aorta Ischemia-reperfusion Induced Myocardial Injury in Rat. http://mt.china-papers.com/2/?p=244347
Por un fallo en el envío de mi anterior comentario la parte refernte a la enfermedad renal crónica ha quedado cortada, por lo que la reenvío con el fin de que quede completa (pido disculpas por este fallo de envío). El comentario correcto de esta parte sería éste:
«Además, en cuanto a la enfermedad renal crónica (ERC) de los pacientes incluidos en este estudio, sólo se ha considerado criterio de exclusión una eTFG de < 30 ml/min. El cálculo de la TFG representa un método más acertado de valoración de la función renal que la mera determinación de la creatinina3. El valor de 60 ml/min y pacientes con uno de < 30 ml/min, es decir, entre pacientes con ERC <2 y pacientes con ERC grado 3"
Excelente Carlos! Un beso
Excelente comentario. Enhorabuena
Querido Dr De la Cruz,
Antes de nada, me gustaría agradecerte tu comentario en esta entrada. Ha sido una crítica muy bien estructurada y con un mensaje subliminal muy importante. Es una opinión personal, pero considero que sin una rigurosa metodología de trabajo, cualquier estudio puede llegar a conclusiones finales erróneas y aún así aceptadas como dogmas de fe por la sociedad médica. En ocasiones, es debido a una estadística abrumadora más o menos dirigida a demostrar la hipótesis de trabajo y en otras, a una alta sensibilidad a ser influidos por el «impact factor» o el autor de la revista en cuestión. Tampoco hay que olvidar, nuestra relativa inexperiencia en leer artículos con rigor científico. A lo largo de nuestra carrera profesional, nos enseñan poco a valorar crítica y constructivamente los trabajos de investigación. Así es que te lo agradezco doblemente.
Creo que la línea que separa la Inhalatoria de la TIVA es más fina de lo que suponemos. Como hemos dicho en múltiples ocasiones, todavía no contamos con el agente anestésico ideal que supere todas las ventajas e inconvenientes de los otros fármacos. No podemos ser categóricos ya que no disponemos de la información absoluta de cómo ese anestésico trabaja en nuestro organismo y en nuestro cerebro. La farmacocinética, farmacodinámica, farmacogenética, variabilidad interindividual y el estado funcional del paciente son algunos de los factores que pueden modificar el resultado final de dichos fármacos. En base a esto, cualquier búsqueda en la literatura científica nos conducirá a un sinfín de artículos que nos muestran las bondades de la TIVA y otros los beneficios de la inhalatoria. Pero una vez más, el comentario del Dr De la Cruz es muy importante.
Cómo ejemplo:
1. A comparison of volatile and non volatile agents for cardioprotection during on-pump coronary surgery. Dr Hert.
http://s3.amazonaws.com/publicationslist.org/data/jan.mulier/ref-154/Comparison%20of%20volatile%20agents%20for%20cardioprotection.pdf
Y la respuesta al autor:
http://www.respond2articles.com/ANA/forums/392/ShowThread.aspx
La conclusión es que no hay una elección farmacológica definitiva.
2. Differential Effects of Propofol and Sevoflurane on Ischemia-induced Ventricular arrhythmias and Phosphorylated Connexin 43 Protein in Rats
http://journals.lww.com/anesthesiology/pages/articleviewer.aspx?year=2009&issue=01000&article=00014&type=fulltext
Y la respuesta al autor:
http://journals.lww.com/anesthesiology/fulltext/2009/08000/propofol_and_cardioprotection_against_arrhythmias.40.aspx
La conclusión es que podría seguirse por esa línea de investigación.
3. The effects of interrupted or continuous administration of sevoflurane on preconditioning before cardio-pulmonary bypass in coronary artery surgery: comparison with continuous propofol
http://onlinelibrary.wiley.com/doi/10.1111/j.1365-2044.2008.05563.x/pdf
Conclusión: el mismo fármaco (Sevoflurane ) según cómo y en qué momento se administre puede variar sus efectos cardioprotectores
Lo que sí es cierto, es que debates de este tipo son importantes y muy necesarios.
Dra Anna Abad
Vicepresidente Grupo Nacional de Anestesia Total Intravenosa (GATIV)
Dr.de la Cruz.o seu comentario é uma aula de Anestesiologia,Dra. Ana deu nos uma aula de pesquisa na net.Obrigado aos dois.
Soy médico Anestesiologo recién egresado, hice mi tesis en TIVA y siento que a este estudio le hace falta más detalle, no todos los pacientes llegan a un plano anestésico adecuado con las mismas concentraciones en plasma o en sitio efecto de propofol, a consecuencia los efectos adversos del medicamento, hipo tensión, apnea, etc, pacientes jóvenes requieren más dosis, u otros factores como el tabaco, sexo, son cosas que notamos en el transcurso de los años de estudio, siento que deberían realizar grupos individuales de estudio, x edad, sexo, tipo de cirugía y llevar un registro con signos vitales cada 2 minutos Después de 15 min cada 5 min el registro, después valorar concentraciones en plasma y sitio efecto, y si hubo bajas de los signos vitales tomar estudio de cardiología, comparara también con BIS, y anotar el total de dosis por paciente, y anotar el Modelo farmacocinetico empleado, es mucho detalle pero apenas así , en lo personal confiaría en los resultados, les repito, soy recién egresado, soy un simple Anestesiologo que le gustó la anestesia intravenosa, saludos