 ílvaro Ramiro *, Pablo Troncoso **, Ernesto Martínez-García **, José Ramón Villa ***
ílvaro Ramiro *, Pablo Troncoso **, Ernesto Martínez-García **, José Ramón Villa ***
Introducción
Las Mucopolisacaridosis (MPS) engloban un conjunto de desórdenes en el almacenaje celular lisosomal y se asocia al acúmulo de glucosaminoglicanos (GAG) en órganos y tejidos (1). La organomegalia, la disostosis múltiple, las valvulopatías, el retraso metal y del crecimiento, y la inestabilidad cervical son hallazgos frecuentes de estas entidades (1,2). El manejo de la vía aérea en estos pacientes puede suponer un reto para el anestesiólogo debido a alteraciones tanto anatómicas como fisiológicas.
Caso clínico
Un niño de 6 años y 13 Kg. de peso, diagnosticado de Síndrome de Maroteaux-Lamy (MPS tipo VI) es programado para extracción dental múltiple por policaries. En la exploración física presenta biotipo gargóleo y pectum carinatum. Entre sus antecedentes destacan enfermedad de Von Willebrand y adenoamigdalectomía. Se encuentra en tratamiento enzimático con Galsulfasa, siendo portador de un acceso central.
En la consulta de preanestesia se comprueba la correcta movilidad de la articulación temporomandibular, evidenciándose una buena apertura bucal, macroglosia y Mallampati IV. En todos los registros consta correcta ventilación con mascarilla facial y laríngea, sin evidenciarse dificultad. Presenta una laringoscopia previa con una puntuación de III/IV en la clasificación de Cormack-Lehane.En esa ocasión a pesar de la mala visión, la intubación se llevó a cabo con laringoscopia directa sin requerir otros dispositivos. Además de las pruebas complementarias de rutina, se solicitó un nuevo estudio polisomnográfico, siendo sugestivo de un patrón obstructivo y Síndrome de Apnea Obstructiva del Sueño (SAOS) severo. Asimismo, se realizó un nuevo estudio ecocardiográfico, a pesar de encontrarse asintomático desde el punto de vista cardiológico en el momento actual, evidenciándose un prolapso mitral ya conocido con Insuficiencia Mitral (IM) leve-moderada.
Se administró en planta Atropina a dosis de 0,01 mg.Kg-1 i.v. como antisialogogo junto a factor de Von Willebrand a través de un Port-a-cadh. En quirófano, se procede a monitorizar al paciente con ECG, presión arterial no invasiva y pulsioximetría. Se indujo al paciente con sevoflurano al 8% con el objetivo de alcanzar un plano anestésico muy profundo para poder manipular la vía aérea de forma segura, preservando la ventilación espontánea. Una cuidadosa laringoscopia fue realizada sin hiperextensión cervical, constatándose una mala visión de estructuras, identificando únicamente una epiglotis rígida no movilizable. Se insertó una mascarilla laríngea (ML) desechable Ambú Aura-i # 2,5, y ésta se conectó a su vez a un codo Swivel, permitiendo así mantener la vía aérea permeable y mantener un plano anestésico profundo al introducir el fibrobroncoscopio.
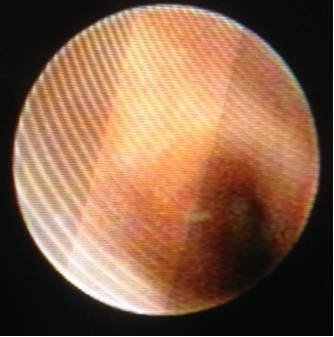
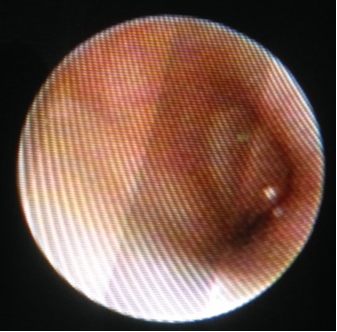
Una vez comprobada una buena ventilación con auscultación y capnografía, se realizó una primera fibroscopia (Olympus BF 2,8 mm) a través de la ML. El avance hacia la glotis se llevó a cabo con mucha dificultad debido a la rigidez de la epiglotis. A nivel subglótico se observa un compromiso del tercio inferior de la luz traqueal, siendo un hallazgo frecuente de esta enfermedad (figuras 1 y 2). Se infiltró lidocaína al1% sobre y bajo las cuerdas vocales (1,5 mg.Kg-1).
Bajo la visión fibroscópica de la glotis, se avanzó en primer lugar una guía metálica (Terumo GR3501 Radiofocus Guide Wire; 035″ x 150cm x 3cm) a través del canal de trabajo, con el propósito de servir de fiador para un catéter intercambiador de Cook (11 Fr; 2.3 mm ID, Cook Medical Incorporated, Bloomington, IN USA). Una vez en la luz traqueal se progresó un tubo endotraqueal (TET 4,5 mm. ID) montado sobre el intercambiador a través de la ML. Sin embargo, al retirar el dispositivo supraglótico se produjo una extubación accidental, a pesar de utilizar un TET más pequeño a modo de estabilizador o prolongador. Por ello, tras ventilación manual con mascarilla facial, la ML fue recolocada con éxito.
En este punto, con la impresión de que un TET del 4,5 era apropiado ya que su diámetro era menor que el de la estenosis subglótica y que éste era progresable hacia el tercio distal de la tráquea sin producir trauma en la vía aérea, decidimos montarlo directamente sobre el fibrobroncoscopio. Una vez visualizada la carina el tubo endotraqueal se progresó a través del fibrobroncoscopio, intubándose el paciente por segunda vez. En esta ocasión la retirada de la mascarilla laríngea no produjo la salida accidental del tubo.
Durante el procedimiento se aseguró el mantenimiento anestésico con la administración continua de sevoflurano y un alto flujo de oxígeno al 100% a través de la ML para evitar reactividad de la vía aérea y/o un posible episodio de desaturación. La cirugía transcurrió sin incidencias con el paciente en ventilación espontánea sin relajación neuromuscular.
Al término de la cirugía se administraron dosis tituladas de remifentanilo hasta 1 µg.Kg-1, con el objetivo de profundizar al paciente y disminuir la reactividad de la vía aérea sin perder la ventilación espontánea,permitiendo así extubar al pacinte lo más despierto posible. El paciente fue trasladado a Reanimación con oxigenoterapia sin transcurrir complicaciones en el postoperatorio inmediato.
Discusión
El acúmulo de GAG en la vía aérea superior puede producir macroglosia, hipertrofia adenoamigdalar y laxitud o rigidez de los tejidos blandos de la laringofaringe, produciendo su colapso (2). La obstrucción de la vía aérea puede tener lugar a múltiples niveles. El depósito de MPS en la mucosa traqueal puede asociarse a obstrucción y traqueo-broncomalacia. Múltiples anormalidades pueden comprometer la ventilación de estos pacientes. La reducción en la capacidad vital (CV) producida por alteraciones morfológicas en la caja torácica, tales como cifoscoliosis o pectum carinatum, es un ejemplo de ello. Esto, sumado al compromiso mecánico del diafragma por organomegalias, contribuye a que estos pacientes a menudo desarrollen una enfermedad restrictiva pulmonar (1,2). La disfunción respiratoria frecuentemente tiene también un componente obstructivo, siendo un diagnóstico habitual el síndrome de Apnea del Sueño (SAOS) (2). Las secreciones respiratorias son abundantes y espesas, lo que puede dificultar la fibroscopia. Respecto a las alteraciones óseas, es de especial relevancia la hipoplasia de la apófisis odontoides, condicionando inestabilidad cervical con riesgo de compresión medular especialmente en los tipos IV y VI de la enfermedad (2).
Como en todo caso de Vía Aérea Difícil (VAD), la concepción previa de un plan de actuación es fundamental. En este caso, tratándose de un caso de MPS, las características propias de este grupo de enfermedades nos orientaban no sólo hacia una hipotética dificultad de intubación, sino hacia una posible dificultad de ventilación (1, 2, 3). Por ello, las acciones llevadas a cabo se fundamentaron en mantener la ventilación espontánea y en asegurar una correcta oxigenación y aporte de agente hipnótico.
La inducción inhalatoria con agentes halogenados sin la administración de relajantes musculares es considerada por algunos autores de elección en el manejo de la VAD para conseguir un plano anestésico adecuado (evitando así la irritación de la vía aérea), sin compromiso de la ventilación espontánea (4). Existen múltiples agentes intravenosos de acción corta que suponen una alternativa, tales como propofol en perfusión con/sin remifentanilo o la ketamina en bolos de 0,5 mg.kg (1, 4).
En este caso, el alto riesgo de sangrado debido a la necesidad de extraer múltiples piezas dentarias en el contexto de un paciente con enfermedad de Von Willebrand fue un factor determinante para decidir intubar al paciente en lugar de ventilarlo a través de una ML.
Recientemente, se han actualizado las guías clínicas para el manejo de la VAD de la Sociedad Americana de Anestesiología (5). En ellas la mascarilla laríngea intubadora (ILMA) tiene un papel destacado debido a su doble utilidad como herramienta para ventilar e intubar, ya sea a ciegas o sirviendo como guía al fibrobroncoscopio.
A pesar de su actualización, la guía americana no ha realizado hasta el momento un algoritmo específico de manejo de VAD en el paciente pediátrico a diferencia de otras sociedades, como la del Reino Unido o la catalana a nivel nacional. En ellas se refleja el auge en el que se encuentra la técnica de intubación bajo visión fibroscópica a través de ML en caso de vía aérea difícil esperable en pediatría (4,6,7). Esto se debe a que la técnica de intubación a ciegas a través de ML no está recomendada en este tipo de pacientes (4,5). Además, existen publicaciones que atribuyen mayor tasa de éxito y menor tiempo de intubación cuando la fibroscopia se realiza a través de una ML respecto a una cánula orofaríngea modificada (Williams) (5). Por último, otra ventaja de esta técnica es la posibilidad de ventilación continua al manipular la vía aérea a través de la ML y mantener un plano hipnótico profundo.
En un caso de MPS, inicialmente se desconoce el calibre real de la tráquea. Decidimos tomar como plan inicial de intubación la técnica de Seldinger con guía e intercambiador, ya que es un método que permite progresar, de manera rápida y poco traumática, tubos de diferentes tamaños.
El riesgo de extubación accidental al retirar la ML una vez posicionado el tubo en la luz traqueal está reportado en la literatura, y se han descrito diferentes métodos para evitar que esto suceda (8). Aumentar la longitud del tubo con un prolongador o estabilizador es uno de ellos. La ILMA Fastrach® presenta un elongador específico, pero no se encuentra disponible para pacientes con un peso inferior a 30 Kg., siendo la número 3 la más pequeña hasta el momento (8). Por eso utilizamos un TET más pequeño para este fin. Mantener el catéter intercambiador de Cook o progresar una guía metálica a través del canal de trabajo del fibrobroncoscopio son otras técnicas descritas que podrían haber permitido una rápida reintubación en caso de salida inesperada del TET (9). En el estudio de Muhlebach et al. realizado en 31 pacientes diagnosticados de MPS los hallazgos fibroscópicos más frecuentes en 105 procesos anestésicos son: depósitos de GAG e hipertrofia amigdalar en un 72%, y laringomalacia en un 31%. Los depósitos en vía aérea inferior y traqueobroncomalacia como en nuestro caso se dan en el 46% (3). Por ello, evitamos realizar algún intento de intubación con laringoscopia directa u otro dispositivo y realizamos la fibrobroncoscopia de entrada, con el fin de producir el mínimo trauma sobre la vía aérea.
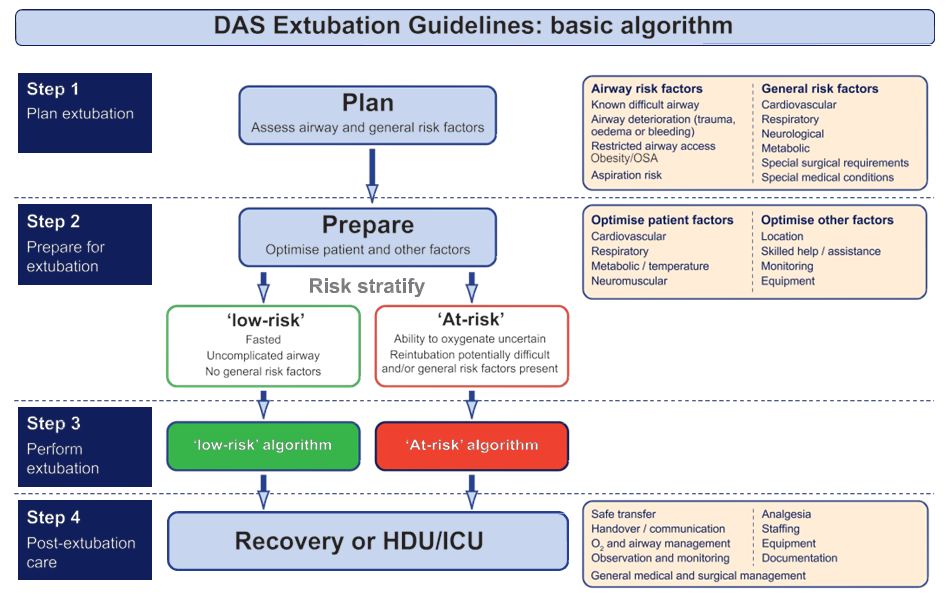
En el contexto de manejo de este caso de VAD esperable es fundamental el proceso de extubación. Siguiendo las guías de extubación de la Sociedad de VAD del Reino Unido consideramos este paciente“ at risk“ (de riesgo), por lo que optamos por realizar el procedimiento tras una completa recuperación de la consciencia en pleno estado de alerta (10).
La presencia del TET puede producir tos y espasmos en la vía aérea durante la educción anestésica (7,10). Los efectos supresores de la tos y la capacidad de atenuar los cambios cardiovasculares en la extubación de los opioides son conocidos desde hace años (10). Como ya hemos mencionado, las infusiones de remifentanilo han sido descritas como método de sedación para el manejo de la VAD (4). Decidimos administrar este agente porque es un modo de evitar efectos adversos en la vía aérea a la vez que permite mantener la ventilación espontánea. La técnica de extubación con remifentanilo está descrita en estas guías clínicas.
Conclusiones
La necesidad de cirugía en el caso de un paciente de mucopolisacaridosis supone un reto incluso para el anestesiólogo más experimentado. Afrontar el manejo de la vía aérea de estos pacientes requiere la confección de un plan exhaustivo y un abordaje multidisciplinar para disminuir al máximo las complicaciones potenciales. El aspecto fundamental de esta estrategia es mantener la ventilación espontánea bajo un plano anestésico profundo. La intubación asistida por fibroscopia a través de dispositivos supraglóticos se encuentra en auge en pediatría.
Bibliografía
1.- Berger KI, Fagondes SC, Giugliani R, Hardy KA, Lee KS, McArdle C, et al. Respiratory and sleep disorders in mucopolysaccharidosis. J Inherit Metab Dis. 2013 Mar; 36(2):201-10. (PubMed)
2.- Walker R, Belani KG, Braunlin EA, Bruce IA, Hack H, Harmatz PR, et al. Anaesthesia and airway management in mucopolysaccharidosis. J Inherit Metab Dis. 2013 Mar; 36(2):211-9. (PubMed)
3.- Muhlebach MS, Shaffer CB, Georges L, Abode K, Muenzer J. Bronchoscopy and airway management in patients with mucopolysaccharidoses (MPS). Pediatr Pulmonol. 2013 Jun;48(6):601-7. (PubMed)
4.- Andreu E, Schmucker E, Drudis R, Farré M, Franco T, Monclús E; Grupo SEVA. Algoritmo de la vía aérea difícil en pediatría. Rev Esp Anestesiol Reanim. 2011 May;58(5):304-11. (PubMed)
5.- Apfelbaum JL, Hagberg CA, Caplan RA, Blitt CD, Connis RT, Nickinovich DG; American Society of Anesthesiologists Task Force on Management of the Difficult Airway. Practice guidelines for management of the difficult airway: an updated report by the American Society of Anesthesiologists Task Force on Management of the Difficult Airway. (PubMed)
6.- Barch B, Rastatter J, Jagannathan N. Difficult pediatric airway management using the intubating laryngeal airway. Int J Pediatr Otorhinolaryngol. 2012 Nov;76(11):1579-82. (PubMed)
7.- S Ramesh, R Jayanthi, and SR Archana. Paediatric airway management: What is new?. Indian J Anaesth. 2012 Sep-Oct; 56(5): 448““453. (PubMed)
8.- Gerstein NS, Braude DA, Hung O, Sanders JC, Murphy MF. The Fastrach Intubating Laryngeal Mask Airway: an overview and update. Can J Anaesth. 2010 Jun;57(6):588-601. (PubMed)
9.- Choi EK, Kim JE, Soh SR, Kim CK, Park WK. Usefulness of a Cook® airway exchange catheter in laryngeal mask airway-guided fiberoptic intubation in a neonate with Pierre Robin syndrome -A case report-. Korean J Anesthesiol. 2013 Feb;64(2):168-71. (PubMed)
10.- Difficult Airway Society Extubation Guidelines Group, Popat M, Mitchell V, Dravid R, Patel A, Swampillai C, Higgs A. Difficult Airway Society Guidelines for the management of tracheal extubation. Anaesthesia. 2012 Mar;67(3):318-40. (PubMed)
ílvaro Ramiro *, Pablo Troncoso **, Ernesto Martínez-García **, José Ramón Villa **** Unidad de Anestesia, Reanimación y Cuidados Críticos. Hospital Universitario Fundación Alcorcón.
** Unidad de Anestesia y Reanimación. Hospital Infantil Universitario Niño Jesús.
*** Servicio de Neumología. Hospital Infantil Universitario Niño Jesús.


Hola
He leído con interés el artículo presentado. Felicito a los autores por el artículo y porque dichos pacientes son de extremo riesgo y su manejo debe ser cuidadosamente medido.
Respecto a la técnica, quisiera hacer varias reflexiones. Hablan de una intubación con un tubo de 4,5 mm. Parece lógico utilizar un fibroscopio pediátrico (3,7 mm) y no realizar manipulaciones a ciegas. Las malformaciones asociadas a esta patología hacen que la mucosa sea muy friable y de fácil sangrado por su infiltración por GAG. La existencia de un cuello corto y la limitación para la extensión cervical por la rigidez cervical y la posible existencia de una malformación en la odontoides, hacen que deba considerarse como una glotis muy anterior y el ángulo que debe seguir el intercambiador sea muy pronunciado, con un alto riesgo de que arrastre la guía metálica a esófago en lugar de introducirse en la tráquea. No alcanzo comprender el motivo del uso del intercambiador, disponiendo de un fibroscopio de 2,8, ya que su diámetro externo es similar, y su introducción implica la retirada del fibroscopio. Parece lógico introducir el fibroscopio en la traquea y hacer progresar el tubo como se realizó en la parte final de la maniobra
La intención de mi comentario, es simplemente alertar sobre las dificultades técnicas de este procedimiento, algunas de sus posibles complicaciones, y recordar que el manejo en dichos pacientes de la VAD requiere una amplia experiencia.
En relacion a la eleccion de intubar directamente con el tubo montado en el fibroscopio o usando primero guia metalica e intercambiador: En nuestro centro hemos estado usando el «enfoque» y técnica preconizada por el hospital de niños de Manchester. Probablemente el enfoque usado por ellos está sesgado porque ellos tienen un pool de pacientes muy amplio (gran gama de edades) con pacientes ya mas mayores y evolucionados en que el tema de la estenosis de via aérea baja es critica y su manejo mas difícil. En esos casos la opcion del intercambiador permite hacer una sola fibroscopia (avanzar guia e intercambiador) y luego probar hasta que entre el tubo del tamaño que sea para ese paciente en particular. En nuestro centro tenemos niños por ahora relativamente jóvenes y probablemente se pueda «acertar» a la primera montando un tubo relativamente fino con balon sobre el fibro, que es otro enfoque igualmente válido, usado por otros grupos. En buena parte la eleccion de técnica va a depender de la experiencia del operador y del plan anestésico trazado. Nuestra experiencia en el manejo de estos niños es relativamente corta (ha habido un auge reciente en la cantidad de niños con mucopolisacaridosis, debido a la aparicion de terapias enzimáticas o trasplante de médula ósea, que han aumentado el número de estos niños que pasan por quirófano). Y nuestro enfoque trata de ser muy «conservador». Empezamos con la técnica de Manchester pero esperamos que según ganemos más experiencia podremos ampliar el abanico de opciones de manejo de vía aérea.
Muchas gracias por el comentario y el interés en el caso. Un saludo.
En primer lugar Dr Monclus muchas gracias por haber encontrado interés en este case report. No puedo estar más de acuerdo con usted en que el manejo de este tipo de pacientes es extraordinariamente complejo y requiere un plan de actuación preciso. Tal como ha mencionado, no realizamos manipulaciones a ciegas, tan sólo hicimos una laringoscopia directa cuidadosa sin hiperextensión cervical para reportar en la historia el grado en la escala Cormack Lehane modificada. Atendiendo a su pregunta, incluimos en nuestro plan de actuación el intercambiador porque desconocíamos el grado de estenosis traqueal y por tanto no sabíamos que número de tubo endotraqueal admitiría exactamente. Una vez progresado el intercambiador de Cook, nos planteamos q
Perdón continúo aquí
Una vez progresado el intercambiador de Cook, nos planteamos que sería posible progresar cuidadosamente un TET de un cierto calibre. En el caso que de que éste no sobrepasase la estenosis así podríamos progresar otro de un calibre menor ocasionando el menor trauma posible. El motivo de progresar la guía metálica fue poder realizar la maniobra bajo visión directa a través del canal de trabajo del fibrobroncoscopio flexible. Entiendo su planteamiento, de hecho, cuando progresamos la guía metálica y nos disponiamos a fiar el intercambiador se produjo una salida accidental de la misma y finalmente realizamos la intubación bajo visión directa fiando el tuboendotraqueal con el fibrobroncoscopio. Pero dimo este paso porque ya habíamos observado la estenosis y objetivamente sabíamos que el tubo elegido salvaría el compromiso de la luz traqueal sin traumatizar la mucosa.
Muchas gracias