Fraile JR (1), García Quiroga R (2), Montoro J (3), De la Fuente E (2), Martínez Meco L (3)
(1) Jefe de Servicio de Anestesiología. Hospital General Universitario de Guadalajara. España
(2) FEA Anestesiología. Hospital General Universitario de Guadalajara. España
(3) MIR Servicio de Anestesiología. Hospital General Universitario de Guadalajara. España
Justificación y objetivos
La intubación fibróptica (IFO) es actualmente una técnica esencial para el manejo de la vía aérea difícil (VAD), especialmente en cirugía planificada (1). Sin embargo, la implementación de este recurso en un hospital general, y su incorporación a la práctica clínica, presenta importantes dificultades económicas, técnicas, organizativas y de formación del personal facultativo y auxiliar. Aunque son numerosos los estudios de control de calidad de la técnica en eficacia y seguridad (2, 3), no hemos encontrado referencias que analicen el proceso de implementación y los resultados para la organización quirúrgica. Asumir plenas competencias en este campo es un objetivo básico para los servicios de anestesiología, con objeto de evitar la dependencia de otros servicios clínicos (neumología, otorrinolaringología, cirugía torácica), y mejorar la organización, la eficiencia y la seguridad del bloque quirúrgico.
Objetivo: describir el proceso de implementación de la IFO, la práctica clínica y analizar los resultados obtenidos en el Hospital General Universitario de Guadalajara (España) tras los dos primeros años de su desarrollo.
Material y métodos
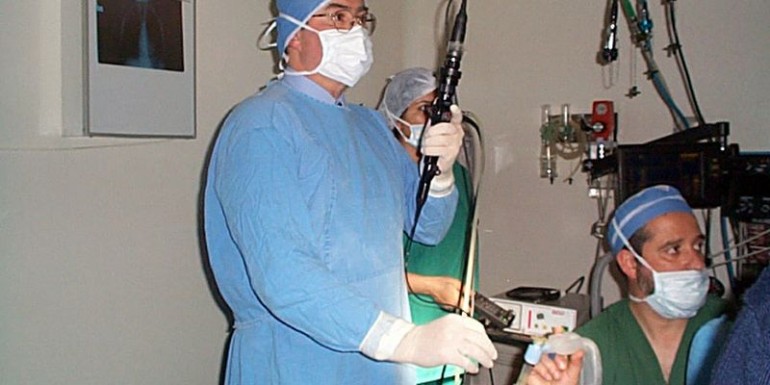
En mayo de 2013 el Servicio de Anestesiología recibe un equipo de fibrobroncoscopia nuevo (Storz Videoendoscopio flexible 5.5×65 11301BNXK, monitor CMOS 8402ZX, carro de soporte Airway TROLL-E), que por sus características permite iniciar un proceso de formación e implementación de la IFO en el área de salud de Guadalajara (España). En ese momento, sólo uno de los 22 facultativos del Servicio disponía de la formación y capacitación para llevar a cabo la técnica, otros dos facultativos habían recibido formación práctica, y los restantes solo disponían de conocimientos teóricos en IFO.
Estrategia de formación y capacitación de facultativos especialistas para IFO:
1. Propuesta y creación de un grupo de facultativos con especial dedicación a la vía aérea difícil, y designación como jefe de equipo al facultativo más experto.
2. Proceso escalonado de formación de los facultativos:
a. Asistencia a un curso acreditado externo de vía aérea difícil que incluyera la IFO.
b. Formación interna: sesiones clínicas, talleres de IFO y de mantenimiento del equipo. Prácticas libres con maniquíes y equipo auxiliar.
c. Prácticas autogestionadas y supervisadas con pacientes sin dificultades de vía aérea (mínimo entre 6 y 10 casos).
3. Capacitación por el jefe de equipo:
a. Asignación de casos reales de VAD bajo supervisión.
b. Aceptación por el jefe de equipo y por el facultativo de la asignación de casos reales de vía aérea difícil como responsable principal sin supervisión.
4. Criterios éticos aplicables al proceso de formación de especialistas: no se consideró aceptable cambiar la vía de intubación por razones formativas, ni la intubación con el paciente despierto cuando no estuviera clínicamente indicada.
5. Todos los facultativos en proceso de formación en IFO estaban plenamente capacitados para el manejo de la vía aérea difícil. Por ello se consideró importante permitir la autogestión en el grado de supervisión requerido y no asignar casos reales hasta que el propio profesional no se sintiera plenamente capacitado.
Protocolo de gestión de riesgo de vía aérea difícil (PGRVAD)
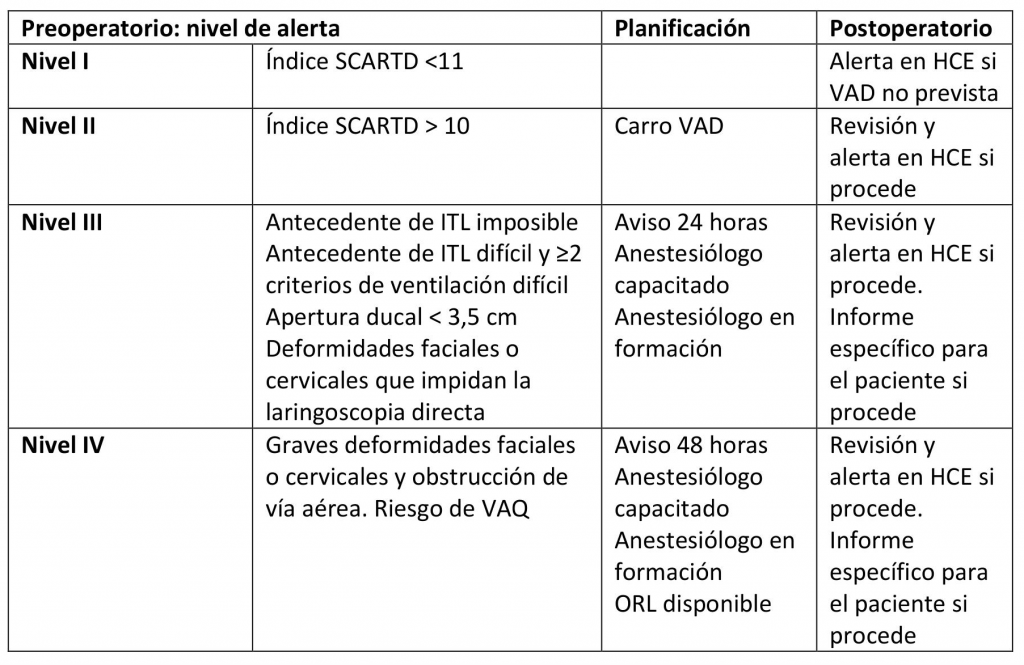
Se reelaboró en los primeros meses el PGRVAD de la Gerencia de Área Integrada de Guadalajara (anexo 1) (PDF) para adaptarlo a los nuevos recursos. El protocolo fue presentado en sesión clínica del Servicio de Anestesiología y en sesión General del Hospital, y se encuentra accesible en la intranet para cualquier usuario de nuestro centro. Dicho protocolo organizativo (tabla I) tiene por objeto la identificación del riesgo de VAD y la planificación de los recursos humanos y materiales necesarios para garantizar una asistencia adecuada a los pacientes y para el logro de los objetivos docentes previstos.
Recogida de datos
Desde el 1 de junio de 2013 se recogieron de forma prospectiva los datos de todos los pacientes en los que se empleó IFO:
1. Preoperatorios: sexo, edad, IMC, intervención programada o urgente, factores de riesgo de vía aérea difícil, nivel de alerta de bloque quirúrgico: I, II, III, IV (según protocolo específico).
2. Técnica de IFBC: planificada (plan A) o urgente tras intubación fallida (plan B); vía oral o nasal; anestesia general o tipo de anestesia local; incidencias; adecuación o no al protocolo de actuación establecido. Incidencias y complicaciones.
3. Postoperatorios: creación o modificación de alerta en historia clínica electrónica conforme a protocolo.
4. Se recogieron los anestesiólogos implicados en cada caso como responsable o ayudante.
Para la evaluación del proceso de implementación se revisó un periodo de dos años (1 de enero de 2014 a 31 de diciembre de 2015). Para este periodo se recogieron también los datos de actividad quirúrgica, cancelaciones o aplazamientos por problemas de vía aérea, consultas a otros especialistas (neumólogos, ORL, cirujanos), y lesiones atribuibles a hipoxemia o a la IFO.
Resultados y control de calidad
Durante el periodo de estudio 26 anestesiólogos formaron parte durante algún periodo de tiempo de la plantilla, que osciló entre los 21 y los 23 facultativos especialistas. De ellos 11 solicitaron formación específica en vía aérea difícil, y realizaron al menos un curso externo acreditado. Dos facultativos ya habían realizado con anterioridad cursos de formación. De estos 13, 9 continuaron su proceso de aprendizaje interno con pacientes sin VAD. Al finalizar el periodo de estudio solo 4 de ellos estaban capacitados y aceptaban la plena responsabilidad en la atención de pacientes con VAD.
Durante estos dos años se intervinieron en nuestro centro 13.869 pacientes programados y 4.007 urgentes. Ningún paciente fue cancelado por problemas de vía aérea. Se consultó a otros especialistas por VAD en 3 ocasiones (traqueostomía con local en alerta nivel IV: todas conforme a protocolo). En dos casos, durante los cuatro primeros meses, fue necesario cambiar la fecha de la intervención para poder garantizar los recursos humanos necesarios. Los casos de IFO por vía aérea difícil se resumen en la tabla II.
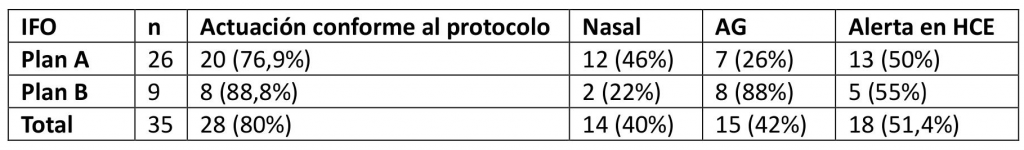
De los 26 casos en los que se utilizó la IFO como plan A, en 20 se había establecido el nivel de alerta III en el informe preoperatorio, y se habían seguido adecuadamente las normas de planificación y asignación de casos. En los otros 6 casos el nivel de alerta establecido era II, pero el anestesiólogo optó por no llevar a cabo ningún intento previo de intubación laringoscópica.
Solo en una ocasión un paciente con nivel de alerta III fue intubado mediante laringoscopia, requiriendo para ello varios intentos, el uso de videolaringoscopio y guía de Esmann. No hubo episodios de hipoxemia, pero si una lesión menor de partes blandas.
Siete de los 9 pacientes en los que se utilizó la IFO como rescate tras intubación fallida tenían un nivel de alerta II, pero en los otros dos casos no existían criterios de riesgo de VAD.
Se registró un solo caso de IFO fallida, en un paciente con nivel de alerta II en el que se decidió utilizarla como primera opción. El fallo se relacionó con la obstrucción del canal de aspiración por secreciones y se decidió llevar a cabo la intubación con videolaringoscopio sin nuevos incidentes.
En este periodo se llevaron a cabo un total de 30 IFO planificadas con finalidad docente, todas conforme a los criterios éticos establecidos.
En tres ocasiones se llevó a cabo la IFO en situaciones de emergencia: imposibilidad de intubación y ventilación manual difícil. Dos de ellas en la Unidad de Cuidos Intensivos y otra en el quirófano de urgencias, todas ellas con resultados satisfactorios.
El fibrobroncoscopio se utilizó también en cuatro ocasiones para inserción y comprobación de bloqueadores pulmonares en cirugía torácica.
Discusión y comentario
La publicación de estudios relacionados con la implementación de técnicas en el ámbito hospitalario, y la evaluación de resultados, es infrecuente. Sin embargo, consideramos que en un tema de tanta relevancia como la gestión de riesgos por VAD, estos estudios pueden resultar de utilidad a las organizaciones para incorporar nuevas tecnologías a la práctica asistencial establecida.
Nuestro PGRVAD se adaptó para asumir plenas competencias en VAD una vez iniciada la implementación de la IFO. Los niveles de alerta establecidos en el informe preoperatorio fueron presentados y discutidos en el Servicio, adoptándose con un alto nivel de consenso. Se utilizó la escala de la Sociedad Catalana de Anestesiología (4) por su practicidad. La escala permite establecer un punto de corte para la alerta por posible VAD en base a criterios de exploración clínica generalmente aceptados (5). Establecimos de forma arbitraria más de 10 puntos para el nivel de alerta II.
El nivel II no conlleva cambios en la planificación quirúrgica y es asumido por todos los profesionales. El nivel de alerta III concreta los casos en los que la IFO se considera como primera elección o como única alternativa posible siguiendo los criterios más habituales (1). Los algoritmos más difundidos no especifican este aspecto, dejando la indicación de IFO como primera opción a criterio del facultativo (6). En nuestro caso era importante concretarlo para disminuir la variabilidad en el informe preoperatorio, dado que el nivel III implica una alerta específica para la planificación quirúrgica. Esta alerta aparece claramente visible en el informe preoperatorio y obliga al Servicio de Admisión y al Servicio Quirúrgico correspondiente a avisar, con al menos 24 horas de anticipación, a la secretaría de anestesia para la programación del paciente. Esto permite a la Jefatura de Servicio la planificación de los recursos humanos: anestesiólogo responsable y anestesiólogo ayudante, algo esencial para la formación e implementación de la técnica.
Heidegger T y cols (3) incluyen en su protocolo asistencial la indicación de IFO oral o nasal como única alternativa a la laringoscopia tradicional con pala de Macintosh para VAD (6). Esto amplia notablemente el número de casos de IFO (13.5% de todas las intubaciones), lo que sin duda facilita la formación del personal, pero no está bien documentado que aporte un mayor beneficio al paciente. Su algoritmo de actuación difiere notablemente de los propuestos por algunas de las principales sociedades científicas (7, 8). En nuestro centro, la práctica clínica se ajusta más a estos últimos, utilizando con eficacia los recursos habituales para rescate en intubación difícil, especialmente: guías, videoaringoscopios y mascarilla laringea. Ello explica la escasa necesidad de recurrir a la IFO (1.5/1000 intervenciones, 0.6 IFO/anestesista/año), al igual que ocurre en series muy extensas aportadas por otros autores (5, 9). En todo caso, en nuestro hospital, un protocolo como el propuesto por Heidegger T, hubiera sido imposible de desarrollar por falta de personal entrenado y de recursos materiales. Sin embargo, nuestros anestesiólogos pueden establecer la indicación de IFO para criterios clínicos de riesgo no explicitados como alerta III, tal como ocurrió en 6 de los 26 casos en los que se optó por dicha técnica como primera opción (plan A).
Llama la atención en nuestro estudio que algunos anestesiólogos interesados, que realizaron cursos externos, no continuaron posteriormente con su proceso de aprendizaje. Esto probablemente se relaciona con la presión asistencial que soporta el equipo. La dedicación de tiempo “extra” a prácticas para formación puede generar inconvenientes con cirujanos, enfermeros o auxiliares, que deben implicarse también en tareas de apoyo y mantenimiento. Mantener la motivación es por tanto difícil, pero también esencial. En nuestro centro consideramos inviable para la organización un programa de rotaciones por quirófanos específicos tal y como proponen otros autores (10, 11). Por otra parte tampoco consideramos esta opción como la más adecuada. Los anestesiólogos utilizaron libremente las ayudas disponibles de maniquíes y equipos, y practicaron con pacientes sin dificultades de vía aérea solicitando apoyo cuando lo consideraron oportuno. Este planteamiento, más liberal y autogestionado, se ve favorecido por el pequeño tamaño de nuestras instalaciones, lo que hace posible una cooperación rápida y eficaz entre los profesionales con diferentes niveles de formación en IFO. También permitió la simulación de situaciones de alta complejidad para entrenar el factor humano con la metodología CRM (Crisis Resource Managment ) (12).
Consideramos aconsejable un número de entre 6 y 10 IFO antes de la habilitación y la propuesta para la asignación de casos reales bajo supervisión. Este número, aunque arbitrario, es generalmente aceptado desde el trabajo de Johnson C y cols de 1989 (13). Sin embargo, el proceso de formación solo se ha documentado para médicos residentes (11, 13), y es posible que existan diferencias para la formación de facultativos con experiencia y habilidades en el manejo de la VAD con otros muchos recursos técnicos.
También hemos comprobado dificultades en los profesionales para asumir su plena competencia tras completar las fases anteriores. Los anestesiólogos que finalmente lo hicieron en este periodo precisaron un mínimo de tres casos reales bajo supervisión. Resulta evidente que la baja incidencia de casos es lo que dificulta la autoafirmación de competencias.
Para nuestro grupo, lo importante no fue establecer el número de casos necesario para la habilitación, sino las sensaciones percibidas por el propio profesional sobre su capacidad para el desempeño de la tarea. El factor humano en entornos de alta complejidad es esencial a la hora de abordar nuevas competencias, y por tanto, no es aconsejable (y difícilmente viable a nuestro juicio) la imposición ejecutiva. Para la organización es muy importante el incremento del número de profesionales con competencias plenas en VAD con objeto de facilitar la programación quirúrgica de estos pacientes. Durante los primeros meses, fue necesario cambiar la fecha de programación quirúrgica de tres pacientes que requerían IFO. Esta circunstancia no volvió a darse a partir de contar con tres anestesiólogos capacitados. Para atender la demanda en cirugía programada, consideramos adecuado el número actual de anestesiólogos capacitados (5), pero necesitaríamos al menos 10 para asegurar que alguno formara parte a diario del equipo de atención continuada, mejorando así la seguridad en el bloque quirúrgico y en otras áreas: urgencias y cuidados intensivos. Actualmente nuestro servicio no puede cubrir todos los días, y es el neumólogo localizado el que acude en caso necesario, y así consta en nuestro protocolo (aunque en el periodo analizado no fuera necesario su concurso). Consideramos que la IFO es una competencia que debe incorporarse a los equipos de presencia física y este es una de nuestros objetivos de mejora.
En todos los casos en los que se estableció el nivel de alerta tres el protocolo se siguió de forma correcta en cuanto a la planificación y asignación de los pacientes, y salvo en un caso, se llevó a cabo la IFBC sin complicaciones.
Sin embargo, hubo bastante variabilidad en el desarrollo de la técnica. En un 26% de los casos se prefirió la anestesia general con o sin relajación neuromuscular. En los que se hicieron con anestesia local se utilizaron diferentes técnicas: punción cricotiroidea (4 casos), nebulización con mascarilla facial (6 casos), nebulización con cánulas especiales e instilación a través de FBC (9 casos). También varió la posición del operador: face to face (20 casos) o posterior (15 casos). Esta variabilidad cabe explicarla por el hecho mismo de ser una actividad en proceso de implementación, y en que no se ha impuesto ningún protocolo concreto de actuación, permitiendo a cada profesional desarrollar su método en base a su formación y experiencia. Dado que no hay evidencia científica sobre las ventajas de una u otra técnica (1), consideramos que nuestro planteamiento favorece el aprendizaje y amplía las competencias del equipo.
La IFO adquiere cada vez más protagonismo también en la intubación imposible no prevista, y ya se contempla en los algoritmos promovidos por las sociedades científicas, especialmente a través de mascarilla laríngea (7, 8). En un hospital de pequeño tamaño como el nuestro, que permite una comunicación inmediata entre profesionales, y una rápida accesibilidad al equipo, la IFO pudo resolver numerosos casos de intubación imposible no prevista (incluso fuera de quirófano), reduciendo los intentos fallidos y evitando la cancelación de las intervenciones. Esta alternativa parece ir ganando presencia en nuestro hospital a medida que se incrementa el número de anestesiólogos competentes en IFO y se ha promovido en sesiones clínicas con el objetivo de reducir los intentos fallidos por laringoscopia. En ninguno de estos rescates se utilizó mascarilla laríngea. En dos casos se hizo la IFO a través de mascarilla facial fenestrada y cánula de VAMA®. En los otros 5 se llevó a cabo en apnea tras hiperventilación, cuatro casos con cánula de VAMA® y uno a través de Airtraq®.
Recogimos un total de seis incidentes. Dos de ellos por errores en la limpieza y preparación del equipo que provocaron averías y la inutilización temporal del mismo. Los otros cuatro fueron fallos en la ejecución de la técnica que se resolvieron con la participación de otro anestesiólogo más experto: mala preparación del paciente, fallo del sistema de aspiración, agotamiento de la batería, mala visibilidad por empañado de la óptica.
En el PGRVAD se decidió no trasladar directamente la alerta de VAD, del formulario de evaluación preoperatoria a la barra de alertas de la pantalla de identificación de pacientes en la historia clínica electrónica (Mambrino XXI v5. 4.0 n). Se optó por hacerlo después de comprobar el grado de alerta real en quirófano para evitar los falsos positivos. La laringoscopia postintubación es poco fiable para establecer la calidad de la visión sin intubación (14), pero sí creemos que puede descartar laringoscopias difíciles establecidas previamente con criterios clínicos. En la correcta cumplimentación de la alerta tras la intubación es en lo que hemos obtenidos peores resultados: solo se realizó correctamente y se entregó el informe pertinente en la mitad de los casos, incluso en los pacientes con intubación imposible no prevista. Este punto, sin embargo, es de gran importancia para la gestión de riesgo en el área de salud, y mejorar este resultado se ha presentado como objetivo específico para plan de calidad de 2016.
Concluimos que nuestra estrategia liberal de formación, evaluación y autoevaluación de competencias en IFO, apoyada en un protocolo organizacional completo para la identificación y gestión de riesgos por VAD, ha tenido unos resultados asistenciales satisfactorios y ha tenido una acogida favorable por parte de los profesionales. Sin embargo, la escasa incidencia de casos reales de VAD que requieran IFO, la presión asistencial y el factor humano en entornos de alta complejidad, dificultan la realización de prácticas supervisadas y el mantenimiento de la competencia de quienes asumen plenas responsabilidad en IFO.
Protocolo de gestión de riesgo de vía aérea difícil (PGRVAD) de la Gerencia de Área Integrada de Guadalajara (PDF)
Bibliografía
1) Collins SR, Blank RS. Fiberoptic intubation: an overview and update. Respiratory Care 2014; 59: 865-880 (PubMed) (HTML) (PDF)
2) Yepes Temiño MJ, Panadero Sánchez A, Callejas González R, Carrascosa Moreno F, Pérz Valdivieso JR. An awake fiberoptic intubation protocol: descriptive retrospective assessment of safety and efficacy. Rev Esp Anestesiol Reanim 2011; 58: 80-84 (PubMed)
3) Heidegger T, Gerig HJ, Ulrich B, Schnider TW. Structure and process quality illustrated by fiberoptic intubation: analysis of 1612 cases. Anesthesia 2003; 58: 734-739 (PubMed) (HTML) (ePDF)
4) Kheterpal S, Healy D, Aziz MF, Shanks AM, Freundlich RE, Linton F, et al. Incidence, predictors, and outcome of difficult mask ventilation combined with difficult laryngoscopy. A report from the multicenter perioperative outcome group. Anesthesiology 2013; 119: 1360-1369 (PubMed) (HTML)
5) Heidegger T, Gerig HJ, Henderson JJ. Strategies and algorithms for management of the difficult airway. Best Practice & Research Clinical Anesthesiology 2005; 19: 661-674 (PubMed)
6) Apfelbaum JL, Hagberg CA, Caplan RA, Blitt CD, Connis RT, Nickinovich DG et al. Practice guidelines for management of the difficult airway: an updated report by the American Society of Anesthesiologists Task Force on Management of the difficult airway. Anesthesiology 2013; 118: 251-70 (PubMed) (HTML)
7) Freck CM, Mitchell VS, McNarry AF, Mendonca C, Bhagrath R, Patel A et al. Difficult Airway Society 2015 guidelines for the management of unanticipated difficult intubation in adults. Br J Anaesth 2015; 115: 827-848 (PubMed) (HTML) (PDF)
8) Aziz MF, Brambrink AM, Healy DW, Willet AV, Shanks A, Tremper T et al. Succes of intubation rescue techniques after failed direct laryngoscopy in adults: a retrospective comparative analysis from the Multicenter Perioperative Outcomes Group. Anesthesiology 2016 (PubMed) (HTML)
9) Mariscal Flores ML, Jiménez García MJ, García Molina C, Martínez Hurtado E. Proyecto de aprendizaje del fibrobroncoscopio del Servicio de Anestesiología del Hospital Universitario de Getafe. AnestesiaR 2016; 3 agosto (HTML)
10) Goldman K, Ferson DZ. Education and training in airway management. Best Practice & Research Clinical Anesthesiology 2005; 19: 717-732 (PubMed)
11) Rall M, Dieckmann P. Safety culture and crisis resource management in airway management: general principles to enhance patient safety in critical airway situations (PubMed)
12) Johnson C, Roberts JT. Clinical Competence in the performance of fiberoptic laryngoscopy and endotracheal intubation: a study of resident instruction. Journal of Clinical Anesthesia 1989; I: 344-349 (PubMed)
13) Foglia J, Archer D, Pytka S, Bughirzada L, Duttchen K. Does laryngoscopic view after intubation predict laryngoscopic view before intubation? Jornal of Clinical Anesthesia 2016; 33: 469-475) (PubMed)
14) Henderson JJ, Popat MT, Latto IP, Pearce AC. Difficult Airway Society guidelines for management of the unanticipated difficult intubation. Anesthesia 2004; 59: 675-694 (PubMed) (HTML) (ePDF)
Cómo citar: Rodríguez Fraile, J. R., García Quiroga, R., Montoro García, J., de la Fuente Tornero, E., Martínez Meco, L. (2020). Implementación de la intubación fibróptica en un hospital general y análisis de resultados. Revista Electrónica AnestesiaR, 10(10), 6. https://doi.org/10.30445/rear.v10i10.761