Charco Roca, L. M. (1), Ortiz Sánchez, VE. (1), Ruiz tornero, A. M. (2). Hernández Martínez , J. J. (3), Bonmatí García L. (4), Rubio Postigo, G. (4)
(1) Facultativos especialistas de Área, Servicio de Anestesiología y Reanimación
(2) Facultativo especialista de Área, Servicio de Cardiología
(3) Facultativo especialista de Área, Servicio de Neurología
(4) Personal de Enfermería del Área de Reanimación
Hospital Virgen Del Castillo, Yecla (Murcia)
RESUMEN
Un varón de 32 años presentó, tras sufrir fractura diafisaria de fémur por caída accidental desde una altura de tres metros, un deterioro neurológico progresivo con tomografía computerizada cerebral normal. Fue ingresado en la Unidad de Reanimación con una elevada sospecha de síndrome de embolismo graso. El paciente presentaba sintomatología neurológica leve y lesiones cutáneas compatibles con el cuadro clínico. La RMN mostró imágenes cerebrales que apoyaban el diagnóstico del cuadro clínico. El diagnóstico precoz permite identificar al paciente como de alto riesgo por la potencial posibilidad de complicaciones sistémicas graves.
INTRODUCCIÓN
El síndrome de embolia grasa (SEG) es una complicación grave que puede presentarse en pacientes con fracturas esqueléticas, fundamentalmente en aquellos con fracturas cerradas de huesos largos. Dada su asociación con los politraumatismos, se presenta con mayor frecuencia en la segunda y tercera década de la vida (1).
Aunque cerca del 90% de estos pacientes presentan fenómenos subclínicos de embolismo graso, la incidencia del SEG postraumático de relevancia clínica está descrita en un porcentaje muy inferior de casos, que oscila según las series publicadas, entre el 0,2 y el 35%, y parece aumentar proporcionalmente al número de fracturas involucradas (2).
El Embolismo Graso es la obstrucción en el flujo de un vaso sanguíneo por material lipídico liberado a partir de los huesos fracturados, mientras que el SEG es un conjunto de síntomas que reflejan el embolismo graso en el sistema respiratorio e incluye manifestaciones neurológicas, insuficiencia respiratoria y petequias, junto con alteraciones analíticas.
Presentamos un caso de SEG sufrido por un paciente joven tras una fractura diafisaria de fémur de inicio fundamentalmente neurológico y con buena evolución clínica.
CASO CLINICO
Presentamos el caso de un varón de 32 años, sin antecedentes patológicos de interés, que fue traído por el servicio de emergencias a urgencias hospitalarias tras sufrir una caída accidental desde una palmera (3 metros de altura aproximadamente). Fue diagnosticado mediante exploración física y pruebas radiológicas de fractura transversa del tercio medio del fémur izquierdo y se aplicó como tratamiento inicial una tracción de partes blandas de 5 kg por parte del traumatólogo de guardia, quedando ingresado en planta de hospitalización a la espera de tratamiento quirúrgico definitivo. El paciente no había sufrido traumatismo craneoencefálico, abdominal ni torácico.
Al despertarse en la planta de hospitalización, a las 10 horas del traumatismo, el paciente presentó obnubilación y desorientación. El traumatólogo decidió avisar a neurología que tras realizar TAC craneal y punción lumbar con resultados normales comentó el caso con el Servicio de Anestesiología y con la sospecha de síndrome de embolia fue ingresado en Reanimación para completar estudio y seguimiento evolutivo.
A su ingreso en Reanimación en la exploración neurológica se presentaba confuso con tendencia al sueño que requerían maniobras dolorosas para la apertura ocular. Emitía lenguaje espontáneamente pero de poco contenido e incoherente aunque era capaz de responder a ordenes sencillas, no era capaz de nominar, repetir ni ejecutar dos secuencias. En la exploración de pares craneales mostraba pupilas isocóricas y normorreactivas con reflejos de amenaza conservados. Motilidad ocular externa sin limitaciones, pero imposibilidad de continuar el dedo con bamboleo en posición central. Resto de pares craneales normales. Era capaz de movilizar de manera simétrica tres extremidades, el miembro inferior izquierdo no era valorable por fractura de fémur inmovilizada. Presentaba reflejos osteotendinosos algo disminuidos (ROT: ++/++++) con reflejo cutáneo plantar (RCP) extensor izquierdo. La sensibilidad estaba conservada y la coordinación no era valorable por falta de colaboración del paciente.
La exploración física y constantes vitales al ingreso en Reanimación no mostraban alteraciones salvo taquicardia sinusal a 130 lpm, fiebre de 38.2ºC y SpO2 de 92% con FiO2 al 60%. La radiografía de tórax no mostraba signos congestivos ni otros hallazgos patológicos y en la gasometría arterial se observaba PaO2 de 89 mmHg. Fueron solicitadas otras complementarias realizándose una RM cerebral que mostraba lesión en esplenio de cuerpo calloso y en centros semiovales que restringían la difusión de probable origen edematoso-inflamatorio. No se observaban lesiones hemorrágicas o desmielinizantes. Previo al ingreso en Reanimación se había realizado un TAC craneal que ya mostraba ausencia de sangrado intra ni extraaxial, no presentaba desplazamientos de la línea media o alteraciones en la densidad del tejido cerebral.
Se solicitó una interconsulta a cardiología que realizó un ecocardiograma descartando foramen oval, y observó ligera dilatación de cavidades derechas, con el resto de estructuras normales y fracción de eyección conservada. Se solicitó también la realización de un fondo de ojo a oftalmología que fue informado sin hallazgos compatibles con embolia grasa, únicamente visualizando una papila derecha pálida.
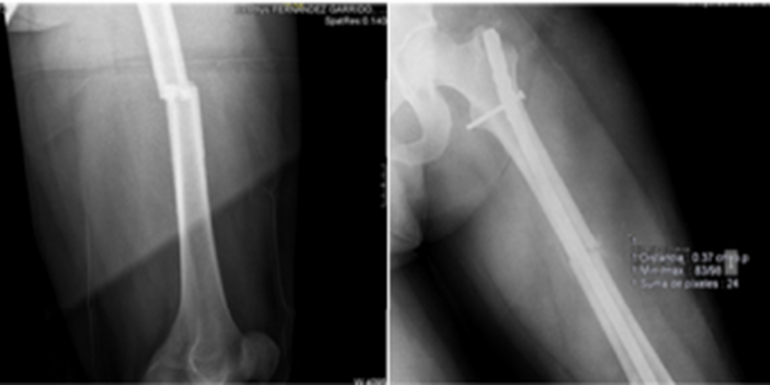
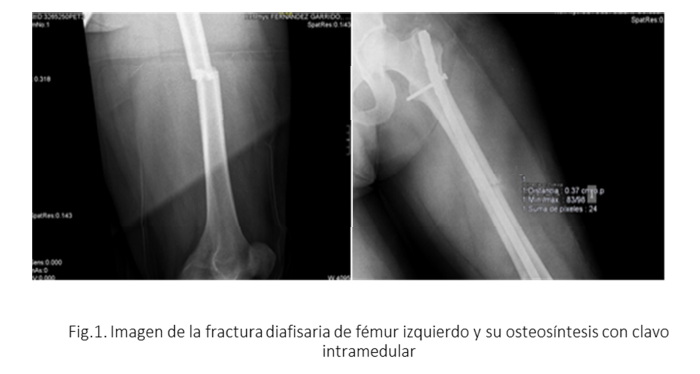
A las 48 horas del debut de la clínica neurológica fue intervenido quirúrgicamente para osteosíntesis de la fractura de fémur mediante clavo intramedular (Fig.1) bajo anestesia raquídea, cursando la intervención y el postoperatorio sin incidencias.
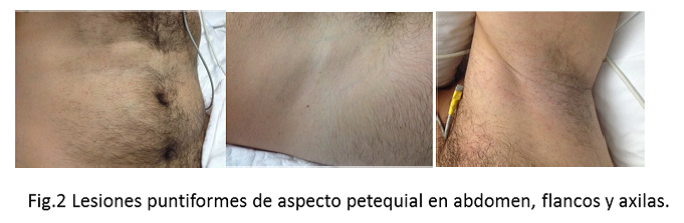
A los 3 días de inicio de la clínica neurológica aparecieron en la piel del paciente lesiones puntiformes localizadas en flancos, parte superior del tórax y axilas (Fig. 2).
Durante su estancia en Reanimación mantenía Glasgow oscilante de 14-12 desde el ingreso, con fluctuación diaria con mejoría matutina y empeoramiento vespertino, en los que comprendía parcialmente órdenes, preguntas y estaba somnoliento. Presentó rigidez meníngea asociada a fotofobia detectada tras 2 días de estancia Reanimación y que persistía al alta. Para la intervención quirúrgica se realizaron dos punciones raquídeas en diferentes niveles, obteniendo en ambas líquido hemático que no aclaraba, se sospechó cefalea post punción dural como origen de esta clínica. A los 7 días fue dado de alta a planta de hospitalización con Glasgow 14 (O: 4, V: 4, M: 6) y persistiendo cierta bradipsiquia pero con un lenguaje coherente, orientado y colaborador. No se apreciaban otras focalidades neurológicas salvo un Babinski izquierdo.
En planta fue seguido por el servicio de neurología que instauró tratamiento con AAS 300mg vía oral cada 24h, clonazepam 0.5 mg por las noches y HBPM 40 mg subcutánea cada 24h hasta inicio de deambulación. Fue dado de alta a domicilio sin complicaciones sobreañadidas del postoperatorio y asintomático desde el punto de vista neurológico. A los dos meses en una revisión en consulta externa por neurología se presentaba asintomático.
DISCUSIÓN
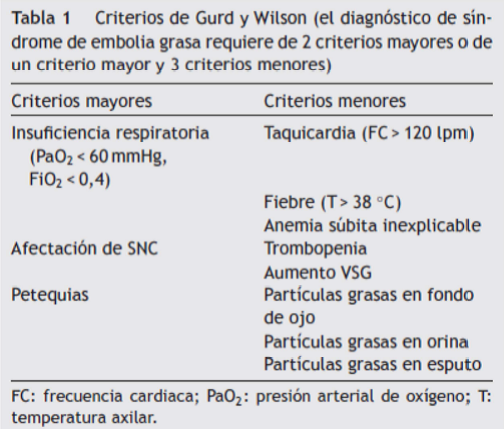
El SEG aparece tras un intervalo libre de síntomas de 24 a 72 h y se manifiesta típicamente por la tríada clínica de insuficiencia respiratoria, manifestaciones neurológicas y petequias (3), junto con alteraciones analíticas tales como anemia y trombopenia. El diagnóstico resulta un reto en la práctica médica diaria, puesto que no existen exploraciones que permitan un diagnóstico de certeza y este continúa siendo eminentemente clínico. En este sentido se han publicado en las últimas décadas diversos criterios diagnósticos, siendo los de Gurd y Wilson los más aceptados (Tabla 1) (4).
La clínica respiratoria es la más frecuente (presente casi en un 100% de los casos) y generalmente es la más precoz. La morbimortalidad del síndrome viene determinada fundamentalmente por la gravedad del cuadro respiratorio y hasta el 50% de los pacientes pueden precisar ventilación mecánica. Las manifestaciones neurológicas aparecen en el 80% de los casos y suelen ser síntomas transitorios, aunque pueden dejar secuelas en algún caso. El exantema petequial está presente en el 20-50% de los casos y es el signo clínico más específico, aunque también el más tardío. Otras manifestaciones clínicas descritas son el fracaso renal agudo, la depresión miocárdica, la ictericia y la fiebre (Tabla II).

El deterioro neurológico progresivo en un paciente con fractura de huesos largos y ausencia de traumatismo craneal, debe hacernos sospechar una embolización grasa paradójica, la cual está estrechamente relacionada con la existencia de foramen oval permeable. Su presencia aumenta el riesgo de posteriores embolizaciones y obliga a extremar las precauciones en la manipulación quirúrgica definitiva. Se ha descrito una mejoría del cuadro clínico tras el cierre preoperatorio del foramen oval (5). En el caso clínico presentado esto fue descartado cuando se inició la sospecha de SEG mediante un ecocardiograma transtorácico.
El diagnóstico del SEG es fundamentalmente clínico, y debe basarse en la observación de los signos clínicos clásicos en un paciente de riesgo, en ausencia de explicaciones alternativas. La RM cerebral resulta de gran utilidad en el manejo de los pacientes con SEG, aunque su realización puede verse dificultada por la presencia de materiales protésicos.
En cuanto a datos de laboratorio pueden hallarse datos de hipoxemia en casi todos los pacientes con SEG, con frecuencia los valores de PaO2 son < de 60 mm/Hg. Sin embargo la ausencia de hipoxemia no excluye la presencia de SEG. La hipoxemia generalmente suele acompañarse de alcalosis. La presencia de anemia es uno de los hallazgos más tempranos esperados después de un trauma severo. En los casos de SEG sin datos aparentes de hemorragia el hematocrito puede llegar hasta el 30% en aproximadamente el 75% de los pacientes dentro del 1° y 2° día posterior al trauma. El hallazgo de plaquetopenia es una alteración clasificada también como típica del SEG, aunque muchos estudios recientes indican que la plaquetopenia ocurre solamente en un 30% de los pacientes (3), coagulación intravascular diseminada (CID), un discreto incremento en la actividad del complemento o un patrón de elevación de los ácidos grasos libres en sangre y orina que nunca se correlacionan ni con el diagnóstico ni con la gravedad del cuadro.
Se han descrito factores de riesgo generales y específicos para el desarrollo de SEG. Los factores de riesgo generales son: estados de hipovolemia postraumática y daño pulmonar agudo, inestabilidad perioperatoria con recuperación hemodinámica posoperatoria inadecuada y disminución de la reserva cardiorrespiratoria. Los factores de riesgo específicos relacionados con procedimientos ortopédicos son el reemplazo articular después de fracturas del fémur, reemplazo de cadera con cemento o sin él y de prótesis de rodilla de alto volumen, procedimientos bilaterales, el fresado intramedular y el limado óseo después de fracturas femorales o de metástasis.
No existe tratamiento específico, motivo por el que es fundamental su prevención, que comienza con la inmovilización temprana y la fijación precoz de las fracturas y puede incluir medidas más controvertidas como el uso profiláctico de corticoides. La heparina, aspirina y los dextranos reducen la adhesividad plaquetaria y la formación de microagregados (2), aunque el uso de dextranos ha sido rechazado por sus efectos negativos en la coagulación y la función renal. Una vez establecido el cuadro clínico, una pronta sospecha diagnóstica y un tratamiento de soporte adecuado pueden reducir de modo sustancial las complicaciones y la mortalidad, que se estima es cercana al 5-15% (2).
El cuadro clínico de nuestro paciente sugiere una embolia grasa secundaria a la fractura diafisaria de fémur y cumple todos los criterios necesarios de Gurd y Wilson (dos criterios mayores que son la afectación neurológica y la presencia de petequias y dos criterios menores que son taquicardia y fiebre).
CONCLUSIONES
El SEG afecta sobre todo a pacientes con fracturas cerradas de huesos largos. Es de diagnóstico difícil y potencialmente muy grave. Presenta manifestaciones clínicas respiratorias, neurológicas y de coagulopatía, propias de la clínica clásica del síndrome y una mortalidad considerable, cercana al 10%.
El SEG presenta un período asintomático latente de 12-72 horas, y un período sintomático resultado de los múltiples microémbolos grasos que llegan a los órganos diana. El diagnóstico es por tanto clínico, su forma leve pasará desapercibida o será mal diagnosticada, mientras que la mayoría de los casos graves no se diagnostican hasta la autopsia.
El deterioro neurológico tras un traumatismo puede deberse a varios motivos. Entre los más frecuentes se encuentran la hemorragia intracraneal, la hipoxemia y el shock. Tras descartar estas causas, el deterioro neurológico tras un traumatismo con fracturas, debe hacernos sospechar un embolismo graso. Las manifestaciones neurológicas del síndrome de embolia grasa tienen, por lo general, buen pronóstico. Los casos graves sugieren una embolización cerebral (paradójica) masiva y se asocian a la existencia de un foramen oval permeable.
Los signos y síntomas del SEG son inespecíficos, a excepción de las petequias no existen signos patognomónicos de este síndrome. Las pruebas de laboratorio no son específicas. Por tanto para el diagnóstico es necesaria la alta sospecha clínica para poder instaurar el tratamiento adecuado en cada momento. La medida profiláctica más efectiva está en reducir las fracturas lo antes posible después de la lesión. Posiblemente el aspecto más importante sea corregir la hipoxemia.
BIBLIOGRAFíA
- White T, Petrisor BA, Bhandari M. Prevention of fat embolism syndrome. Injury. 2006; 37 Suppl 4:S59-67.(PubMed) (PDF)
- Mellor A, Soni N. Fat embolism. Anaesthesia. 2001; 56: 145-54. (PubMed) (PDF)
- Georgopoulos D, Bouros D. Fat embolism syndrome: clinical examination is still the preferable diagnostic method. Chest. 2003; 123: 982-3. (PubMed) (PDF)
- Gurd AR, Wilson RI. The fat embolism syndrome. J Bone Joint Surg Br. 1974; 56B:408-16. (PubMed)
- I. Ruiz-Gimeno, M.ª A. Ferre, M.ª T. Napal, F. Pelegrín. Rev. Esp. Anestesiol. Reanim. 2006; 53: 187-190) (PubMed)



Caso interesante para recordar y repasar el embolismo graso, aunque me llama la atención que un paciente joven con fractura diafisaria de femur no se intervenga de urgencias para tratamiento quirúrgico precoz. Esta es la política habitual en el centro donde trabajo, es considerada una urgencia precisamente por el riesgo de embolismo graso.
La intervención quirúrgica urgente para fijación de las fracturas de huesos largos es lo recomendable e imperativo para evitar esta complicación.
En el caso expuesto no se realizo de esta forma por la conjunción de varios factores; que el accidente se produjo un día festivo, que fue recibido en un hospital comarcal en el q solo hay un traumatologo de guardia ( no es excusa pero analizando los factores precipitantes esto tuvo peso) y posiblemente el desconocimiento general de la verdadera incidencia de este sindrome.
Gracias por su interés en el caso.
A mi hijo lo durmieron por enbolos de grasa que se le fue al cerebro por quebradura de fémur tendra problema para despertar