Vicho Pereira R.
Intensivista y profesor de ecocardiografía del paciente crítico (ECOCRITIC)
Introducción
En esta revisión se recomiendan una serie de prácticas clínicas para el manejo del paciente con shock séptico basado sobre todo en las nuevas guías del manejo de la sepsis 2016 (1) y en la conferencia del consenso del shock (2).
El grado de recomendación hoy en día del manejo del paciente crítico guiado por ecografía es muy alto y evidentemente, eso incluye a un paciente tan complejo hemodinámicamente como el séptico. Se sabe que la sepsis puede combinar diferentes tipos de shock (vasopléjico, hipovolémico, disfunción miocárdica izquierda y/o derecha), y si además el paciente presenta una cardiopatía de base (miocardiopatía, estenosis aortica, cardiopatía isquémica) determina que sea imprescindible el manejo con ecografía. Además, la disfunción diastólica en el séptico, que ya ha sido muy estudiada, supone un aumento de la mortalidad muy importante y sólo se podría diagnosticar y manejar correctamente guiada con un ecocardiograma doppler.
Con todo ello, se pretende hacer una reflexión sobre el uso de las técnicas de monitorización hemodinámica continua, que si bien se recomienda su uso, éste al menos debe ir asociado a la ecografía ya que:
– tienen artefactos,
– pierden calibración (ej: PICCO en pacientes con temperatura < 35ºC),
– sus valores a veces oscilan de forma grosera (calibración inicial de la termodilución del PiCCO),
– hay algunas patologías prevalentes que supra o infra estiman en gran medida los valores normales (ej: gasto cardiaco por Swan-Ganz o PICCO en pacientes con insuficiencia tricúspide moderada o severa) (3).
Todos estos argumentos han sido los que han llevado a la monitorización hemodinámica por ecocardiografía doppler a la categoría de la mejor práctica clínica en la conferencia de consenso del manejo del shock (2) y de ahí su uso como herramienta clínica guía en el paciente en shock séptico.
Guía de manejo hemodinámico del paciente séptico
1) Una vez diagnosticado el paciente en shock séptico debe ser manejado como una emergencia.
2) Fluidoterapia.
Precisaría inicialmente 30 ml/kg de fluidoterapia, sobre todo a expensas de cristaloides (incluso por encima de gelatinas) en 3h. Los hidroximetilalmidones parecen estar proscritos por su nefrotoxicidad y aumento de mortalidad.
En esta fase el ecocardiograma doppler es opcional pero pasadas 3h habría que realizar el primer estudio hemodinámico que tendría que incluir valoración dinámica de precarga para así guiar el tratamiento en combinación con otros objetivos tisulares como: la saturación venosa central de oxígeno (SVcO2) gap de CO2, lactato, presión arterial media (PAM) con un target de 65 mmHg, SaO2, frecuencia respiratoria y diuresis horaria.
Queda claro que no hay que tomar ninguna decisión de volemia sobre cualquier valor aislado de pruebas estáticas de precarga por cualquier sistema de monitorización hemodinámica (presión venosa central (PVC), presión capilar pulmonar (PCP), E/e…). La realización de pruebas dinámicas de precarga para guiar la repleción evitará el anasarca que aumenta la morbimortalidad de estos pacientes. Por este motivo, y por estudios posteriores, el protocolo de manejo inicial hemodinámico del shock séptico del doctor Rivers esta denostado.
Monitorización con ECO dopppler
Las mediciones por ecocardiografía doppler se harán en un plano apical 5 cámaras:
-Relación E/e. E: Velocidad pico del llenado pasivo, e: media de velocidad pico del doppler tisular pulsado mitral y septobasal. Sus valores en cuanto a interpretación son similares a los de la presión capilar pulmonar en el catéter de la arteria pulmonar. Valor aislado onda e de doppler tisular pulsado (DTI) significa función diastólica independiente de precarga (<9 disfunción diastólica, alta mortalidad).
-IVT de TSVI (integral velocidad tiempo del tracto de salida del ventrículo izquierdo justo bajo la aórtica). Un valor de 20 cm corresponde aproximadamente a 75 cc de volumen sistólico. El resultado se multiplica por la frecuencia cardiaca para obtener el gasto cardiaco (GC)
-Velocidad máxima del flujo aórtico. > 4 m/s sugiere estenosis aortica moderada-severa.
-Valoración global semicuantitativa de la contractilidad del ventrículo izquierdo. Se estima la fracción de eyección como buena o supranormal, levemente deprimida, moderadamente deprimida o severamente deprimida.
-Cálculo de las resistencias vasculares sistémica (RVS). (PAM-PVC) x 80 / GC
-TAPSE (excursión sistólica del anillo tricúspide). < 15 mm disfunción sistólica del ventrículo derecho.
-Pruebas dinámicas de precarga: Si son respondedores y hay datos analíticos o clínicos de hipoperfusión se optará por la repleción.
En Ventilación Mecánica (con volumen tidal 8 ml/kg):
a) 100 cc de coloide en 1 min. Respondedor si aumenta la IVT de TSVI> 10% (4).
b) Variación > 36% en el calibre de la vena cava superior (ecocardiografía transesofagica) define al respondedor (5).
c) Variación > 18 % en el calibre de la vena cava inferior ecocardiografía transtorácica en plano subcostal define al respondedor (6).
d) Levantamiento pasivo de piernas a 45º durante 1 min, respondedor si aumenta > 10% la velocidad del flujo aórtico. Limitación: pacientes con hipertensión abdominal (7).
En Ventilación espontanea:
a) Levantamiento pasivo de piernas a 45º durante 1 min, respondedor si aumenta > 10% de sistólico por ecocardiografía. Limitación: pacientes con hipertensión abdominal (8).
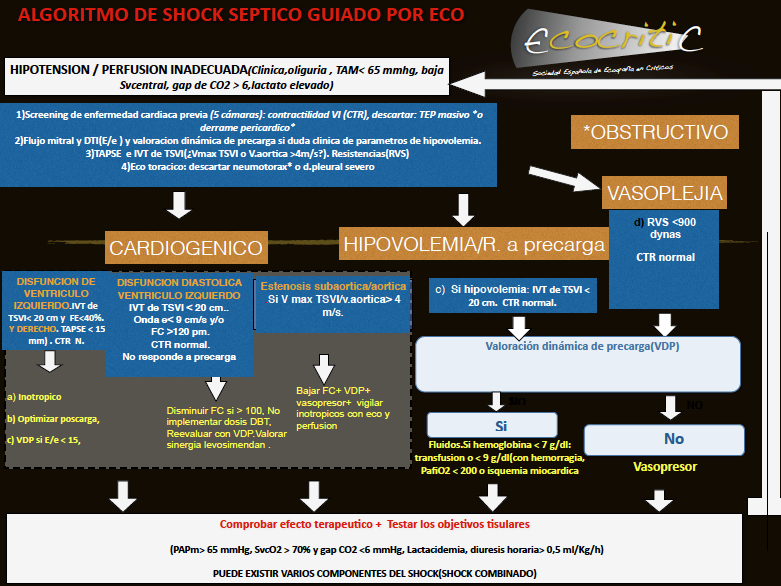
Con este análisis se abordan los diferentes componentes del shock, se podrá descartar alguna cardiopatía basal que influya en el manejo hemodinámico (sobre todo la estenosis aortica o subaórtica severa) y guiar drogas vasoactivas y replección siempre con una intensidad directamente relacionada con los parámetros de perfusión tisular antes analizados. Se adjunta un algoritmo del manejo del shock séptico guiado por ecocardiografía (figura 1). Se aconseja, sobre todo si se trata de una sepsis de origen respiratorio, hacer también una valoración pleuropulmonar para filiar extensión del foco, descartar neumotórax y derrame pleural. Se debería realizar un ecocardiograma doppler diario tras el primero y se puede asociar un sistema de monitorización continua para tener, sobre todo gasto cardiaco latido a latido, pero habrá que valorar su verdadera utilidad (¿se toman muchas decisiones con esta medida durante el ingreso?, ¿la técnica y la calibración son correctas?). Tras la conferencia de consenso del shock, el gold estándar para comprobar si los parámetros hemodinámicos son correctos ya no son los métodos contínuos sino la ecocardiografía doppler.
3) Uso de drogas vasoactivas.
-Si el paciente esta vasoplejico (RVS bajas) se iniciará noradrenalina. El objetivo no siempre será normalizar las resistencias, si hay una adecuada reserva miocárdica aunque los valores de RVS se encuentren en límite bajo de la normalidad, el individuo puede compensar esta situación elevando el gasto cardiaco. La idoneidad de este manejo lo marcará la evolución favorable de los parámetros de perfusión tisular (ej: si las resistencias son de 750 dynas pero el paciente aumenta diuresis, normaliza SVcO2…)
Debemos recordar que la sobredosificación de noradrenalina puede ser perniciosa por varios motivos: arritmogénica, si aumenta mucho la postcarga puede empeorar la contractilidad del ventrículo izquierdo y por lo tanto el GC, aumenta la postcarga de ventrículo derecho y puede participar como factor desencadenante de fallo ventricular derecho. Por todo ello aumenta la mortalidad cuanto más elevadas son las dosis. Para disminuir las dosis de noradrenalina se sugiere añadir vasopresina o adrenalina aunque hay solo moderada evidencia.
-La dopamina queda relegada a pacientes que tengan una bradiarritmia y hay evidencia en contra de usarla a dosis dopaminérgicas.
-La dobutamina es el inotrópico de primera línea. La dosificación se realizará con el objetivo de aumentar el gasto cardiaco, el transporte de oxígeno y la perfusión tisular en aquellos pacientes no respondedores a fluidoterapia.
La disfunción miocárdica sistólica de ventrículo izquierdo de la sepsis es definida como fracción de eyección (FE) <40% e índice cardiaco < 2 l/min/m2 (9). Hay que tener en cuenta que hay pacientes con disfunción sistólica pero mantienen gasto cardiaco adecuado a base de dilatación y taquicardia; esto implica que la FE no debe ser un parámetro ecográfico guía. Algunos estudios demuestran que este valor bajo aislado no aumenta la mortalidad.
Merece la pena comentar en este apartado que la valoración del DTI es importante cuando elijamos los inotrópicos; si bien un valor bajo de onda e (inferior a 9 cm/s) supone disfunción diastólica (10), que ha demostrado aumento de mortalidad en estos pacientes que presentan mala tolerancia a la taquicardia inducida por la sepsis o el empleo de inotrópicos. Llama la atención que en estas guías no comenten nada en este sentido cuando existe ya incluso un metanálisis con buen análisis multivariado donde se concluye que la disfunción diastólica del ventrículo izquierdo en el shock séptico aumenta la morbimortalidad. Incluso se ha visto que la disfunción diastólica inicial severa y reversible de estos pacientes puede ser secundaria al disbalance entre la oferta y demanda coronaria mientras el paciente no se encuentra adecuadamente replecionado, y que mejoraría tras la optimización de la fluidoterapia llegando el musculo cardiaco a la meseta del curva de Frank Starling
En esta situación se debería valorar sinergias de inotrópicos como levosimendan y dobutamina para evitar dosis elevadas de este último aunque sería prácticamente un uso compasivo pues no hay aun estudios que avalen esta combinación (11). Tampoco se hace hincapié en estas guías en el valor de disfunción del ventrículo derecho en la sepsis demostrada hace años por el grupo de Viellard Baron et al (9) y que se relacionaba también con alta mortalidad. En estos pacientes, para tratar esta disfunción, habría que probar si el ventrículo derecho responde a precarga sobre todo si no se ve excesivamente dilatado (relación VD/VI < 1), bajar poscarga (optimizar ventilación mecánica, disminuir hipercapnia, drenar drenajes pleurales moderados-severos…) y si no es suficiente optar también por dobutamina.
4) Uso de corticoides.
Con una buena reanimación hemodinámica salvo, si acaso, el paciente es tomador crónico de corticoides o tiene disfunción adrenal crónica.
5)Transfusión de hematíes.
Solo se recomienda transfundir hematíes por debajo de 7 g/dl si el paciente no tiene isquemia miocárdica, hipoxemia (PafiO2 <200) o hemorragia aguda en cuyo caso el target sería 9 g/dl.
Bibliografía
1. Rhodes A, Evans LE, Alhazzani W, Levy MM, Antonelli M, Ferrer R et al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016. Intensive Care Med. 2017 Jan 18. (PubMed) (HTML) (PDF)
2. Cecconi M, De Backer D, Antonelli M, Beale R, Bakker J, Hofer C et al Consensus on circulatory shock and hemodynamic monitoring. Task force of the European Society of Intensive Care Medicine. Intensive Care Med. 2014 Dec;40(12):1795-815. (PubMed) (HTML1) (HTML2) (PDF)
3. Balik M, Pachl J, Hendl J. Effects of the degree of tricuspid regurgitation on cardiac output measurements by thermodilution. Intensive Care Med 2002; 28:1117—1121. (PubMed) (HTML)
4. Muller L, Toumi M, Bousquet PJ, Riu-Poulenc B, Louart G, Candela D et al. AzuRéa Group. An increase in aortic blood flow after an infusion of 100 ml colloid over 1 minute can predict fluid responsiveness: the mini-fluid challenge study. Anesthesiology. 2011 Sep;115(3):541-7. (PubMed) (HTML)
5. Vieillard-Baron A, Chergui K, Rabiller A, Peyrouset O, Page B, Beauchet A, et al. Superior vena cava collapsibility as a gauge of volume status in ventilated septic patients. Intensive Care Med 2004; 30:1734—1739. (PubMed) (HTML)
6. Barbier C, Loubieres Y, Schmit C Hayon J, Ricôme JL, Jardin F, et al. Respiratory changes in inferior vena cava diameter are helpful in predicting fluid responsivess in ventilated septic patients. Intensive Care Med 2004; 30:(9):1740-6. (PubMed) (HTML)
7. Lamia B, Ochagavia A, Monnet X, Chemla D, Richard C, Teboul JL. Echocardiographic prediction of volume responsiveness in critically ill patients with spontaneously breathing activity. Intensive Care Med 2007, 33:1125-1132. (PubMed) (HTML)
8. Préau S, Saulnier F, Dewavrin F, Durocher A, Chagnon JL. Passive leg raising is predictive of fluid responsiveness in spontaneously breathing patients with severe sepsis or acute pancreatitis. Crit Care Med. 2010 Mar;38(3):819-25. (PubMed)
9. Vieillard-Baron A, Prin S, Chergui K, Dubourg O, Jardin F. Hemodynamic instability in sepsis: bedside assessment by Doppler echocardiography. Am J Respir Crit Care Med. 2003 Dec 1;168(11):1270-6. (PubMed) (HTML) (PDF)
10. Sanfilippo F, Corredor C, Fletcher N, Landesberg G, Benedetto U, Foex P et al Diastolic dysfunction and mortality in septic patients: a systematic review and meta-analysis Intensive Care Med (2015) 41:1004–1013. (PubMed) (HTML)
11. Morelli A, De Castro S, Teboul JL, Singer M, Rocco M, Conti G, et al(2005).Effects of levosimendan on systemic and regional hemodynamics in septic myocardial depression.Intensive Care Med 31:638-644. (PubMed) (HTML)