Ferreras Vega R (1), Méndez Marín MD (1), Rubio Pascual P (2)
(1) FEA anestesia, reanimación y terapia del dolor pediátrico, hospital 12 de Octubre, Madrid.
(2) Jefe de servicio de anestesia, reanimación y terapia del dolor pediátrico, hospital 12 de Octubre, Madrid.
Introducción
El agua es el principal componente de nuestra masa, especialmente en el paciente pediátrico, sobre todo en la etapa de neonato y lactante. Se distribuye en dos compartimientos, extracelular (LEC) e intracelular (LIC). El sodio es el principal catión del LEC, por esa razón su balance y regulación son vitales para mantener el funcionamiento celular y la perfusión de los tejidos.
Las alteraciones del sodio o disnatremias aumentan la morbimortalidad en el periodo perioperatorio. Debido a su importancia y a la frecuente aparición en la práctica habitual, existen múltiples guías para el diagnóstico diferencial y corrección de las mismas. Sin embargo, nuestra práctica clínica ocurre en un contexto determinado, el peri- y postoperatorio. Esto hace que podamos enfocar de forma más dirigida el origen de la hiponatremia
Objetivos
El objetivo de esta revisión descriptiva, es resumir la fisiopatología de la hiponatremia especialmente enfocada a un contexto quirúrgico y a sus implicaciones anestésicas.
Métodos
La revisión ha sido realizada a partir de la información extraída de: 2 guías clínicas y 12 publicaciones originales.
Los artículos referenciados tienen un mínimo de 7 citas y las guías usadas están avaladas por sociedades nacionales, referenciadas en la bibliografía.
Descripción
1. Conceptos básicos:
Para abordar la hiponatremia repasaremos una serie de conceptos básicos.
a) Osmolaridad y Osmolalidad: osmolalidad cuando la concentración es expresada en osmoles por Kg de agua. Osmolaridad si es en osmoles por litro de solución. En la práctica, ambos términos se utilizan de forma indistinta en el lenguaje de la clínica cotidiana, pues la diferencia suele ser pequeña. En el caso del plasma hablaremos de Osmolalidad plasmática efectiva (Osmp). La regulación del volumen de LIC depende principalmente de Osmp. Cómo el sodio es el principal ion del LEC, la natremia junto a la glucemia pueden estimar la osmolalidad plasmática efectiva, que es la que afecta al flujo de agua (ecuación 1).
Ecuación 1: OSMOLALIDAD PLASMÁTICA EFECTIVA

b) Cuantificación de excreción agua libre: cantidad de agua libre que es eliminada a nivel renal, por unidad de tiempo. Su valor nos avisa de si hay reabsorción o excreción de agua. La hallamos mediante la siguiente fórmula (ecuación 2).
Ecuación 2: ACLARAMIENTO DE AGUA LIBRE DE ELECTROLITOS

Es considerada como una fórmula de gran utilidad para estimar la capacidad renal de excretar agua libre y una idea de la posible respuesta a la restricción hídrica.
c) Sodio urinario (Na o): Diferencia estados de hipovolemia de normovolemia vs euvolemia (si no hay uso de diuréticos). En hiponatremia, se espera un aumento en la reabsorción tubular de sodio (sodio urinario < 10 mEq/L). Mientras que, en > 20 mEq/L, indica una posible alteración en la regulación del sodio.
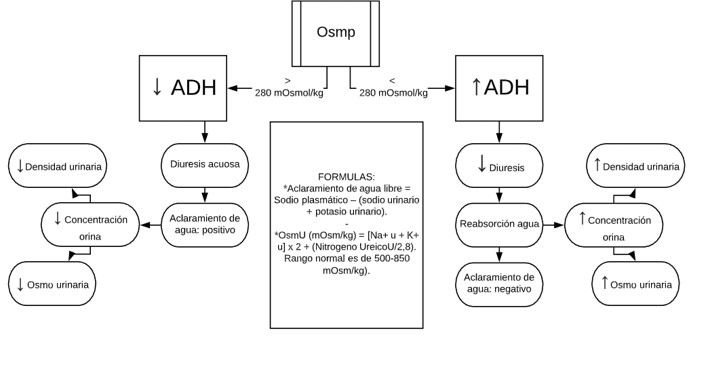
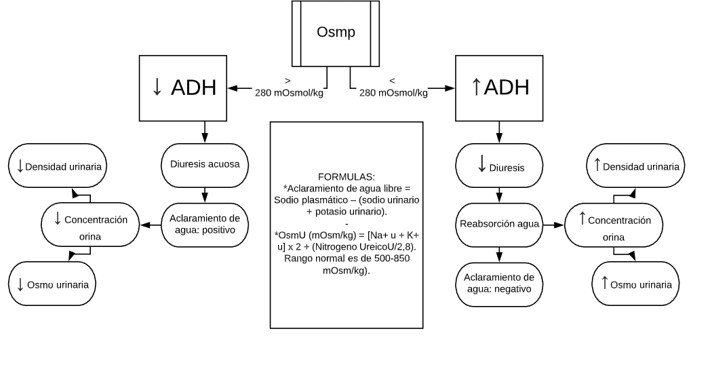
d) Hormona antidiurética (ADH) o vasopresina: aumenta la reabsorción de agua libre en los túbulos colectores, aumentando la osmolalidad urinaria y disminuyendo el volumen urinario, y tiende a producir hiponatremia. La cuantificación de la excreción de agua libre y la osmolaridad urinaria evalúan la función de la ADH. Algoritmo 1.
Algoritmo 1. RESUMEN DE LA REGULACIÓN DE LA ADH FUNCIONAMIENYO DE ADH.
e) Agua corporal total: Su cálculo va a depender del sexo, altura, edad y masa del paciente. Existen algunas revisiones sobre esta fórmula (1). No obstante, es habitual el uso de estimaciones simplificadas (tabla-1).
Tabla 1. Distribución del agua corporal en función de la etapa de desarrollo en pediatría.
| AGUA COPORAL TOTAL (ACT) en Litros |
| Prematuro: 0.8 x peso (kg) |
| Lactante menor de 1 año=0.70 x peso (kg) |
| Escolar: 0.6x kg varones y 0.5x kg en mujeres |
Tras haber repasado los conceptos fisiológicos básicos, nos centramos en la hiponatremia en el contexto quirúrgico.
2. Hiponatremia (hNa):
Si objetivamos una concentración sérica de sodio menor a 135 mmol por litro, se considera hNa, que es la causa más común de alteración hidroelectrolítica en niños (1).
Definimos hiponatremia leve si el sodio medido por electrodo específico de iones se encuentra entre 130 y 135mmol/L, moderada entre 125 y 129mmol/L y grave cuando es <125mmol/L.
Las manifestaciones clínicas se dan principalmente a nivel neurológico (letargo, estupor, coma). Dependen tanto de la gravedad de la hiponatremia (tabla-2), como de su velocidad de instalación. En las formas de aparición lenta (10 a 14 días) es posible encontrar un sodio plasmático menor a 120 mEq/l en un paciente asintomático.
Tabla 2. Relación de gravedad de hiponatremia con síntomas.
| Sodio 130- 135 mEq/L: cefalea, irritabilidad, disminución de la atención, alteraciones en la marcha |
| 120-130 mEq/L, náuseas, vómitos, confusión, desorientación, somnolencia, bradipsiquia |
| < 120 mEq/L, estupor, convulsiones, coma, depresión respiratoria. |
En el contexto quirúrgico, vamos a clasificar la hNa en el niño, dependiendo de si ocurre en el preoperatorio o postoperatorio (Algoritmo-2).
Algoritmo 2: diagnóstico diferencial de la hiponatremia en el contexto anestésico, del paciente pediátrico.
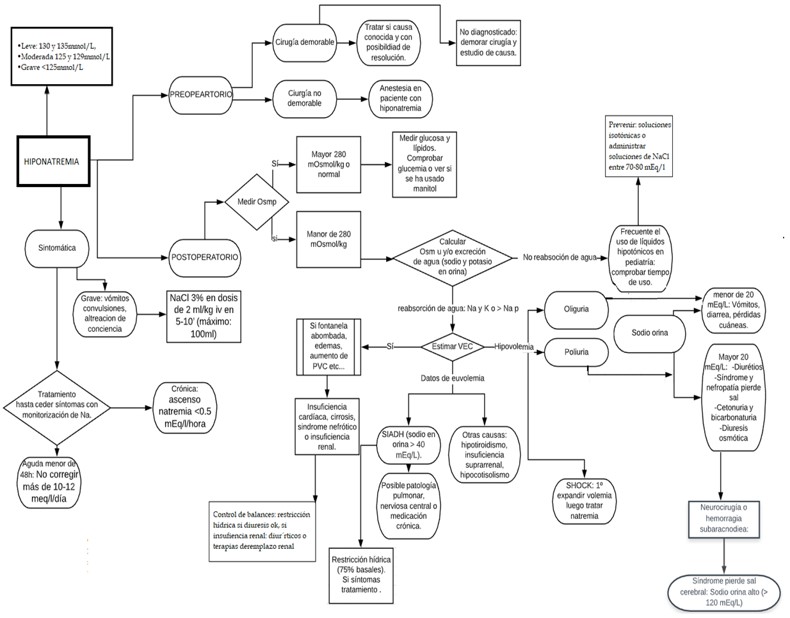
Comentarios al algoritmo:
a) Hiponatremia con hiperglucemia: estimaremos el sodio corregido con la cifra de glucemia. (ecuación 3).
Ecuación 3: SODIO CORREGIDO EN HIPERGLUCEMIA
b) Corrección con NaCl al 3%: la hiponatremia con síntomas moderados o graves se beneficia del tratamiento con suero salino hipertónico 3%. Aunque, no suele estar disponible y puede ser necesaria su elaboración. El SSN al 3% se prepara añadiendo 11 ml de suero al 20% a 89 ml de suero 0.9%, 1 litro de esta solución 3% tiene 513mEq de sodio. Aproximadamente 1 ml/kg de Suero 3% incrementa el Na sérico en 1 mEq/L.
En el caso de síntomas graves, debemos corregir el sodio hasta la desaparición de estos (sobre todo convulsiones). En los casos de coma o convulsiones iniciaremos cloruro de sodio al 3% a 2 ml/kg iv en 5-10’ (máximo: 100ml), repitiendo hasta resolución de síntomas.
Continuaremos con la corrección, si es necesario, pudiendo llegar 1 mEq/l/h en los casos crónicos y hasta 2 mEq/L/h en los agudos, pero igualmente es necesario respetar el umbral de los 8-10 mEq/l/24h.
La fórmula de Adrogué–Madias (ecuación 4) (2) permite calcular el cambio de la natremia esperado con la corrección. No obstante, puede infraestimar el cambio en casos de hiponatremia menor a 120 mEq/L (3). En patología con pérdidas importantes de volemia (diabetes insípida nefrogénica grave, hiperglucemia) el sodio debe ser medido cada 4 horas durante el primer día (4). Si la situación es estable puede hacerse cada 6 horas (4). Pero en pacientes inestables puede ser necesaria horaria (4).
Si se necesita el uso de suero hipertónico 3%, el proceso es el siguiente:
Ecuación 4: VELOCIDAD DE REPOSICIÓN (ml/h)
Ejemplo: lactante de 4 meses 8 kg, sodio plasmático de 125 mEq/L, y queremos llegar a los 135 mEq/L, a un ritmo de ascenso de 0.5 mEq/L.
- Cálculos: ACT en lactante 10kg x 0.7 L/Kg= 7 L. Gradiente Na =10 mEq/L (135-125). Déficit de sodio= 70 mEq (7Lx10mEq/L)
- Tiempo de terapia10 mEq/L/0.5 mEq/L/h=20 horas (tiempo de terapia).
- Velocidad de NaCl para subir a 140 mEq/L, el sodio a ratio de: 0.5 mEq/kg/h.
- 1000×0.5x (7+1) / (513-130) = 10 ml /h durante 20h de una solución de suero 3% para corregir el déficit deseado en ese peso y esa edad, sin sobrepasar los 0.5 mEq/L/h. Se debe monitorizar cada 3-4 h para variar ritmo de infusión ya que se tratan de cálculos matemáticos y pueden existir variaciones importantes.
c) Riesgos de la corrección:Es conocido que la corrección de la hiponatremia de forma agresiva, puede tener consecuencias fatales para el niño. La mielinosis pontina puede llevar a la muerte y entre sus síntomas tenemos el deterioro del nivel de conciencia, parestesias, disfagia y mutismo.
Desde el año 1982, está descrito este riesgo asociado a la corrección de la natremia, el llamado síndrome de desmielinización osmótica, que conduce a la mielinolisis central pontina o extrapontina.
Para prevenirla, usaremos ratios de corrección determinados. En las hNa crónicas sintomáticas, no podemos superar los 0.5 mEq/l/hora, los 8-10 mEq/24 h (5) (10-12 para otros autores) o los 18 mEq/48h.
2.1 Hiponatremia en el preoperatorio
Preoperatorio: el niño puede tener una hiponatremia con una causa filiada. En este caso y con una cirugía no emergente, tendremos que averiguar si es aguda o crónica:
• Si se trata trastorno crónico y estable (ya optimizado), procederemos a la cirugía teniendo en cuenta las consideraciones anestésicas que más adelante veremos.
• Sin embargo, si se trata de una situación aguda, actuaremos en función de la urgencia quirúrgica y la capacidad de corrección de la disnatremia. Una de las causas más frecuentes que asocian hiponatremia y posibilidad de cirugía, en el niño, son las pérdidas gastrointestinales de agua y electrolitos (vómitos, diarrea). En el lactante la hiponatremia es más frecuentemente debida a hipovolemia (Osmp disminuida, urinaria aumentada con absorción de agua y sodio en orina). Pueden poner en peligro la vida del paciente y necesitar cirugía (vólvulo intestinal). Hay que determinar claramente la urgencia quirúrgica vs la situación emergente. En algunos casos, la resolución de las alteraciones metabólicas se indica antes de comenzar el acto anestésico, como en la estenosis hipertrófica del píloro.
• Si no se encuentra diagnosticada la causa, valoraremos la gravedad de los síntomas, el tiempo de instauración y realizaremos un diagnóstico diferencial (Algoritmo 2). La exploración del niño es fundamental y esta difiere del adulto (sobre todo en neonatos y lactantes con fontanela abierta).
2.2 Hiponatremia en el postoperatorio del niño:
En el postoperatorio del paciente pediátrico, requieren especial mención el SIADH, la deshidratación y el síndrome pierde sal cerebral.
2.2.a. Secreción inadecuada de ADH (SIADH)
Es la causa más frecuente de hiponatremia euvolémica en pacientes hospitalizados (6). Hay que descartar fármacos que producen esta patología, así como afecciones pulmonares o del sistema nervioso central (SNC). Pero sobre todo en nuestro medio lo vamos a ver en estados de ansiedad, dolor, stress, náuseas, que son frecuentes en el postoperatorio
El diagnóstico diferencial tiene que tener en cuenta el sodio urinario mayor a 40 mq/L y los balances hídricos. Ofrece mayor dificultad su diferenciación con el síndrome pierde sal cerebral (SPSC). La principal diferencia es la hipovolemia y deshidratación, con balances negativos, más evidente en SPSC. La diuresis suele ser menor de 1 ml/kg/h, aunque no siempre es así. Recordar que en el paciente pediátrico la oliguria se considera cuando el débito es menor de 1ml/kg/h en lactantes y < 500 ml/1.73 m2 en niños mayores.
El SIADH suele responder a una restricción hídrica: 75% de basales en situaciones agudas pudiendo llevar al 50% en crónicas.
Teniendo en cuenta las basales según la fórmula de Holliday-Segar, se disminuirá esta última un 25%, para conseguir esa restricción del 75%.
Si esta terapia no es suficiente para normalizar el sodio, se podrá efectuar una sobrecarga con urea. La urea en dosis de 10 a 40 g / día produce diuresis osmótica y una mayor excreción de agua. Un procedimiento fácil es disolver 15-30 g de urea en un vaso de jugo de naranja y administrar dos o tres vasos al día después de las comidas. El inconveniente de la urea es su sabor. También se ha usado clásicamente la furosemida (0.1 mg/kg dosis inicial). La demeclonida no es de uso frecuente pero también puede considerarse. El uso de Vaptanes aún no está aprobado en la población pediátrica, pero se usa fuera de guía.
2.2.b. Hiponatremia hipovolémica
La fisiología hemodinámica del niño (sobre todo lactante y neonato) es diferente al adulto. En los lactantes el gasto cardíaco se relaciona directamente con la frecuencia cardíaca y tiene una importancia mayor cuanto más pequeño sea el niño (GC= Volumen de eyección x Frecuencia cardíaca). El lactante y sobre todo el niño prematuro, tolera mal la depleción de volumen. Esto se debe a que su volumen sistólico no varía, dependiendo su gasto cardíaco principalmente de la frecuencia cardíaca, siendo este mecanismo de compensación limitado.
En la exploración de un paciente hipovolémico pediátrico es necesario tener en cuenta los umbrales fisiológicos de su edad. Además, la hipotensión es un signo tardío de hipovolemia, necesitando poner especial atención en el manejo del shock (7). Este, debe ser tratado antes que la hiponatremia (dosis iniciales entre 10-20 ml/kg 15 minutos), estabilizando al paciente (7). Entre las causas más frecuentes de hiponatremia hipovolémica en el niño están la diarrea, hemorragias y quemaduras.
2.2.c. Síndrome pierde sal cerebral (SPSC)
Puede ocurrir durante el postoperatorio de cirugía intracerebral, aunque la causa más frecuente es la hemorragia subaracnoidea (8). En el SPSC existe una pérdida renal de sodio, secundario a un daño cerebral, que desemboca en una hipovolemia (poliuria e hipovolemia). En situación fisiológica, ante un estado de hipovolemia e hiponatremia, esperaríamos encontrar un sodio en orina menor de 20 mEq/L. Sin embargo, no ocurre en este síndrome, postulándose como origen de este cuadro una disfunción del péptido natriurético auricular. Además, encontraremos sodios urinarios mayores (≥120 mEq/L) incluso que en el SIADH (≥40-60mEq/L).
El tratamiento está basado en dos pilares: tratar la causa subyacente y reponer volumen mientras tratamos la hiponatremia. Para la reposición, usamos solución salina isotónica en casos leves o moderados, mientras que la solución hipertónica 3% se reserva para casos más graves. La fludrocortisona 0,1-0,2 mg /12h ha mostrado resultados favorables, manteniéndose hasta estabilizar el cuadro. Es necesario un seguimiento de al menos dos semanas, con determinaciones periódicas de la natremia.
2.3. Prevención de hiponatremia en el paciente pediátrico: uso de fluidoterapia isotónica.
En el paciente pediátrico existe una tendencia al mantenimiento con sueroterapia hipotónica. En el año 2006, fueron publicados los resultados de una encuesta realizada en Reino Unido sobre el tipo de soluciones usadas en el niño para el mantenimiento previo a la cirugía. El uso de soluciones hipotónicas era muy frecuente (9).
Por otra parte, si además el niño se somete a una cirugía dónde el riesgo de desarrollar SIADH está aumentado, se eleva la incidencia de hiponatremia. Como resultado, aparecieron estudios (10,11) que abogaban por el uso de soluciones isotónicas en el contexto quirúrgico como forma de prevención de la hiponatremia.
2.4 Implicaciones anestésicas del niño con hiponatremia:
La hiponatremia es a menudo una manifestación de enfermedad subyacente, por lo que el historial preanestésico es fundamental para elaborar una estrategia de abordaje.
El edema cerebral suele desaparecer al alcanzar niveles séricos de 130 mEq/L, eligiéndose arbitrariamente una concentración de 131 mEq/L como el límite inferior de sodio para posponer una intervención quirúrgica electiva (12). Concentraciones menores a 130 pueden provocar edema cerebral y agitación postoperatoria, además de la disminución de las necesidades de hipnosis.
La anestesia regional nos permite evaluar la clínica neurológica, pero está limitada en niños por la necesidad de sedaciones profundas, que se requiere en ocasiones para mitigar la ansiedad.
Conclusiones
La hiponatremia en un contexto quirúrgico eleva la morbimortalidad del procedimiento. Además, su manejo requiere una curva de aprendizaje importante, debido a la cantidad de formulaciones para su tratamiento y a los diagnósticos diferenciales. No obstante, la aparición de hiponatremia en el postoperatorio puede orientarnos en el diagnóstico diferencial. Por esta razón, el uso de algoritmos orientados a un ámbito concreto, junto a calculadoras médicas, puede ayudarnos en el manejo de las disnatremias.
Así, el autor de este artículo pone a disposición del lector una app de creación propia que resume lo descrito en este artículo, disponible de forma gratuita en el siguiente enlace:
https://play.google.com/store/apps/details?id=appinventor.ai_rubenferrerasvega87.Sodio2

Bibliografía
1. Upadhyay A, Jaber BL, Madias NE. Incidence and prevalence of hyponatremia. Am J Med. 2006; 119:S30-5. DOI: 10.7861/clinmedicine.17-3-263 (HTML)
2. Adrogue, H.J and Madias, N.E. Hyponatremia N Eng J Med; 2000: 342:1581-1585. PMID: 10824078 DOI: 10.1056/NEJM200005253422107 (PubMed)
3. Berl T. The Adrogué–Madias formula revisited. Clin J Am Soc Nephrol; 2007: 1098–1099 PMID: 17928464 DOI: 10.2215/CJN.03300807 (HTML)
4. Tomlinson B.E., Pierides A.M., Bradley W.G. (1976) Central pontine myelinolysis. Q J Med 179: 373–386. PMID: 948540 (PubMed)
5. Sterns R.H., Riggs J.E., Schochet S.S. (1986) Osmotic demyelination syndrome following correction of hyponatremia. N Engl J Med; 1986: 314: 535–542. PMID: 3713747 DOI: 10.1056/NEJM198606123142402 (PubMed)
6. Upadhyay A, Jaber BL, Madias NE. Incidence and prevalence of hyponatremia. Am J Med Am J Med. 2006;119(7 Suppl 1):S30-5. PMID: 16843082 DOI: 10.1016/j.amjmed.2006.05.005 (HTML)
7. Ellis S.J. Severe hyponatremia: complications and treatment. Q J Med; 1995: 88: 905–909 PMID: 8593551 (PubMed)
8. Arieff AI, Gabbai R, Goldfine ID. Cerebral Salt-Wasting Syndrome: Diagnosis by Urine Sodium Excretion. Am J Med Sci. 2017;354(4):350-354. DOI: 10.1016/j.amjms.2017.05.007. (PubMed)
9. Way C, Dhamrait R, Wade A, Walker I. Perioperative fluid therapy in children: a survey of current prescribing practice. Br J Anaesth. 2006 S;97(3):371-9. PMID: 16873386 DOI: 10.1093/bja/ael185 (PubMed)
10. Neville KA, Sandeman DJ, Rubinstein A, Henry GM, McGlynn M, Walker JL. Prevention of hyponatremia during maintenance intravenous fluid administration: a prospective randomized study of fluid type versus fluid rate. J Pediatr. 2010;156(2):313-9. DOI: 10.1016/j.jpeds.2009.07.059 PMID: 19818450 (PubMed)
11. Sterns RH. Evidence for Managing Hypernatremia: Is It Just Hyponatremia in Reverse? Clin J Am Soc Nephrol. 2019 7;14(5):645-647 PMCID: PMC6500936 DOI: 10.2215/CJN.02950319 (PubMed)
12. Hirsch IA, Tomlinson DL, Slogoff S: The overstatedrik of preoperative hypokalemia Anesth Analg 198867: 131-136. PMID: 3341565 (PubMed)
Lecturas recomendadas
https://www.nefrologiaaldia.org/es-articulo-trastornos-del-agua-disnatremias-197
Guías clínicas
http://secip.com/wp-content/uploads/2018/06/Protocolo-SIADH-Diabetes-Insipida-SDR-Pierde-Sal.pdf