Artículo Original: Beaubien-Souligny, W., Rola, P., Haycock, K., Bouchard, J., Lamarche, Y., Spiegel, R., Denault, A. Y. Quantifying systemic congestion with Point-Of-Care ultrasound: development of the venous excess ultrasound grading system. Ultrasound J. 2020; 12: 1-12.DOI: 10.1186/s13089-020-00163-w (HTML)
García-Montoto Pérez F.
MD. PhD. EDAIC.
Coordinador UCI de Anestesia.Tutor MIR.
Complejo Hospitalario Universitario de Cáceres.
Especialista en Anestesiología y Reanimación.
Introducción
El manejo hemodinámico del paciente crítico se ha enfocado tradicionalmente al mantenimiento de un adecuado gasto cardiaco y de la presión arterial con la administración de fluidos y de vasopresores o inotrópicos.
Sin embargo, la perfusión de los diferentes órganos se ve afectada por otros factores, entre ellos por la congestión venosa, no siendo la presión venosa central (PVC) un parámetro que permita una valoración fiable de la misma (1).
Esto es especialmente notable en pacientes con sobrecarga hídrica, insuficiencia del ventrículo derecho o hipertensión pulmonar. Si además se produce un fallo renal esta situación se verá agravada por una mayor congestión venosa. La perfusión de los órganos vitales se verá dificultada por el edema intersticial producido por una elevación de la presión hidrostática, así como una disfunción de la barrera endotelial. Esta situación será mayor en órganos encapsulados (riñón y cerebro) donde la elevación rápida de la presión intersticial producirá un descenso del flujo sanguíneo. Además esto conlleva un aumento de las distancias de difusión dentro del intersticio, perjudicando aún más la oxigenación de los mismos.
Por todo lo anterior, actualmente es un desafío clínico disponer de un sistema que mida la congestión venosa de forma clara y fiable. Aunque se ha asociado el aumento de la presión venosa central (PVC) con complicaciones por congestión, no está claro qué niveles implican la necesidad de una actuación clínica. Otros parámetros como el balance hídrico acumulado, las variaciones de peso o el examen físico para valorar el edema tienen limitaciones importantes y pueden no ser proporcionales a la congestión venosa real existente (2).
La ecografía POCUS permite a los clínicos realizar una valoración a pie de cama de la situación hemodinámica a tiempo real. Con las modalidades Doppler podemos evaluar el volumen y los factores ligados a la congestión así como los límites de la capacitancia venosa que darán un aumento rápido de las presiones. Se han propuesto ya varios marcadores, así como las consecuencias que implica el aumento de la congestión venosa tras ser medida. El problema aparece con la interpretación de forma aislada de estos marcadores. Por ello, la combinación de varias de estas medidas puede aumentar la utilidad clínica para detectar de forma fiable la congestión venosa.
Objetivos
El objetivo principal del estudio analizado fue desarrollar un sistema de clasificación de la congestión venosa por ultrasonido (VExUS) y validar su potencial valor clínico en la predicción de la aparición de la insuficiencia renal aguda (IRA) tras cirugía cardiaca usando los datos previos existentes de un estudio de cohortes prospectivo reciente (3).
Como objetivo secundario se planteó comparar su utilidad clínica frente a las mediciones de PVC.
Material y métodos
El estudio fue un diseño post-hoc observacional prospectivo en un solo centro terciario que incluyó a 145 pacientes adultos sometidos a cirugía cardiaca. Se realizó en un periodo de tiempo comprendido desde agosto 2016 a julio 2017.
Se incluyeron pacientes programados para cirugía cardiaca con bomba extracorpórea ysin patología aguda crítica.Establecieron una descripción de los criterios de inclusión y exclusión (3). Cabe destacar que aquellos pacientes con un diagnóstico previo de insuficiencia renal aguda (IRA) o delirio fueron excluidos del estudio. Así como aquellos pacientes con condicionantes clínicos que pudieran artefactar las mediciones Doppler de la vena porta (como cirrosis o trombosis portal), o con enfermedad renal crónica grave (FG < 15 mL/min) o en diálisis.
Las medidas ecográficas POCUS que se realizaron fueron: Doppler en vena hepática, vena porta y venas intra-renales, así como medición de la vena cava inferior (VCI). Se realizaron en cinco momentos: previo a la cirugía, al ingreso en la UCI, y en los días 1 al 3 de estancia en UCI. El método para realizar las mediciones ecográficas estádescrito en una publicación previa (3) y se añadió el registro con ECG para valorar las fases de las ondas a estudio. Cabe destacar que la medición de la VCI se realizó en la zona intra-hepática a 2 cm de la unión con las venas hepáticas, en una visión longitudinal en el foco sub-xifoideo como se describe en la literatura.
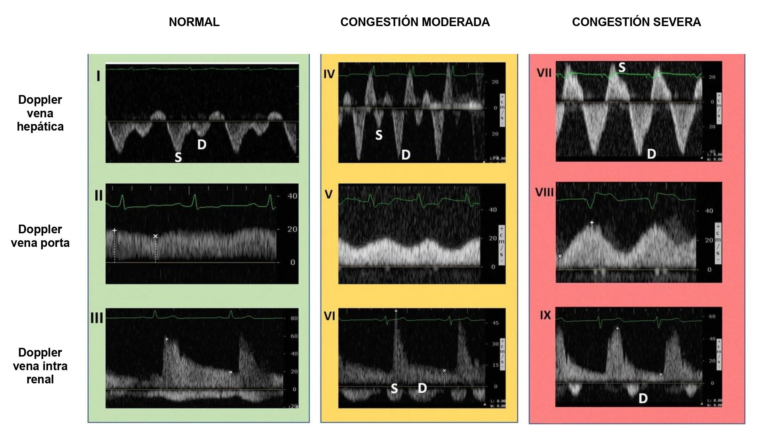
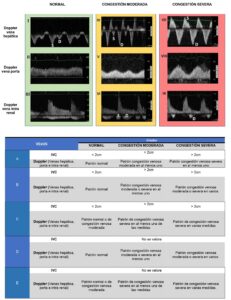
Basado en la idea original de uno de los autores (Dr. Philippe Rola) un equipo multidisciplinar compuesto por anestesiólogos, nefrólogos, médicos de urgencias e intensivistas desarrollaron un prototipo de congestión venosa que llamaron VExUS (figura 1). Propusieron cinco patrones (A-E) según los parámetros observados. Estos parámetros combinaban el diámetro de la VCI y la forma de la onda Doppler de las venas hepáticas, vena porta y venas inter-lobulares renales. El Doppler hepático se consideraba moderadamente alterado cuando el componente de la onda sistólica (S) era de menor magnitud que el componente de la onda diastólica; y se consideraba gravemente alterada cuando el componente sistólico estaba invertido. El Doppler portal se consideraba moderadamente alterado cuando se observaba una variación en la velocidad durante el ciclo cardiaco entre 30-50% y se consideraba gravemente alterado si era>50%. El Doppler de las venas inter-lobulares renales se consideraba moderadamente alterado cuando existía una discontinuidad entre la fase sistólica y diastólica y se consideraba gravemente alterado si solo se apreciaba la fase diastólica durante el ciclo cardiaco.
Presentaron la asociación de cada evaluación con cada grado VExUS, y la diferencia entre los diferentes grados se midió usando un test ANOVA de una vía o un test Kruskall-Wallis según estuviera indicado por la distribución de los datos. Cuando existió un resultado significativo (p<0.05) se pasó una prueba post-hoc de Bonferroni.
Resultados
Tras la cirugía, 49 pacientes del total de 145 tuvieron IRA pero ninguno necesito técnicas de reemplazo renal.
La congestión venosa grave (grado 3) fue mucho menos frecuente en los sistemas C y E comparado con el resto (A, B y D). Hubo una asociación con niveles más altos de EuroSCORE II y los grados de congestión grave.
En el periodo postoperatorio la presencia de congestión grave (grado 3) estuvo asociada con la aparición de IRA en todos los modelos. Pero fue el sistema VExUS C el que presentó la asociación más fuerte (HR 3.69, IC 1.65-8.24, p=0.001). Dicha asociación se mantuvo tras ajustarla con el riesgo basal de IRA, así como con la escala vasopresores-inotrópicos (VIS). Solo el sistema VExUS C para la congestión moderada (grado 2) tuvo una asociación con la presencia de IRA (HR 2.65, IC 1.07-6.60 p=0.036).
Al evaluarlo al ingreso en la UCI tras la cirugía, la congestión grave (grado 3) definida por el sistema VExUS C tuvo una alta especificidad (96% IC 89-99%) pero baja sensibilidad (27% IC 15-41%) para diagnosticar el desarrollo de IRA, con un LR (+LR 6.37 IC 2.19-18.5) que supero el rendimiento del resto de sistemas. Todos los sistemas tuvieron una baja sensibilidad (< 75%). Por otro lado ninguno de los datos de PVC estudiados, o de las medidas ecográficas estudiadas individualmente superaron al grado 3 del VExUS C con su +LR.
El resto de marcadores de congestión (balance hídrico, NT-pro-BNP y PVC) se asociaron con la congestión grave (grado 3) en todos los sistemas VExUS estudiados. Pero la asociación fue más fuerte con el grado 3 del sistema VExUS C para el balance hídrico y la PVC.
Con estos resultados que aporta el estudio, los autores encuentran que la congestión grave (grado 3 VExUS C) definida como alteraciones graves del flujo en varios patrones junto con la dilatación de la VCI (>2cm) tiene una asociación fuerte con el desarrollo de IRA en comparación con otros hallazgos ecográficos. Además es importante destacar que dicha asociación se mantiene tras ajustar con el riesgo conocido de IRA así como con la necesidad de vasopresores-inotrópicos (VIS) tras la cirugía. Tuvo una alta especificidad, aún con una sensibilidad baja, con un LH + moderado superando los puntos de corte de medición de la PVC. Si se observaba solo la PVC, esta tuvo un bajo rendimiento diagnóstico con una especificidad de 41%,lo que apunta a que no es un parámetro con suficiente fuerza para detectar la congestión clínicamente significativa. En cualquier caso, la asociación de la PVC en los sistemas VExUS mejoró levemente su especificidad, por lo que no debe descartarse su uso conjunto.
Discusión
Nos encontramos ante un estudio con un desarrollo muy serio y bien establecido. Plantean un objetivo primario clarocon una implicación clínica directa.
Tiene una adecuada validez interna, los resultados claramente son aplicables a la población estudiada y permiten que sean reproducibles. La mayor limitación es su validez externa, y son los propios autores los que inciden en la limitación de ser un estudio de un solo centro y en una muestra muy concreta, pacientes postoperados de cirugía cardiaca. Tiene por tanto un sesgo de selección, por lo que ellos sugieren que deben realizarse más estudios, en pacientes con situaciones clínicas diferentes. Por otra parte, perciben cierto grado de error aleatorio, y sugieren que podría corregirse con una muestra más amplia, a pesar de que la muestra parecería adecuada a priori.
Es importante destacar que la asociación de la congestión venosa a la presencia de IRA tiene una alta especificidad. Por ello cuando no exista un grado 3 VExUS C podríamos confirmar que no se desarrollará IRA. Pero su baja sensibilidad nos debe recordar que la presencia de IRA no será solo debido a la congestión, y que la alteración de la permeabilidad jugará un papel fundamental en la situación deletérea. Esto será de especial importancia en el shock distributivo.
Que haya una pequeña proporción de pacientes con signos de congestión venosa grave sin IRA apunta al hecho ya conocido de que la perfusión depende también del flujo arterial. Por ello, la estrategia dirigida a mejorar la perfusión de órganos no puede pivotar solo en la valoración de la congestión venosa, sino que debe incluir la información de la perfusión arterial.
En un completo análisis crítico por parte de los propios autores describen que al ser un estudio post-hoc faltan parámetros que consideran que hubieran sido de gran ayuda. Principalmente la valoración ecográfica pulmonar y la determinación del agua extrapulmonar.
Las diferentes medidas ecográficas están perfectamente definidas, detallando de forma objetiva los parámetros a estudio, y las características que permiten clasificarlas como normal, congestión moderada y congestión grave. También se establece dónde medirlo, qué modo usar y que patrón es necesario que esté alterado, aunque sea referenciado a diversos artículos, algunos de propia autoría. Este punto es de especial interés, sobre todo porque una limitación de la ecografía es la variabilidad interoperador, por ello es de vital importancia una claridad extrema para cada parámetro incluido en el índice VExUS. Quizás debamos ser críticos en que la validación y descripción de las medidas que se aportan como referencias recae sobre el mismo equipo investigador, y diferentes publicaciones aportadas que son solo de ellos mismos.
Por otro lado, como nos recuerdan los propios autores, no conviene olvidar las limitaciones de cada marcador ecográfico que conforma el VExUS. Así la vena hepática está muy influida por la insuficiencia tricuspídea, la vena porta y la PVC dan importantes falsos positivos en población joven y muy deportista y el Doppler venoso intra-renal técnicamente es más difícil de medir. De ahí la importancia de la suma de los cuatro parámetros.
Los resultados son de un interés manifiesto. Aportan una vía de investigación con un novedoso método POCUS para valorar la congestión. Tienen un tratamiento muy detallado, buscando afianzar sus resultados al cruzar el estudio con la probabilidad de IRA previa a la cirugía y con la escala VIS.
Creo que es una herramienta muy útil para validar en diferentes contextos clínicos de forma inmediata, y un gran punto de partida para realizar nuevos estudios que nos permitan aumentar la capacidad de valorar la congestión venosa. Lo ideal por tanto sería sumar esta herramienta a las ya establecidas en el manejo hemodinámico y sus implicaciones clínicas. Un grupo de pacientes de especial interés serán aquellos con shock séptico, un tipo de shock distributivo con alteración en la permeabilidad de membranas, y con un riesgo importante de sufrir las consecuencias de un exceso de resucitación hídrica.
Todos los estudios POCUS en general, y este en particular, establecen unos beneficios potenciales con un mínimo riesgo para el paciente. El coste principal será el de los equipos y la formación del personal, pero está superado con creces por la capacidad diagnóstica y versatilidad POCUS.
Por último, otra de las grandes virtudes del estudio radica en las figuras que presenta. Especialmente aquella que presenta claramente los patrones del nuevo diseño VExUS, así como la que presenta la curva de rendimiento diagnóstico o curva ROC. La información de las tablas es clara y permite un seguimiento conciso con la metodología descrita.
Conclusión
Nos encontramos ante un artículo de enorme relevancia, ya que abre la puerta a la valoración con POCUS de la congestión venosa.Así, este novedoso sistema de clasificación de congestión venosa (VExUS) está basado en la combinación de múltiples hallazgos ecográficos. La presencia de al menos dos alteraciones graves (Doppler en vena hepática, portal o intra-renal) con una VCI ≥2 cm de diámetro al ingreso en la UCI tras una cirugía cardiaca indica un alto riesgo de sufrir IRA postoperatorio.
El manejo hemodinámico del paciente crítico se ha enfocado tradicionalmente al mantenimiento de un adecuado gasto cardiaco y de la presión arterial con la administración de fluidos y de vasopresores o inotrópicos. Pero es ya también conocido que una terapia hídrica restrictiva, independientemente de líquido utilizado, tiene un efecto beneficioso sobre la mortalidad y que ha dado lugar a la propuesta del protocolo ROSE (4). Además, existe consenso en que la sobrecarga hídrica y la insuficiencia del ventrículo derecho se asocian a lesiones en múltiples órganos y efectos adversos (5). La ecocardiografía como Point-Of-Care es una herramienta que nos permite una valoración funcional de la situación hemodinámica del paciente con shock, que podemos centrar en el cálculo del volumen sistólico, con la integral de la velocidad por el tiempo (IVT). Mercadal et al nos presentan una propuesta que permite realizar una valoración de los diferentes tipos de shock y su abordaje, conjuntamente con la clínica (valoración de la perfusión), intentando diferenciar la patología crónica de la aguda (6). Con la propuesta de este artículo tenemos la posibilidad de cerrar el sistema de valoración hemodinámica incluyendo la evaluación de la congestión venosa, y así adecuar la necesidad hídrica real y poder ser más restrictivos.
Finalmente, debemos remarcar la necesidad de llevar a cabo más estudios para validar el sistema VExUS en diferentes contextos clínicos, que confirmen los criterios óptimos y determinen si puede usarse para individualizar el manejo hemodinámico de la congestión venosa y por tanto de la perfusión de órganos.
Bibliografía
- De Backer D, Vincent J-L Should we measure the central venous pressure to guide fluid management? Ten answers to 10 questions. Crit Care. 2018; 22:43 (HTML)
- Cook DJ, Simel DL. The rational clinical examination. Does this patient have abnormal central venous pressure? JAMA. 1996;275:630–634 (HTML)
- Beaubien‐Souligny, W., Benkreira, A., Robillard, P., Bouabdallaoui, N., Chassé, M., Desjardins, G., et al. Alterations in portal vein flow and intrarenal venous flow are associated with acute kidney injury after cardiac surgery: a prospective observational cohort study.J Am HeartAssoc. 2018;7(19): e009961.doi:10.1161/JAHA.118.009961 (PubMed)
- Malbrain, M. L., Van Regenmortel, N., Saugel, B., De Tavernier, B., Van Gaal, P. J., Joannes-Boyau, O., Monnet, X. Principles of fluid management and stewardship in septic shock: it is time to consider the four D’s and the four phases of fluid therapy. Ann Intensive Care. 2018;8 (1) 66.doi: 10.1186/s13613-018-0402-x (PubMed)
- Prowle, J. R., Echeverri, J. E., Ligabo, E. V., Ronco, C., &Bellomo, R. Fluid balance and acute Kidney injury. Nat Rev Nephrol. 2010;6(2), 107-15.doi: 10.1038/nrneph.2009.213 (PubMed)
- Mercadal, J., Borrat, X., Guerra, G., Elí, R., & Zavala, E. Ecocardiografía funcional en la unidad de reanimación como monitor hemodinámico. MedCrit. 2017;31(2), 84-92. (PDF)





Excelente articulo, donde puedo conseguir informacion para poder realizar la valoracion doppler portal y de venas interlobares renales? Gracias
Gracias por su valoración.
Las referencias del artículo le serán de gran ayuda. En concreto las imágenes del artículo de Beaubien‐Souligny et al.
Un saludo cordial.
Gracias
Hay sin embargo mucho sesgo de referencia, autocita y se basa en una población muy especial: los postcirugía cardíaca, que ya tienen un sustrato previo alterado – por algo van a cirugía – lo que hace difícil la aplicación de sus resultados en pacientes médicos o quirúrgicos con escasa o ninguna patología hemodinámica previa. Ya ni hablemos de la dificultad técnica del propio PoCUS para identificar y medir doppler en vena hepática, porta o intrarrenales. Lo único fácil aquí es medir la cava, y aún en este aspecto hay variaciones interobservador, así como influencia de la valvulopatía, cardiopatía o ventilación mecánica invasiva y no invasiva.
Efectivamente, por eso se detalle que es un camino nuevo por explorar, y que los resultados son bajo una población muy específica de un único centro. Queda detallado en la conclusión de la revisión crítica.
Donde discrepo es en la dificultad técnica, porque no lo es. Solo requiere un profesor inicial que sepa dirigir la exploración, y tras ello se hace reproducible. Las variaciones interobservador se dan siempre en POCUS, y la infuencia en la VMI o VMNI se define por conceptos diferentes como valoracion de colapsabilidad o distensibilidad.
Muchas gracias por la valoración y la aportación.
Un saludo cordial,