Sayalero Rodríguez P (1), Lomillos Prieto N (2), López Serrano MR (3), Riestra Ayora JI (4)
(1) FEA Anestesiología del Hospital Universitario de Getafe, España
(2) FEA Neurociugía del Hospital Puerta de Hierro, España
(3) FEA Neurocirugía, Hospital Universitario de Getafe
(4) FEA Otorrinolaringología, Hospital Universitario de Getafe
Cómo citar este artículo: Sayalero Rodríguez, P., Lomillos Prieto , N., López Serrano, M. de los R., & Riestra Ayora, J. I. (2024). Cirugía de hipófisis. Revista Electrónica AnestesiaR, 16(4). https://doi.org/10.30445/rear.v16i4.1196
Introducción
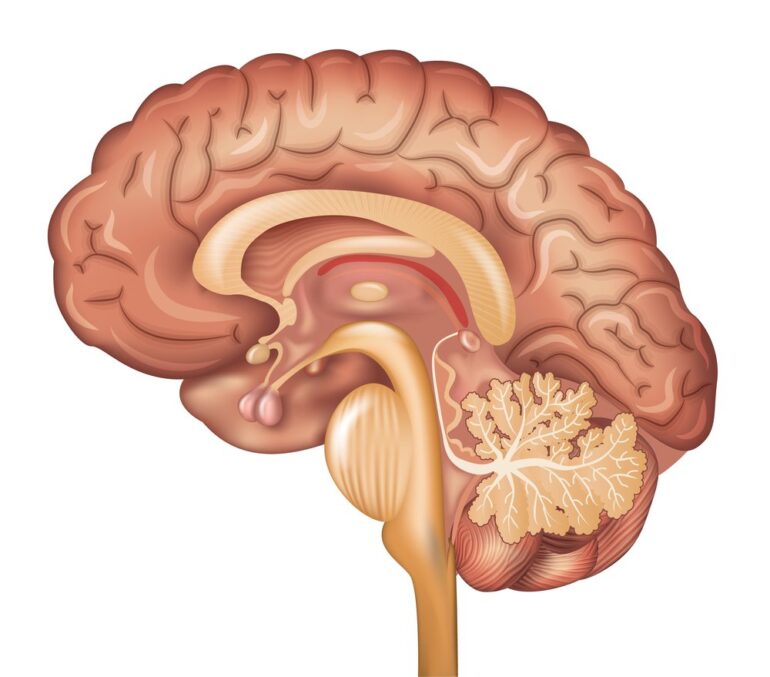
La hipófisis es una glándula única de 1cm de diámetro alojada en la silla turca del hueso Esfenoides, en la línea media de la base del cráneo. Está dividida en Hipófisis posterior o Neurohipófisis; e Hipófisis anterior o Adenohipófisis, que deriva de las células epitelioides de la bolsa de Rathke y donde una proliferación monoclonal puede originar un adenoma hipofisario.
Aunque la cirugía endoscópica transesfenoidal es de elección para tratar, también, otros tipos de lesiones (craneofaringiomas, quistes de la bolsa de Rathke, etc.); nos referiremos en este capítulo únicamente a los adenomas hipofisarios por ser éstos los más frecuentes ya que suponen un 10% de los tumores cerebrales primarios.
La relevancia de estos tumores deriva de dos circunstancias: La primera es que la hipófisis está contenida en un espacio cerrado y pequeño que se encuentra relacionado anatómicamente con el quiasma óptico, arterias carótidas, nervios oculomotores y III ventrículo. La segunda es que el tumor puede originarse a partir de células secretoras de hormonas y dar lugar a síndromes por hipo/hipersecreción hormonal. Proponemos por tanto la siguiente clasificación según la clínica que producen:
- Asintomáticos: hallazgo por prueba de imagen. La indicación quirúrgica la marca el gran tamaño al diagnóstico o crecimiento progresivo del tumor durante la vigilancia radiológica
- Síndromes por Hipersecreción: GH (hormona de crecimiento), ACTH (corticotropina), PRL (prolactina), TSH (hormona tiroestimulante).
- Síndromes por Hiposecreción: panhipopituitarismo o déficit selectivo de ACTH, ADH (hormona antidiurética) u hormona tiroidea.
- Efecto masa, por compresión de estructuras adyacentes a la hipófisis.
- Apoplejía hipofisaria.
Al final del capítulo se desarrollarán, desde el punto de vista anestésico, las consideraciones específicas a tener en cuenta en alguna de las patologías previamente citadas, especialmente en los casos de hiperproducción de hormona de crecimiento o GH (Acromegalia) y Corticotropina o ACTH (Síndrome de Cushing). La consulta de preanestesia irá enfocada a evaluar estas consideraciones.
Todos los pacientes son valorados por neurooftalmología por la alta frecuencia de afectación del quiasma óptico y consecuente defecto en la campimétrico, así como por endocrinología para conocer y corregir en caso necesario las alteraciones hormonales existentes.
Procedimiento
Como prevención de la insuficiencia suprarrenal aguda postoperatoria (en caso de que se lesionara el parénquima glandular quedando hipofuncionante) administramos hidrocortisona i.v. (1mg/kg) antes de entrar en quirófano.
Posición quirúrgica
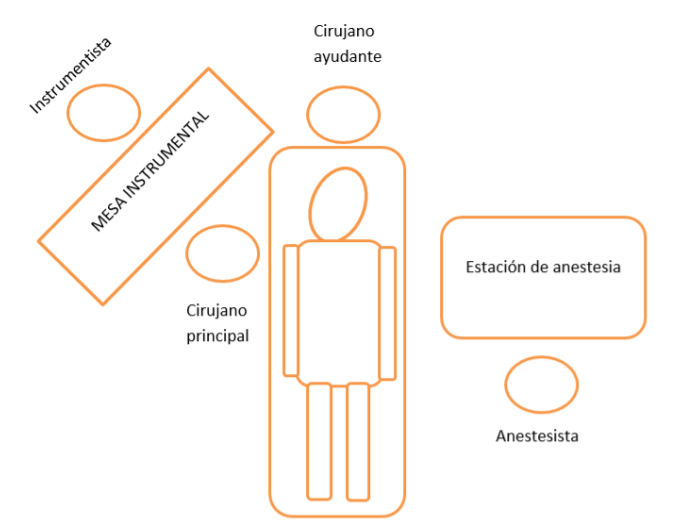
Decúbito supino con cabecero elevado 30-45º, con lateralización cefálica hacia la derecha, ya que los cirujanos se colocarán generalmente a la derecha del paciente.
La fijación de la cabeza con Mayfield puede ser útil, así como sistemas de navegación, según preferencias del cirujano.
Se recomienda canalizar venas y arteria en miembro superior izquierdo, que estará disponible durante la cirugía. La estación de anestesia quedará asimismo a la izquierda del paciente.
Profilaxis antibiótica
Al tratarse de un abordaje transnasal y transesfenoidal se considera una cirugía limpia contaminada (poco habitual en neurocirugía), por lo que usaremos Amoxicilina/Ác. clavulánico 2g/200mg. Postoperatoriamente se suele mantener hasta retirada de taponamiento nasal.
Técnica anestésica
Por lo general se trata de pacientes no ancianos sin grandes comorbilidades por lo que las posibilidades anestésicas son variadas. La elección de TIVA (Anestesia total intravenosa) con propofol como mantenimiento anestésico frente a gases halogenados tiene la ventaja de disminuir el riesgo de náuseas y vómitos en el postoperatorio así como no producir vasodilatación de la mucosa nasal.
Monitorización
En general siempre se monitoriza electrocardiograma, saturación de oxígeno, presión arterial invasiva, diuresis mediante sondaje vesical y BIS. El tubo endotraqueal debe desplazarse hacia la comisura izquierda del paciente para su fijación, ya que los cirujanos acceden desde el lado derecho. Se colocará tras la intubación orotraqueal un taponamiento faríngeo posterior para proteger esófago y vía aérea de la caída de fluidos desde nasofaringe. Es importante asegurar una buena protección ocular. El riesgo de embolia aérea o gran sangrado con necesidad de vasopresores es bajo, por lo que se puede prescindir de la canalización de catéter venoso central, aunque la decisión final se tomará en base a las características del tumor, las comorbilidades del paciente y la experiencia del equipo de quirófano. Pasa asegurar una relajación muscular suficiente se usará si es posible un neuroestimulador durante la cirugía.
La cirugía es llevada a cabo al inicio por un cirujano otorrinolaringólogo (ORL) para facilitar el acceso hasta el seno esfenoidal. Tras la administración de vasoconstrictor tópico (lentinas con Oximetazolina), realizan turbinectomía uni o bilateral de cornete medio ganando así espacio para la entrada y salida del instrumental, y posteriormente etmoidectomía y esfenotomía para exponer el campo de trabajo del neurocirujano. Paralelamente preparan la cobertura del lecho quirúrgico para el final de la intervención, usando habitualmente para este fín el colgajo nasoseptal pediculado o la mucosa del cornete medio. Los neurocirujanos realizan la apertura del suelo de la silla turca (habitualmente adelgazado), durotomía y acceso al contenido intraselar para la resección del tumor. Habitualmente éste es de consistencia más blanda que la propia hipófisis.
Fluidoterapia
Se evitan soluciones hipoosmolares aunque este tipo de cirugías no requiere de especiales consideraciones en cuanto a fluidos intraoperatorios.
Analgesia
No se trata de una cirugía especialmente dolorosa, por lo que los requerimientos analgésicos no son excesivos, pero atención durante la primera fase (ORL) ya que el cirujano se beneficiará de una tensión arterial baja para evitar que el sangrado de la mucosa nasofaríngea dificulte la visibilidad a través del endoscopio rígido. Al final de la cirugía la administración de cloruro mórfico en torno a 2-4 mg suele ser suficiente para una buena calidad analgésica en el postoperatorio inmediato.
Sangrado
Ésta es una cirugía que, en caso de no haber complicaciones, suele sangrar relativamente poco, con un descenso menor de 2 puntos de hemoglobina.
Duración
Variable. En nuestro centro suele ser de 3-5 h según la complejidad del adenoma.
Complicaciones intraoperatorias específicas
- Hipertensión durante la fijación de la cabeza (Mayfield) e infiltración de vasoconstrictor sobre mucosas.
- Embolismo aéreo venoso: raro. Es por ello que tendemos a evitar canalizar catéteres venosos centrales.
- Fuga de líquido cefalorraquídeo por rotura del diafragma selar.
- Complicaciones hemorrágicas: poco frecuentes pero muy importantes.
- Lesión del seno cavernoso (venoso), donde se alojan los pares craneales III, IV, V1, V2 y VI. Suele resolverse con la aplicación de hemostáticos con trombina.
- Lesión de la arteria carótida interna. Es la complicación más grave y afortunadamente es muy poco frecuente (<1%). A nivel endoscópico únicamente se puede intentar controlar la hemorragia realizando un “packing” (comprimir + uso de hemostáticos). Será necesario trasladar al paciente a radiología intervencionista donde se tratará de forma endovascular para evitar el desarrollo de una fístula carótido-cavernosa o un pseudoaneurisma de la porción intracavernosa de la ACI. Anestésicamente trataremos de mantener estabilidad hemodinámica mientras nos enfrentamos a una hemorragia masiva con muy alto riesgo de isquemia cerebral extensa.
Complicaciones en el postoperatorio inmediato
- Riesgo de obstrucción de vía aérea (nariz taponada, necesaria respiración por boca). Está contraindicado el uso de CPAP.
- Epistaxis. Si se sospecha una lesión vascular deberá realizarse una angio-TC para su diagnóstico y un tratamiento endovascular urgente.
- Diplopia/parálisis oculomotora (III, IV, VI pares craneales), habitualmente transitoria por la manipulación quirúrgica.
- Pérdida de agudeza visual. Puede empeorar un déficit establecido previo o producirse una disminución de la agudeza visual de novo por afectación de los nervios y quiasma óptico.
- Fístula de líquido cefalorraquídeo. Ocurre hasta en un 12% de los casos. Pequeños desgarros del diafragma selar incrementan el riesgo de fístula. Se evita usando hemostáticos y sellantes una vez resecado el tumor, para cerrar el defecto en el suelo de la silla turca. En los casos de alto riesgo además se usa grasa libre abdominal son especialmente útiles los colgajos pediculados por su menor tasa de necrosis (aumenta la adherencia al estar vascularizados), así como colocación de un catéter intradural lumbar para drenaje de líquido cefalorraquídeo con el objetivo de disminuir la presión intracraneal.
- Neumoencéfalo, meningitis y hematoma intracraneal. Es necesaria, como en el resto de cirugías del sistema nervioso central, una vigilancia neurológica postoperatoria estrecha.
Las complicaciones endocrinológicas suelen ocurrir más tardíamente. Se dan sobretodo alteraciones en la secreción de ADH: de forma más temprana se vigilará la aparición de Diabetes insípida por falta de ADH/vasopresina, que se tratará con reposición de líquidos y Desmopresina iv. Más tardíamente (tras 1 semana) puede ocurrir una Secreción Inadecuada de ADH.
El panhipopituitarismo por la lesión de la totalidad de la glándula o del tallo hipofisario. Requerirá de tratamiento hormonal sustitutivo definitivo, de por vida.
Consideraciones anestésicas específicas según la clínica al diagnóstico.
La forma de presentación de un adenoma hipofisario más aguda y grave es la apoplejía hipofisaria: espontánea o en el contexto de una hemorragia obstétrica (síndrome de Sheehan), un TCE grave o una crisis drepanocítica. Se produce una lesión isquémica o hemorrágica en el adenoma produciendo una clínica de insuficiencia hormonal aguda que se trata con fluidos, terapia hormonal y puede requerir cirugía descompresiva urgente.
Dentro de la clínica por efecto de masa se suelen asociar los siguientes síntomas y estructuras:
| Sintomatología | Estructura afectada |
| Cefalea (típicamente retroocular) | Compresión del diafragma selar |
| Insuficiencias hormonales (específicas o más frecuentemente: hipopituitarismo) | Compresión de tejido hipofisario sano |
| Hemianopsia bitemporal | Compresión de vías ópticas desde la parte superior y anterior de la hipófisis. |
| Desde diplopia hasta oftalmoplejía | Compresión de pares craneales III, IV, VI. |
| Hidrocefalia | Obstrucción en la salida del tercer ventrículo |
| Rinorrea de líquido cefalorraquídeo | Lesión de clivus o seno esfenoidal |
Clínica por síndromes de hipersecreción: acromegalia y Cushing.
Acromegalia
Producido por adenomas somatotropos, productores de hormona de crecimiento. Son pacientes con probable vía aérea difícil con dificultad para ventilar por macrognatia, macroglosia e hipertrofia de tejidos blandos, con una alta frecuencia de síndrome de apnea/hipopneas del sueño.
Pueden sufrir miopatía proximal y cifoescoliosis.
Cardiológicamente presentan frecuentemente hipertensión arterial, hipertrofia ventricular izquierda; y mayor riesgo arritmogénico, isquemia miocárdica y cardiomiopatías.
Síndrome de Cushing
Producido por adenomas productores de Corticotropina. Precisan de un estrecho control glucémico perioperatorio. Mayor frecuencia de HTA. Disminución de la inmunidad celular. Tendencia a la retención de agua y sodio, con hipopotasemia. Alta probabilidad de Sindrome de Apnea-Hipopnea del sueño (SAHS) y posibilidad de ventilación e intubación difícil por las alteraciones anatómicas. Mayor tendencia a la enfermedad tromboembólica venosa.
Bibliografía
Mark S. Greenberg. Capítulo 3, General Care, págs 31-34. Cap21, Tumor, págs 633-665. Handbook of neurosurgery. Thieme, New York. Séptima edición; 2010. (HTML)
Carl H. Snyderman, Paul A.Gardner.Cap3.Endoscopic endonasal approach to the sella for pituitary adenomas and rathke’s cleft cysts,págs 23-37. Skull Base Surgery. Wolters Kluwer, Philadelphia. Primera Edición; 2015. (PubMed)
B. Szekely, N. Liu, M.Dupuy, S.Gaillard, M.Fischler. Tomo 3. Anestesia-Reanimación y cirugía de la hipófisis, págs. 614-615. Enciclopedia Medico quirúrgica. París; 2011. (HTML)
Brooke Swearingen. Transsphenoidal surgery for pituitary adenomas and other sellar masses. UpToDate 2018. (HTML)
David Rojas, A.Palma, N.Wohllk G. Manejo de los adenomas hipofisarios. Artículo de revisión págs. 140-147. Revista chilena neuro-psiquiátrica 2008. (PDF)
Tobias Else, GD. Hammer, V.R.Lingappa. Capítulo 19, Trastornos del hipotálamo y de la hipófisis, págs. 543-564. Fisiopatología médica: una introducción a la medicina clínica. Primera edición, Mexico; 2007. (HTML)