Alonso Ramos I., Iglesias Guitián R., Grande Fernández A.
FEA Anestesiología, Reanimación y Tratamiento del Dolor. Servicio de Anestesiología y Reanimación, Hospital universitario de Getafe, España.
El adenocarcinoma prostático es el cáncer urológico más común en varones (y el segundo en frecuencia global tras el cáncer de pulmón). Es más frecuente en mayores de 60 años y afroamericanos que en caucásicos. Es un tumor hormonodependiente y, gracias al cribaje con PSA, se suele diagnosticar en fase asintomática. Cuando presentan clínica, esta consiste habitualmente en síntomas urinarios similares a la HBP (síntomas obstructivos, retención de orina).
El tratamiento abarca desde la vigilancia conservadora, pasando por la radioterapia y hormonoterapia, hasta la prostatectomía radical. La resección transuretral está indicada en pacientes con hipertrofia benigna de próstata con volumen glandular de 30-80 ml. La prostatectomía simple (generalmente mediante abordaje retropúbico) es infrecuente y está indicada para la resección de glándulas prostáticas de gran tamaño (HBP). La prostatectomía radical se recomienda normalmente en pacientes con cáncer, enfermedad confinada en la próstata y una esperanza de vida superior a diez años.
Descripción del procedimiento: puntos críticos de la cirugía
La prostatectomía radical comprende la resección de toda la glándula prostática y las vesículas seminales, las venas y nervios circundantes y la porción de uretra dentro de la zona de transición de la próstata. Aunque no siempre es posible, se intenta preservar uno o ambos nervios cavernosos para disminuir la disfunción eréctil y la incontinencia urinaria postoperatoria con el objetivo de mejorar la calidad de vida del paciente. La reanastomosis de los extremos uretrales tras la resección prostática es un paso complicado y puede ser aún más difícil por el derrame de orina del cuello vesical al campo quirúrgico (que entorpece la visión del cirujano), por lo que podemos ayudar con fluidoterapia restrictiva (que también nos ayudará a disminuir el edema).
La cirugía abierta implica mayor traumatismo tisular, riesgo de hemorragia y complicaciones postoperatorias (neumonía, TVP, fuga de la anastomosis por el encamamiento prolongado), por ello es cada vez menos realizada.
El desarrollo de las técnicas mínimamente invasivas (cirugía laparoscópica y robótica) ha reducido las complicaciones y por consiguiente son cada vez más empleadas. Tanto el dolor postoperatorio como el tiempo hasta la ingesta de agua, deambulación, defecación, retirada de los drenajes y el alta hospitalaria son más cortos. Sin embargo, la duración del procedimiento, el riesgo de hemorragia oculta, el neumoperitoneo y el Trendelenburg forzado necesarios para realizar este tipo de abordajes plantean un reto para el anestesiólogo.
En este artículo se describe principalmente el manejo intraoperatorio para la prostatectomía radical mínimamente invasiva (cirugía laparoscópica y robótica), por ser la más frecuentemente realizada.
Posición quirúrgica
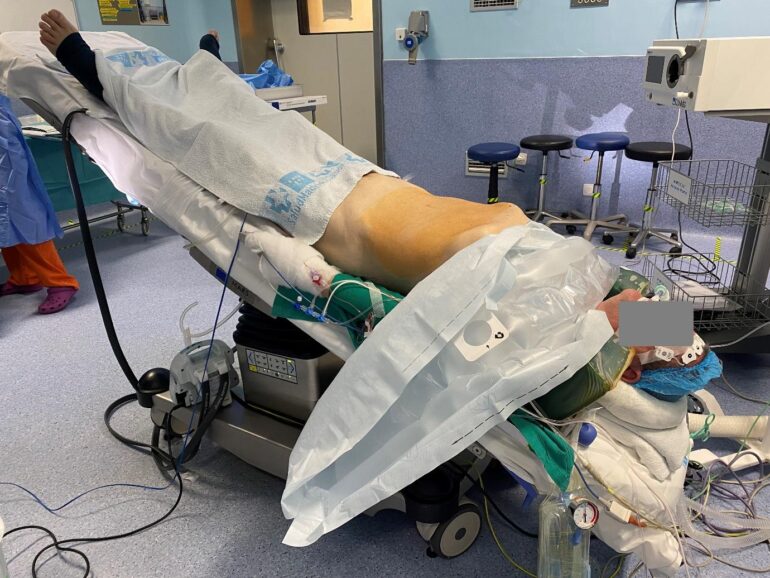
Decúbito supino en Trendelenburg forzado de 30-45º para facilitar el acceso pélvico, por lo que es necesario colocar hombreras acolchadas para proteger de posibles lesiones cervicales y del plexo braquial. Los brazos van pegados al cuerpo, con adecuada protección en los puntos de presión para evitar lesiones nerviosas (nervio radial a la altura del húmero y cubital en el codo). Se deben proteger las manos puesto que, como el paño estéril se pega en la ingle a la altura de las vías, puede ocurrir la salida accidental de las mismas en la retirada de los paños quirúrgicos. (Imagen 1)

Profilaxis antibiótica
La prostatectomía radical se considera una cirugía limpia-contaminada con indicación de profilaxis. En nuestro centro administramos cefuroxima 1500 mg 30-60 minutos antes de la incisión (repitiendo la dosis si la intervención dura más de 4 horas).
En pacientes alérgicos a betalactámicos utilizamos clindamicina 900 mg IV + gentamicina en dosis única IV (calculada según peso del paciente: 4-5 mg/kg).
Opciones de técnica anestésica en la prostatectomía
La posición no es bien tolerada y, eso, junto con la duración de la intervención, hace que sea necesario realizar anestesia general con intubación orotraqueal. El tipo de agente (TIVA o balanceada) depende de la preferencia del anestesista y las características del paciente (debemos tener en cuenta que es necesario evitar las NVPO).
Parece que la TIVA se asocia con mayor tiempo libre de recurrencia y supervivencia en pacientes sometidos a cirugía mayor oncológica, aunque aún no hay evidencia de alta calidad. Es necesario un bloqueo neuromuscular profundo, normalmente con bolos horarios de rocuronio. Además, se recomienda administrar buscapina al finalizar la intervención para el tratamiento del espasmo vesical postoperatorio.
En caso de cirugía robótica, es primordial asegurar la inmovilidad del paciente puesto que, debido a la posición fija de los brazos del robot, movimientos repentinos (como la tos) pueden causar lesiones importantes. Se recomienda, por lo tanto, una perfusión continua de rocuronio. Para ello cargamos tres ampollas de rocuronio de 50 mg (150 mg) en 50 ml de SSF (3 mg/ml) y se administra a una velocidad de 0.1 ml/kg/h para conseguir una dosis de 0.3 mg/kg/h (para 70 kg serían 7 ml/h). Además, se debe tener un plan de emergencia para desenganchar el instrumento, quitar los trócares y desbloquear el robot (para actuar en casos de emergencia de la vía aérea o de infarto cardíaco).
Monitorización
La monitorización es básica estándar, con dos accesos venosos periféricos de buen calibre (14-18 G) con alargaderas (acceso venoso restringido durante la cirugía), presión arterial invasiva (para monitorización hemodinámica y para realizar gasometrías seriadas cada 2-3 h), también monitorización de la profundidad anestésica y del bloqueo neuromuscular (es preciso un bloqueo neuromuscular profundo). Se debe evitar colocar el pulsioxímetro en la oreja, por la posible lectura inexacta debida a la congestión venosa.
Aunque el paciente es sondado al principio de la intervención (estéril por urología), no es posible monitorizar la diuresis puesto que, al realizar la resección prostática, permanece abierta la vía urinaria a la cavidad y se dispersa la orina. También se realiza sondaje rectal por urología. Además, es necesario monitorizar la temperatura y mantener la normotermia con mantas térmicas, calentamiento de los fluidos y otros métodos de calentamiento activo.
La alteración del drenaje linfático puede aumentar las tasas de TVP y embolia pulmonar, por lo que se debe iniciar profilaxis tromboembólica mecánica en quirófano con medias de compresión junto con compresión neumática intermitente.
Fluidoterapia
Se recomienda fluidoterapia restrictiva con cristaloides balanceados y administrar coloides para reponer pérdidas sanguíneas con el objetivo de hemodilución normovolémica. En un paciente adulto, se suelen administrar aproximadamente 1.5-2 L de cristaloides (5 ml/kg/h). Esta fluidoterapia restrictiva puede conllevar depleción relativa de volumen por lo que, tras la anastomosis uretral, administramos un bolo de líquido (últimos 250-500 ml de los cristaloides administrados) junto con un diurético (manitol 0.25 g/kg y/o furosemida 10 mg) para mantener los parámetros hemodinámicos (es frecuente la hipotensión al volver a decúbito supino), apoyar la producción de orina y ayudar a la resolución del edema cerebral.
Analgesia
Se recomienda la analgesia multimodal ahorradora de opioides acompañada de técnicas de anestesia regional. Se pueden utilizar los catéteres incisionales colocados por el cirujano al final de la intervención (analgesia intraoperatoria basada en la vía intravenosa), pero generalmente se prefieren los bloqueos abdominales guiados por ecografía con anestésico local de larga duración antes de la incisión.
En nuestro centro, administramos una perfusión de lidocaína/ketamina/dexmedetomidina acompañada del bloqueo transverso del plano del abdomen y bloqueo de los rectos abdominales con L-bupivacaína 0.25% o ropivacaína 0.2% 40-60 cc. Además, administramos de forma preemptiva paracetamol, ondansetrón, pantoprazol, dexametasona, dexketoprofeno, pantoprazol y sulfato de magnesio 40 mg/kg antes de la incisión quirúrgica, junto con 2-3 mg de cloruro mórfico intravenoso al finalizar la intervención como analgesia preventiva postoperatoria.
En caso de abordaje abierto, se puede completar con analgesia neuroaxial, ya sea raquianestesia con 100 mcg de cloruro mórfico o catéter epidural con un nivel de bloqueo objetivo de T10. En cirugía laparoscópica y robótica no se recomienda la dosificación epidural durante la intervención por la posible difusión cefálica del anestésico local.
Sangrado
La pérdida sanguínea media es de 300-500 ml y, aunque no es frecuente la necesidad de transfusión, se puede producir sangrado brusco durante la intervención difícil de controlar (pudiendo precisar reconversión a cirugía abierta). Se debe optimizar la anemia preoperatoria y reservar sangre para poder administrar hemoderivados.
Duración
La prostatectomía radical laparoscópica se puede realizar en 2-4 h por un cirujano experimentado. La realización de técnicas mínimamente invasivas (cirugía laparoscópica y robótica) pueden prolongar la duración de la intervención hasta 7-10 h (sobre todo durante el periodo de formación).
Complicaciones intraoperatorias específicas
Puede producirse lesión de órganos o lesiones vasculares (sobre todo durante la inserción de los trócares), hipotermia o hemorragia intraoperatoria, que puede precisar la reconversión a cirugía abierta mientras se repone la volemia (coloides 1:1, concentrado de hematíes 0,5:1 con un objetivo transfusional de 7-8 g/dl en pacientes sanos y de 9-10 g/dl en cardiópatas).
El aumento de la presión intratorácica aumenta las presiones venosas prostáticas, incrementando con ello el riesgo de sangrado y de inestabilidad hemodinámica por una embolia gaseosa venosa.
Las alteraciones fisiológicas de la posición en Trendelenburg forzado y el neumoperitoneo son múltiples y suelen requerir ajustes en la ventilación mecánica.
A nivel respiratorio, la compresión diafragmática y pulmonar reduce la capacidad residual funcional, la capacidad vital y la distensibilidad pulmonar, lo que aumenta las presiones pulmonares (para mantener el mismo volumen corriente) y altera la relación ventilación-perfusión (favoreciendo el riesgo de atelectasias e hipoxemia, que se deben prevenir con una adecuada PEEP).
Además, como la insuflación de CO2 exige un mayor volumen-minuto para compensar el CO2 absorbido, pueden aumentar aún más las presiones pulmonares y eso supone un riesgo de barotrauma. Se recomienda una ventilación protectora con presión meseta máxima de 30 mmHg (se permite hasta 35 mmHg en cirugía robótica), a expensas de aumentar la frecuencia respiratoria para mantener un adecuado volumen minuto.
La hipercapnia permisiva es una estrategia ventilatoria posible en casi todos los pacientes, salvo en pacientes con insuficiencia renal (en los que incluso la acidosis respiratoria leve puede suponer una hiperpotasemia importante). Se puede utilizar ventilación controlada tanto por volumen (VCV) como por presión (PCV), aunque la PCV provee mejor complianza y preservación de la relación ventilación-perfusión.
Por otro lado, al instaurar el neumoperitoneo se reduce la distancia de las cuerdas vocales a la carina 1 cm por lo que se debe prestar atención a una posible intubación selectiva en caso de desaturación intraoperatoria.
A nivel hemodinámico, aumentan las resistencias vasculares (sistémicas y pulmonares) y la presión arterial, pudiendo disminuir el gasto cardíaco y aumentar el consumo miocárdico de oxígeno, con riesgo de isquemia y arritmias.
A nivel neurológico, aumenta la presión intraocular (precaución en pacientes con glaucoma), con riesgo de lesión isquémica del nervio óptico y de úlceras corneales; y también aumenta la presión intracraneal, pudiendo comprometer el flujo sanguíneo cerebral (puede ser recomendable la monitorización con Doppler transcraneal u oximetría cerebral) y producir edema cerebral así como disfunción cognitiva postoperatoria.
Por último, se pueden producir úlceras orales y quemaduras conjuntivales debido al reflujo gastroesofágico, por lo que se deben administrar antiácidos, drenar el estómago con mediante sonda orogástrica y proteger adecuadamente los ojos.
Observaciones
Por efecto gravitacional, se puede producir no solo edema cerebral sino también edema facial, faríngeo y/o laríngeo que pueden comprometer la permeabilidad de las vías respiratorias y, por ello, se debe comprobar antes de la extubación con una prueba de fugas (siendo un resultado satisfactorio una fuga mayor del 15%).
Se deben realizar maniobras de reclutamiento pulmonar al finalizar la intervención, comprobar la adecuada reversión del bloqueo neuromuscular y realizar una extubación cuidadosa.
Se recomienda mantener al paciente en supino (o ligero anti-Trendelenburg) durante 10-15 minutos antes de despertar al paciente para disminuir el edema laríngeo y el edema cerebral, y reducir así el riesgo de agitación y confusión.
Bibliografía
- Stafford-Smith M. Aparato urinario y anestesia para cirugía urológica. En: Paul G. Barash, editor. Clinical Anesthesia. Philadelphia. 2018. P. 1400-1440.
- Patel J. Anaesthesia for Major Urological Surgery. Anesthesiology Clin. 2022; 40: 175-197. (PubMed)
- Lagarda-Cuevas J. Consideraciones anestésicas en pacientes sometidos a cirugía robótica asistida para prostatectomía radical: reporte de un caso. Revista mexicana de Anestesiología. 2019; 42(4):302-306.
- Ke Chen MD. Effects of pneumoperitoneum and steep Trendelenburg position on cerebral hemodynamics during robotic-assisted laparoscopic radical prostatectomy. Medicine. 2019; 98:21. (PubMed)