Figueiredo González O
FEA Anestesiología y Reanimación
Complexo Hospitalario Universitario de Ourense
Introducción
La hipotermia perioperatoria no intencionada (HPNI) se define como la temperatura corporal central <36ºC antes, durante y/o después de la cirugía con una incidencia entre 6-90% (1).
El riesgo aumenta con la edad ya que los ancianos no pueden aumentar su metabolismo basal en la misma medida que los jóvenes y su mecanismo de vasoconstricción se activa con un umbral más bajo y es de menor intensidad. Y el riesgo disminuye con el sobrepeso ya que los obesos presentan una mayor vasodilatación periférica que el resto de pacientes.
La Sociedad Americana de Anestesiólogos (ASA) se refiere a la monitorización de la temperatura como: «La temperatura debe ser periódicamente medida durante la recuperación anestésica». En Reino Unido, el Instituto Nacional para la Salud y la Excelencia Clínica (NICE) publicó en 2008 unas guías para el manejo de la HPNI (2).
La alteración de la termorregulación producida por la anestesia y la pérdida de calor durante la cirugía por la exposición a un ambiente con bajas temperaturas, determinan hipotermia en un gran porcentaje de pacientes. Según los estudios disponibles, durante los primeros 60 minutos de anestesia, los pacientes pueden perder hasta 1,6ºC por la redistribución del calor del compartimento central al periférico. Alrededor del 50% de los pacientes llegan al quirófano con temperatura <36ºC y hasta el 33% de 35ºC.
El aumento de la temperatura intraoperatoria, el calentamiento de fluidos intravenosos y el calentamiento cutáneo activo son algunas de las medidas descritas para asegurar la normotermia aunque el mejor método es la prevención.
La HPNI no sólo es incómoda, sino que además provoca efectos secundarios que afectan el pronóstico del paciente como:
1) Infección de la herida quirúrgica ya que induce vasoconstricción periférica, con la consiguiente disminución de la presión parcial de oxígeno y deterioro de la función inmunitaria como demostraron los estudios de Hopf (3). Kurz et al. (4) y más tarde Melling (5) demostraron que una disminución de la temperatura de 1,9°C aumentaba la incidencia de infección de 6% a 19% en todo tipo de cirugía.
2) Alteraciones cardiovasculares pues se ha constatado que en pacientes de alto riesgo, una temperatura mantenida <35ºC triplica la incidencia de isquemia miocárdica en el postoperatorio inmediato y que la normotermia puede reducir un 55% el riesgo de aparición de complicaciones cardíacas. Frank (6) puso de manifiesto una mayor incidencia de eventos cardíacos en pacientes coronarios o con alto riesgo cardiovascular a 35,4+/-0,1°C.
3) Coagulopatía debida a la alteración de la función plaquetaria, de la cascada de la coagulación y de la fibrinolisis. Shmied (7) y Winkler et al. (8) revelaron que la hipotermia aumentaba el sangrado quirúrgico y la transfusión un 16% y un 22% respectivamente. Wong (9) concluyó que el calentamiento activo iniciado en el preoperatorio y mantenido hasta el postoperatorio inmediato disminuía significativamente el sangrado. Cavallini (10) observó una disminución significativa en el tiempo de sangría postoperatorio en pacientes hipotérmicos sometidos a cirugía plástica.
4) Efecto prolongado de los fármacos ya que las enzimas encargadas de su metabolización son altamente sensibles a los cambios de temperatura. La hipotermia prolonga la acción del atracurio, vecuronio y rocuronio y disminuye la amplitud del primer twich y el TOF-ratio un 20% por cada ºC que cae la temperatura en el aductor del pulgar. Se prolonga un 20% el tiempo de inicio de acción de la neostigmina. Se reduce un 5% la CAM de los anestésicos volátiles por cada ºC de descenso de la temperatura. La concentración plasmática de propofol aumenta un 30% cuando la temperatura desciende a 34°C. El fentanilo aumenta un 5% en su concentración plasmática durante la fase de equilibrio por cada ºC de descenso de la temperatura.
5) Temblor aunque su etiología sigue sin aclararse por completo.
6) Recuperación postanestésica prolongada: Lenhardt (11) en un estudio aleatorizado en el que incluyó a 150 pacientes asignados a mantener normotermia o hipotermia leve se demostró que la hipotermia retrasaba el alta de la Unidad de Recuperación Postanestésica entre 40-120 min.
El objetivo de nuestro estudio fue comparar la tasa de HPNI en cirugía abierta de colon y recto comparando el colchón térmico eléctrico, del que disponemos en nuestro centro, con la manta de aire forzado bajo paciente.
Materiales y métodos
Estudio prospectivo realizado en el Complexo Hospitalario de Ourense entre Marzo y Junio de 2023 donde se incluyeron todos los pacientes mayores de 50 años sometidos a cirugía abierta de colon y recto.
Se realizaron mediciones intraoperatorias de la temperatura central y se anotaron en una ficha de recogida de datos para calcular la tasa de hipotermia considerándose únicamente la temperatura más baja registrada en toda la cirugía.
Nuestro objetivo primario fue comparar la tasa de HPNI en los pacientes que fueron calentados con el colchón térmico eléctrico y la manta de aire forzado. Para ello se monitorizó la temperatura mínima y se definió como hipotermia cuando se observó una temperatura por debajo de 36ºC.
Los objetivos secundarios fueron evaluar diferencias según la edad de los pacientes (50-69 o ≥70 años) y duración de la cirugía (inferior o superior a 2 horas).
Aleatoriamente, se distribuyó a los pacientes en 2 grupos, en el primero se monitorizó la temperatura usando el colchón térmico eléctrico y el sistema de calentamiento de fluidos de infusión y en el segundo se sustituyó el colchón por la manta de aire forzado bajo paciente.
A todos los pacientes se les midió la temperatura con el sistema SpotOn.
El estudio se realizó de acuerdo con los principios de la declaración de Helsinki, y los datos recogidos han sido tratados conforme la Ley Orgánica 15/99 del 13 de diciembre de protección de datos de carácter personal. Contamos además con la aprobación por parte del Comité ético de nuestro hospital y todos los pacientes firmaron el consentimiento informado por escrito.
Resultados
En total 29 pacientes fueron incluidos en el estudio, 16 de ellos fueron calentados con el colchón térmico eléctrico y el sistema de calentamiento de fluidos de infusión y en los 13 restantes se sustituyó el colchón térmico por la manta de aire forzado bajo paciente.
En el grupo del colchón térmico se observó una tasa de hipotermia del 62,5% para los dos grupos de edad y las diferentes duraciones de anestesia (Gráfica 1)
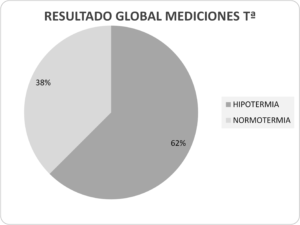
En cirugías de >2 h sufrieron hipotermia el 100% de los pacientes ≥70 años y el 50% de 50-69 años.
Al final de las cirugías de >2 h estaban hipotérmicos el 75% de los pacientes ≥70 años y el 50% de 50-69 años lo que supone el 44% del total de intervenciones monitorizadas.
En el grupo de la manta de aire forzado bajo paciente se observó una tasa de hipotermia del 53,8% para los dos grupos de edad y las diferentes duraciones de anestesia (Gráfica 2).
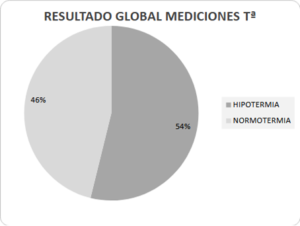
En cirugías de >2 h sufrieron hipotermia el 61,5% de los pacientes ≥70 años y el 30,8% de 50-69 años.
Al final de las cirugías de >2 h estaban hipotérmicos el 12,5% de los pacientes ≥70 años y ninguno de 50-69 años lo que supone el 7,7% del total de intervenciones monitorizadas.
Se obtuvo una reducción de la HPNI del 14% al usar la manta de aire forzado bajo paciente, siendo esta reducción mayor en los pacientes entre 50-59 años intervenidos de cirugías de más de 2 horas.
Discusión
La mayoría de los pacientes sometidos a anestesia general desarrollan hipotermia de modo que su temperatura desciende de 1 a 3ºC, dependiendo del tipo de anestesia, la exposición quirúrgica y la temperatura ambiente. La hipotermia intraoperatoria se desarrolla siguiendo un patrón característico: durante la primera hora, la temperatura disminuye entre 1-1,5ºC por la vasodilatación inducida por la anestesia general, la pérdida de calor producida por las bajas temperaturas dentro del quirófano, las grandes incisiones quirúrgicas y los líquidos intravenosos fríos. Posteriormente sigue disminuyendo de 2 a 3 h debido al disbalance entre la producción metabólica de calor y la pérdida de éste hacia el ambiente, hasta entrar en una fase de meseta, consecuencia del equilibrio entre las pérdidas y la producción metabólica de calor (12).
La monitorización de la temperatura en el intraoperatorio comenzó a instaurarse a principios de los años 60 aunque actualmente, no se monitoriza rigurosamente a pesar de conocerse que mejora el resultado final del paciente quirúrgico. Debe ser monitorizada en procedimientos de >30 min bajo anestesia general y en cirugías de >60 min independientemente de la técnica anestésica.
La mayoría de los dispositivos disponibles, miden la temperatura de forma precisa pero invasiva, por lo que su uso se limita al quirófano y en algunos casos a las unidades de cuidados intensivos. El sistema SpotOn que se coloca en el lateral de la frente es un método no invasivo pero preciso que puede usarse durante todo el proceso perioperatorio. En un estudio se comparó con la sonda esofágica en 69 pacientes sometidos a anestesia general entre 40-220 min calentados con el sistema de aire forzado concluyéndose que las mediciones con el sistema SpotOn se correlacionaban muy bien con las mediciones de la sonda esofágica (13). Se comparó igualmente con el termómetro sublingual y la sonda nasofaríngea concluyendo que proporcionaba medidas de temperatura similares a las proporcionadas por los otros dispositivos.
Los 2 mecanismos más importantes que causan pérdida de calor en el quirófano en orden de importancia son la radiación y la convección. La radiación produce el 60% de las pérdidas, y por ello debe mantenerse una humedad relativa >45% con una temperatura entre 21-24°C. Las guías del NICE dicen en relación a este punto: «la temperatura del quirófano debe ser al menos de 21°C mientras el paciente está expuesto».
El mejor método para asegurar la normotermia es la prevención minimizando las pérdidas de calor por redistribución en la inducción, por radiación y convección desde la piel y por evaporación desde la superficie quirúrgica en exposición y disminuyendo el enfriamiento por administración de fluidos intravenosos. En el intraoperatorio el paciente está vasodilatado y la transferencia de calor es más fácil que cuando se realiza con el paciente en vasoconstricción, que es lo que ocurre en el postoperatorio (14).
El aislamiento pasivo como método único raramente es suficiente para mantener la normotermia en pacientes sometidos a grandes cirugías requiriéndose métodos de calentamiento activo.
Los dispositivos de calentamiento de fluidos evitan el enfriamiento durante la infusión de líquidos fríos ya que se ha estimado que la temperatura desciende 0,25°C por cada litro de coloide o cristaloide administrado a temperatura ambiente y de derivado sanguíneo refrigerado, pero nunca sustituirán al calentamiento activo y no aportarán nada si el ritmo de infusión es lento. Hasankhani (15) demostró una menor incidencia de efectos cardiovasculares y de temblor postoperatorio en pacientes en los cuales se aplicó este método de calentamiento.
El colchón térmico eléctrico produce calentamiento en una lámina conductora de material suave que libera calor uniformemente por toda su superficie. Su tecnología de polímero de carbono flexible posibilita la integración bajo la lámina calentadora del colchón de una capa para el alivio de la presión del paciente. Esto asegura que no exista atenuación de la transferencia térmica dando no obstante al conjunto propiedades antiescaras.
Las mantas de aire forzado reducen la pérdida de calor mediante sustitución del aire frío del quirófano que recubre al paciente por una capa de aire caliente reduciendo así la pérdida por radiación y al crear esa capa de aire más caliente que la piel, aumentan la ganancia de calor por convección. Al estar colocadas bajo el paciente, pueden iniciar el precalentamiento en el mismo momento que éste llega al quirófano, minimizando la caída de temperatura por redistribución. Son muy efectivas porque se alcanza mucha más superficie corporal que con ninguna otra y porque permiten utilizar un método de calentamiento en cirugías donde es imposible poner nada por encima del paciente.
El precalentamiento es una recomendación actual que atenúa considerablemente la disminución inicial de la temperatura al impedir la pérdida de calor por redistribución. Debe realizarse entre 30-60 min antes de la inducción. Cuando no se precalienta, las técnicas de calentamiento intraoperatorio fallan en eliminar la caída inicial de la temperatura.
Nosotros no pudimos precalentar por falta de unidades de calentamiento en el área donde esperan los pacientes antes de pasar al quirófano.
Existen múltiples estudios comparando ambos métodos de calentamiento como el de Santos et al. en el que no se encontraron diferencias significativas en cirugía gastrodigestiva (16) igual que en el de Fanelli et al. después del reemplazo total de cadera electivo (17).
En nuestro estudio, se confirmó como esperábamos una reducción de la HPNI al usar la manta de aire forzado bajo paciente en las cirugías de más de 2 horas en los pacientes entre 50-59 años y no en los ≥70 años como preveíamos.
Conclusión
Podemos concluir que la HPNI se redujo con la utilización de las mantas de aire forzado bajo paciente pero aún así su elevada frecuencia hace necesario prevenirla especialmente en cirugías largas y pacientes añosos. Una limitación del estudio fue el bajo número de pacientes incluido debido a la escasez de material disponible.
Bibliografía
- Harper CM, Andrzejowski JC, Alexander R. Nice and warm. Br J Anaesth. 2008;101:293-5. (PubMed)
- National Institute for Health and Clinical Evidence. Clinical practice guidelines: The management of inadvertent perioperative hypothermia in adults. Disponible en: www.nice.org.uk/CG65 [consultado 9 Sep 2010]. (HTML)
- Hopf HV, Hunt TK, West JM. Wound tissue oxygen tension predicts the risk of wound infection in surgical patients. Arch Surg. 1997;132(9):997-1004. (PubMed)
- Kurz A, Sessler DI, Lenhardt R. Study of Wound Infections and Temperature Group: Perioperative normothermia to reduce the incidence of surgical-wound infections and shorten hospitalization. N Engl J Med. 1996;334(19):1209-15. (PubMed)
- Melling AC, Ali B, Scott EM, Leaper DJ. Effects of preoperative warming on the incidence of wound infection after clean surgery: a randomised controlled trial. Lancet. 2001;358(4):876-80. (PubMed)
- Frank SM, Beattie C, Christopherson R, Norris EJ, Perler BA, Williams GM, et al. Unintentional hypothermia is associated with postoperative myocardial ischemia. The Perioperative Ischemia Randomized Anesthesia Trial Study Group. Anesthesiology. 1993;78(3):468-76. (PubMed)
- Schmied H, Schiferer A, Sessler DI, Meznik C. The effects of red-cell scavenging, hemodilution, and active warming on allogeneic blood requirement in patients undergoing hip or knee arthroplasty. Anesth Analg. 1998;86(2):387-91. (PubMed)
- Rajagopalan S, Mascha E, Na J, Sessler DI. The effects of mild perioperative hypothermia on blood loss and transfusion requirement. Anesthesiology. 2008;108(1):71-7. (PubMed)
- Wong PF, Kumar S, Bohra A, Whetter D, Leaper DJ. Randomized clinical trial of perioperative systemic warming in major elective abdominal surgery. Br J Surg. 2007;94(4):421-6. (PubMed)
- Cavallini M, Baruffaldi, Preis FW, Casati A. Effects of mild hypothermia on blood coagulation in patients undergoing elective plastic surgery. Plast Reconstr Surg. 2005;116(1):316-21. (PubMed)
- Lenhardt R, Marker E, Goll V, Tschernich H, Kurz A, Sessler DI et al. Mild intraoperative hypothermia prolongs postoperative recovery. Anesthesiology. 1997;87(6):1318-23. (PubMed)
- Sessler DI. Perioperative heat balance. Anesthesiology. 2000;92(2):578-96. (PubMed)
- Clinical Evaluation of Spot-OnR, a New Non-Invasive and Continuous Temperature Monitoring System. Juan M. Zaballos, M.D., Ph.D., Unai Salinas, M.D. Policlínica Guipuzcoa, San Sebastian, Spain. (PDF)
- Wong PF, Kumar S, Leaper DJ. Systemic warming as an adjunct to resuscitation in peritonitis: a pilot, randomized controlled trial. Surg Infect (Larchmt). 2007;8(3):387-95. (PubMed)
- Hasankhani H, Mohammadi E, Moazzami F, Mokhtari M, Naghgizadh MM. The effects of intravenous fluids temperature on perioperative hemodynamic situation, post-operative shivering, and recovery in orthopaedic surgery. Can Oper Room Nurs J. 2007;25(1):20-4,6-7. (PubMed)
- Santos RMSF, Boin IFSF, Caruy CAA, Cintra EA, Torres NA, Duarte HN. Randomized clinical study comparing active heating methods for prevention of intraoperative hypothermia in gastroenterology. Rev. Latino-Am. Enfermagem. 2019;27:e3103. DOI: http://dx.doi. org/10.1590/1518-8345.2589.3103. (PubMed)
- Fanelli A, Danelli G, Ghisi D, Ortu A, Moschini E, Fanelli G. The efficacy of a resistive heating under-patient blanket versus a forced-air warming system: a randomized controlled trial. Rev. Anesth Analg. 2009 Jan;108(1):199-201. DOI: 10.1213/ane.0b013e31818e6199. PMID: 19095850 Clinical Trial. (PubMed)