Blanco Becerra C.E; Pérez Prieto, M.; Robledo Rodríguez, M.J.
Servicio de Anestesiología y reanimación Hospital Gutiérrez Ortega. Valdepeñas. Ciudad Real.
La glucogenosis tipo V, también conocida como enfermedad de McArdle, es ocasionada por una deficiencia en la enzima glucógeno fosforilasa muscular, cuya función es iniciar la ruptura del glucógeno mediante la fosforilación de los residuos α1-4glucosil, obteniendo como producto de dicha reacción la obtención de glucosa 1-fosfato.
La esclerosis múltiple es una patología de etiología indeterminada en la que están implicadas distintas hipótesis etiológicas causando afectaciones en el sistema nervioso central que suele ser progresiva y aleatoria.
Se presenta el caso de una primigesta de 35 años, con ambos diagnósticos. Patologías de carácter autoinmune que suponen un reto para el anestesista y el equipo médico, debido a su baja prevalencia y a la falta de estudios o experiencias en el ámbito quirúrgico que nos permitan identificar las posibles consecuencias derivadas de intervenciones anestésicas y obstétricas.
Glucogenosis tipo V o enfermedad de McArdle
En primer lugar se comenzará describiendo la glucogenosis tipo V, también conocida como enfermedad de McArdle, que fue descrita por primera vez a principios de la década de los cincuenta por Brian McArdle, con identificación enzimática a finales de la misma1. La enzima responsable es denominada glucógeno fosforilasa muscular y su función es la de iniciar la ruptura del glucógeno mediante la fosforilación de los residuos α1-4glucosil, obteniendo como producto de dicha reacción la obtención de glucosa 1-fosfato.1
Esta glucógeno fosforilasa muscular se divide, a su vez, en dos tipos de fosforilasas, que interactúan entre sí en el proceso de fosforilación/desfosforilación, siendo activadas por distintos estímulos a su vez, lo que es posible gracias a una diferencia fundamental entre ambas. Por una parte, se encuentra la fosforilasa tipo B que no posee un grupo fosforilo y eso le permite interactuar con moléculas de ATP, glucosa 6-fosfato y glucosa, siendo estas moléculas inhibitorias de la misma, mientras que el AMP en niveles elevados actúa como activador de la fosforilasa, llegando a cambiar su conformación a forma activa hasta en un 80%1.
Este mecanismo de regulación representa un mantenimiento del equilibrio de forma estrecha e inmediata a nivel celular; sin embargo, dicho mecanismo es a su vez influenciado por un mecanismo neural que obedece al proceso fisiológico del estrés. La respuesta del organismo ante la adrenalina generada en la médula adrenal determina, como es bien conocido, la activación de adenilato ciclasa con el consecuente aumento de AMPc. Es importante resaltar que ambas enzimas tienen una importancia significativa en el mecanismo celular de activación de la degradación del glucógeno a nivel muscular1.
La consecuencia de un déficit de la glucógeno fosforilasa muscular se puede comprender de una manera más sencilla si se recuerdan los principios básicos del metabolismo celular. El músculo esquelético puede, por un lado, almacenar glucógeno (que será degradado a glucosa cuando se necesite), obteniendo a su vez —cuando se activa el metabolismo anaeróbico— el lactato como producto final.
Por lo tanto, ante un déficit de la enzima encargada, podemos encontrar por una parte una curva plana de lactato venoso durante el ejercicio intenso, isquemia y acúmulo de glucógeno a nivel muscular, hallazgos que se manifiestan de manera clínica en síntomas que pueden ir desde un síndrome doloroso agudo a incluso debilidad muscular progresiva con intolerancia al ejercicio y contracturas musculares, observándose en aproximadamente la mitad de los casos rabdomiólisis y mioglobinuria2.
En cuanto al diagnostico, ante la sospecha clínica de la enfermedad (cuya prevalencia en España es de 1/400.000 individuos y una incidencias de 1/50.000 nacimientos3 ) se hace necesaria la realización de una biopsia muscular para confirmarlo y así obtener el ARNm para la identificación del gen PYGM en el brazo corto del cromosoma 11 (11q13)1.
Esclerosis múltiple
En otro orden de ideas, la esclerosis múltiple (EM) es una patología de etiología indeterminada en la que están implicadas distintas hipótesis etiológicas como son factores ambientales, infecciones por virus o factores genéticos, de gran relevancia, no solo durante el embarazo y el parto, sino también a la hora de plantearnos una intervención anestésica, ya sea una técnica regional o general4.
La EM en España afecta a un total de 47000 personas, según la Sociedad Española de Neurología, quienes afirman que, en los últimos 20 años, los casos de EM se han multiplicado por dos y que cada año se diagnostican aproximadamente 1800 nuevos casos de esta enfermedad4.
La gran relevancia que adquiere en el ámbito anestésico es debida a que compromete el sistema nervioso central (SNC) y, como bien se sabe, casi todos (por no decir todos) los fármacos utilizados en anestesia, de forma directa o indirecta están relacionados con este.
Esto hace dudar tanto a pacientes como a sanitarios respecto a cuáles pueden ser las consecuencias de un acto anestésico, tanto desde la posibilidad de potenciar brotes como de empeorar la condición del paciente6. La aparición de afectaciones en el SNC suele ser progresiva y aleatoria, causando áreas de desmielinización de los tractos neuronales corticoespinales y respetando los nervios periféricos. La remisión y exacerbación de los brotes es impredecible5.
La clínica de esta enfermedad es muy variada: lo más frecuentes son las paresias y parestesias de una o más extremidades, de manera unilateral sobre todo, pero también ataxia o problemas de visión (como perdida parcial o total de la visión de un ojo, diplopía transitoria o prolongada o visión borrosa). Otros síntomas pueden ser la disartria o bradilalia, fatiga, mareos, disfunción vesical o disfunción sexual5.
Es característico encontrar estos síntomas en un rango de edades de 20 a 40 años de edad y con una prevalencia mayor en mujeres que en hombres.
En la actualidad no existe un tratamiento específico para enfermedad, sin embargo, distintos fármacos han demostrado retrasar el curso natural de la misma4.
Caso clínico de embarazada con glucogenosis tipo V y esclerosis múltiple
Paciente mujer, primigesta, de 35 años de edad, con diagnóstico de glucogenosis tipo V, eritema multiforme y esclerosis múltiple. Es remitida por el departamento de Ginecología y Obstetricia para valoración preanestésica y manejo conjunto en resolución del embarazo.
La paciente refiere diagnostico de glucogenosis tipo V a los 31 años de edad, confirmado con biopsia de muscular, sin antecedentes familiares de la misma. La sintomatología se caracteriza por sensación de cansancio moderado durante el ejercicio, con calambres en miembros inferiores en ocasiones de ejercicio más intenso, que mejoran progresivamente con pausas intermitentes.
Diagnóstico de EM a los 26 años de edad, en seguimiento por la Unidad de Neurología de este hospital. Último brote hace 9 años. La sintomatología (remitida actualmente) de inicio consistía en alteración sensitiva en hemilengua derecha, y posterior en región malar derecha, y fosfenos ocasionales que desaparecieron al cabo de mes y medio.
No dolor no alteración de la motilidad. No alteración sensitiva en extremidades.
Actualmente se ha desestimado el tratamiento, a pesar de valorar distintas opciones, debido a incompatibilidad con patología psoriásica y por riesgo de leucoencefalopatia multifocal progresiva y al no estar justificado debido a presencia de anticuerpos de virus de John Cunningham en paciente con buena situación clínica.
En 2010, diagnóstico de psoriasis sin artritis, de la que posteriormente desarrolló episodios recurrentes de dolores articulares con pico en 2017 y 2020.
El desarrollo del embarazo se dio con total normalidad, sin brotes de EM y sin aumento de la fatiga característica de la GV de la paciente, que refiere además que suele tolerar bien con pequeñas pausas y buena hidratación.
Al ser valorada por el servicio de Anestesiología, se estudia el caso y se determina que no existe ninguna contraindicación anestésica para la resolución del parto vía vaginal ni por cesárea, se clasifica como ASA II, y se contacta con la organización sin fines de lucro para la glucogenosis tipo V (que brindan información adicional3 tanto a sanitarios como a afectados por dicha enfermedad).
Se le indican a la paciente los riesgos comunes y específicos asociados a la analgesia epidural, espinal y anestesia general, se obtiene el consentimiento informado, se le entrega además una hoja de recomendaciones relativas a la enfermedad para ser entregada a los sanitarios en servicio el día que se produzca el inicio del trabajo de parto y se deja una copia de dicha información para que todo el grupo de anestesistas estuvieran al tanto de las recomendaciones planteadas.
Según la historia clínica, la paciente consulta a las 10 AM por contracciones, reportándose 2 cm de dilatación y mecánica uterina efectiva. Es evaluada por la matrona y especialista de guardia e inmediatamente, a su ingreso, se canaliza una vía venosa periférica 18 G braquial izquierda y se comienza fluidoterapia a base de suero glucosado al 5% de mantenimiento 500 ml cada 6 horas.
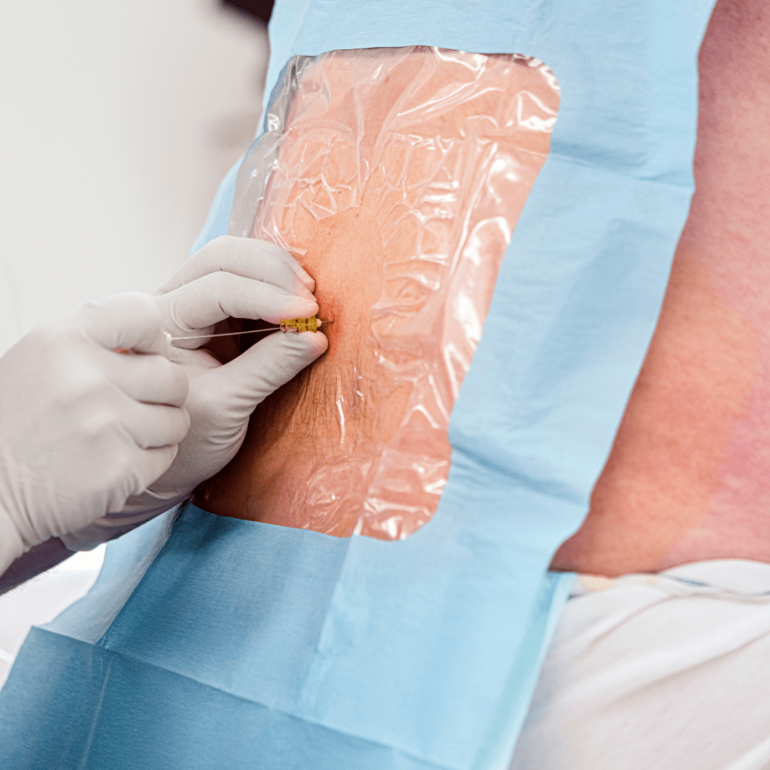
Se le permite a la paciente la ingesta de líquidos claros y, según el partograma, el trabajo de parto se inicia a las 14:45. Aproximadamente a mitad del trabajo de parto, se solicitan niveles de CPK reportados en 171, menores que los reflejados en consulta preanestésica (267). Alcanzados 4 cm de dilatación y transcurrida 1 hora en la sala de partos, la paciente solicita analgesia epidural, que es administrada por la anestesista de guardia previa revaloración anestésica de la paciente (reportando según HC una técnica epidural en L3 de un solo intento con dosis de prueba de 3 ml de bupivacaina 0.25 % con adrenalina sin cambios y fijando el catéter a 12 cm en piel sin complicaciones).
Se administra un bolo inicial de ropivacaína 0.2 % de 7 ml + fentanilo 50 mcg (mezcla total de 8 ml) vía epidural alcanzando un nivel satisfactorio con EVA 0/10 pts a los 10 minutos y se mantiene una perfusión continua de ropivacaína 0.2% + fentanilo 1 mcg/ml, a razón de 6- 8 ml/hr según requerimientos de la paciente.
Aproximadamente a las 4 horas, la paciente se encuentra en dilatación completa llevando el trabajo de parto entre dilatación y expulsión un total de 6 horas. La matrona comenta que, durante el esfuerzo, la paciente continua con la infusión continua de glucosado al 5 % que, hasta el momento del parto, se cuantifico en 500 ml en total.
Casi al final de la expulsión del bebé, la paciente refiere sensación de cansancio y parestesias en miembros inferiores de manera transitoria y resolución espontánea. A las 21:44 horas, según el partograma, se produce el nacimiento necesitando episiotomía y ventosa tipo KiwiR.
Se reporta posterior alumbramiento espontáneo a los 6 minutos, se retira catéter epidural integro, sin ninguna complicación reseñada (Es protocolo del servicio retirar el catéter posterior al parto vaginal si no se presentan complicaciones. En caso de cesárea con epidural se mantiene el catéter en planta).
Al día siguiente, la paciente es evaluada nuevamente por el servicio de Ginecología y Obstetricia. Al momento del alta a las 48 horas, en analítica de rutina, solo reportaba anemia moderada con cifras de 9.1 gr/dl de Hemoglobina con terapia sustitutiva (La CPK solicitada no fue procesada).
Es también valorada por el servicio de Anestesiología y se describe en buenas condiciones generales, sin déficit motor ni sensitivo, un Bromage de 0 puntos y un Hollmen de 1 punto. Asimismo, el servicio de Pediatría refiere en la atención inmediata del recién nacido un Apgar de 09 pts.
No se presentan incidencias, la analítica de rutina solo sin incidencias. La paciente ha acudido posteriormente a su revisión por neurología a los seis meses y reportan que no ha habido incidencias posteriores.
Discusión del caso clínico
Después de una revisión exhaustiva de la literatura disponible, se evidencia que hay poca información relevante y, en particular, ninguna en relación a una paciente con ambas patologías en período de gestación. Lo que, sin duda alguna, hizo saltar las alarmas dentro del equipo quirúrgico, llevando a un manejo integral y multidisciplinar para el abordaje de la paciente.
La falta de estudios o experiencias en el ámbito quirúrgico que nos permitan identificar las posibles consecuencias derivadas de intervenciones como la atención del parto o la operación cesárea, entre otras, eran respuestas importantes a encontrar de cara no solo a resolver la situación sino a informar a la paciente e incluirla en la toma de decisiones.
Dentro de las fuentes consultadas, estaba la asociación de pacientes con glucogenosis, quienes además de brindar apoyo a las personas con dicha afectación cuentan con importante material informativo, de investigación y apoyo tanto para pacientes como para profesionales sanitarios.
Como se describió anteriormente, la paciente se encontraba en un buen estado de salud, con una adaptación fisiológica del embarazo que no modificó la condición basal de ninguna de las dos patologías. Lo que coincide con el reporte del caso clínico de Canedo y cols2.
Sin embargo, la gran incógnita que se planteaba era, si el esfuerzo durante la fase final del trabajo de parto y el agotamiento del inicio del mismo, hubieran podido desencadenar un empeoramiento de la clínica, incluso un posible fallo renal agudo como consecuencia de la mioglobinuria por aumento del consumo de energía, así como también la posible necesidad de una cesárea urgente, derivada de lo anterior o de las complicaciones propias del parto.
Como tal, la técnica anestésica según el tipo de urgencia obstétrica puede plantear distintos escenarios, desde una anestesia conductiva o la realización de una anestesia general en procedimientos urgentes, en cuyo caso, toma importancia el factor de controversia respecto a la EM retratado en el estudio realizado por Stevens et al. respecto a la utilización de relajantes musculares, así como la importancia de evitar el uso de la succinilcolina en la GV debido a que las fasciculaciones pueden generar calambres, rabdomiolisis e insuficiencia renal2que estando implícita una IRA con desequilibrio iónico empeorarían el cuadro clínico.
Asimismo los agentes inhalatorios deben evitarse en este tipo de miopatías debido a su capacidad depresora neuromuscular y, en particular, en el embarazo dada la disminución del tono de la actividad uterina así como la respuesta a uterotónicos, cualidad que se ve disminuída si se utilizan bajas dosis. Sin olvidar el riesgo de desarrollar hipertermia maligna con ambos fármacos en pacientes con miopatías diagnosticadas.2
Tanto en el estudio realizado por Mayorga y Cols.5 como en el realizado por Canedo y Cols.2 se resalta la importancia de la visita preanestésica y de la planificación en la toma de decisiones. De allí que, al igual que ellos, se decidió optar por un manejo multidisciplinario, redactando además una hoja con las recomendaciones mas importantes en el manejo de los posibles escenarios respecto a la paciente incluidos en un anexo.
Por último, la estrategia utilizada va en consonancia con lo descrito por los autores antes mencionados, siendo la analgesia una alternativa segura y eficaz para el manejo de la paciente con ambas patologías, lo que permitió un desarrollo del trabajo de parto sin incidencias fuera de lo común. No se puede dejar de lado la importancia de informar a la paciente, a todo el equipo sanitario implicado, así como la constate actualización para estar al día de los avances, beneficios y riesgos de cada técnica y patología. Igualmente, es importante una revisión de los hechos posterior a la resolución de los mismos para encontrar posibles fallos a mejorar, así como reforzar los aciertos obtenidos. La implementación de las listas de verificación y seguridad son una herramienta de ayuda que, sin duda, puede mejorar la eficacia del equipo médico y la seguridad del paciente.
Conclusiones
Tanto la enfermedad de McArdle como la esclerosis múltiple no tienen por qué alterar el curso normal del embarazo ni la adaptación fisiológica de la madre al mismo. Sin embargo, se pueden presentar en el contexto del parto exacerbaciones en la sintomatología que es recomendable documentar y monitorear. Es recomendable la realización de pruebas de laboratorio, con especial foco en alteraciones de la función renal por mioglobinuria o rabdomiólisis, así como también niveles de glucosa en sangre y equilibrio iónico. Además por supuesto de una estrecha vigilancia clínica.
La realización de un manejo multidisciplinario, así como la de una estrategia de planificación antes los distintos eventos que se puedan presentar, no solo nos asegura una mayor tasa de éxito sino también una mejor preparación de cara al desarrollo de los mismos.
Se recomienda la administración de suero glucosado al 5 % durante el parto manteniendo la normoglucemia. La analgesia epidural para la atención del parto es recomendable pues no solo disminuye el agotamiento de la madre, sino que además mejora el confort de la misma durante el trabajo del parto y proporciona una vía de acceso a una anestesia neuroaxial en caso de ser necesaria, disminuyendo los riesgos de una anestesia general en la embarazada.
En caso de anestesia general, por situación de carácter emergente se recomienda evitar el uso de succinilcolina, vigilar las posibles alteraciones renales y la elección tanto de los agentes hipnóticos como relajantes musculares de acuerdo a la situación que se presente.
Es recomendable evitar el uso de agentes inhalados.
Bibliografía
- García-Consuegra Galiana I. Aspectos moleculares de la enfermedad de McArdle [Tesis]. Madrid. Universidad Complutense de Madrid. Servicio de publicaciones: 2013. (HTML)
- Canedo Caballeira E M. Freire Vila E. Carballo Martínez M J. De la Iglesia López A. Control del embarazo y manejo intraparto en la enfermedad de McArdle. Prog Gin Obst [internet]. 2008. [citado 22 de enero de 2022];51(5)307-310. Disponible en https://www.elsevier.es/es-revista-progresos-obstetricia-ginecologia-151-articulo-control-del-embarazo-manejo-intraparto-S0304501308710914
- Antón Antón B, Asensio Pascual P. Guía informativa para la glucogenosis tipo v (enfermedad de McArdle). Asociación española de enfermos de glucogenosis [internet]. 2010. . [citado 12 de noviembre de 2023]. Disponible en: https://www.glucogenosis.org/wp-content/uploads/2018/04/GUIA-tipo_v.pdf
- Pérez Menéndez A. Sociedad Española de Neurología [internet]. España. Departamento de prensa:2015 [citado 22 de enero de 2022];Sala de prensa. Disponible en: https://www.sen.es/saladeprensa/pdf/Link178.pdf
- Mayorga Buiza M J.; Caba Barrientos F.; Suárez Cordero F.; Echevarría Moreno M. Analgesia epidural para el trabajo de parto en gestante con esclerosis múltiple. RESED Madrid. 2010. 17(5) (HTML)
- Bornemann-Cimenti H, Sivro N, Toft F. et al. Neuroaxial anesthesia in patients with multiple sclerosis – a systematic review. Rev Bras Anestesiol. 2016. (PubMed)