Iglesias Guitián R, Alonso Ramos I, Pretus Rubio S
FEA Anestesiología, Reanimación y Tratamiento del Dolor. Servicio de Anestesiología y Reanimación, Hospital universitario de Getafe, España.
Cómo citar este artículo: Iglesias Guitián, R., Alonso Ramos , I., & Pretus Rubio, S. (2024). Anestesia en la cirugía oncológica de mama. Revista Electrónica AnestesiaR, 16(6). https://doi.org/10.30445/rear.v16i6.1203
Introducción
La cirugía de mama abarca numerosos procedimientos incluidos la escisión de lesiones benignas, drenaje de abscesos o procedimientos estéticos; sin embargo, la indicación más frecuente en cirugía mamaria es la cirugía oncológica.
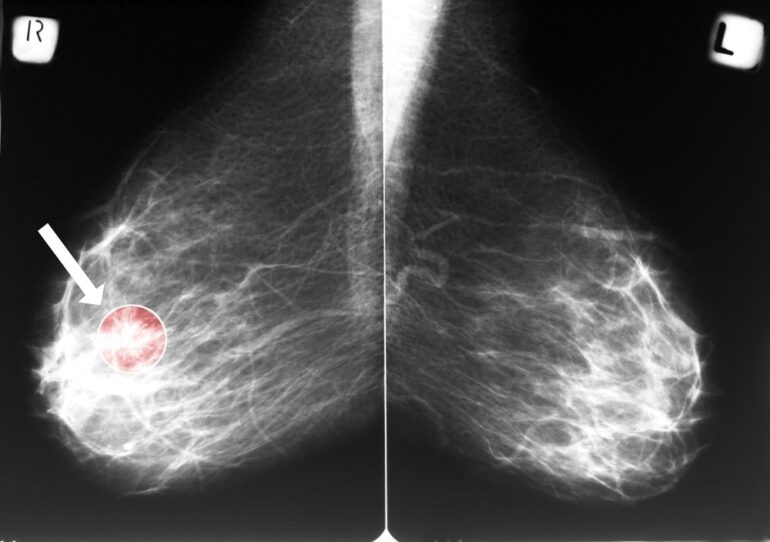
El cáncer de mama, si excluimos los tumores de piel no melanomas, representa el tumor maligno más frecuente de la población femenina en todo el mundo, tanto en los países desarrollados como en vías de desarrollo, y supone una cuarta parte de todos los cánceres en la mujer.
Entre las técnicas quirúrgicas del cáncer de mama están la mastectomía radical, la tumorectomía, la biopsia selectiva de ganglio centinela (BSGC), el vaciamiento ganglionar axilar, o la reconstrucción mamaria tras la resección tumoral.
En estadios tempranos del cáncer de mama, la cirugía supone un paso fundamental dentro del tratamiento multidisciplinar, puesto que puede llegar a ser curativa en sí misma. Con la combinación de radioterapia puede controlar la enfermedad en la mayoría de los casos.
A pesar de eso, alrededor de un 30% de las pacientes fallecen debido a diseminación de la enfermedad. Para erradicar las micrometástasis, se desarrollaron terapias coadyuvantes como la hormonoterapia, inmunoterapia o quimioterapia. No es infrecuente, por lo tanto, que sean complementarias al tratamiento quirúrgico.
La mayoría de las pacientes experimentan altos niveles de ansiedad y estados emocionales negativos ante la posibilidad del diagnóstico de malignidad, así que también es recomendable la medicación ansiolítica preoperatoria.
Procedimiento
Puntos críticos de la cirugía oncológica de mama
El tratamiento quirúrgico del cáncer de mama ha ido evolucionando en los últimos años. La técnica más frecuente hasta los años 70 era la mastectomía radical (Halsted) que consistía en la extirpación de la mama, piel circundante, músculos pectorales y ganglios linfáticos axilares, lo que generaba gran morbilidad y discapacidad en el brazo ipsilateral, además de deformidad en la pared torácica.
La mastectomía radical modificada, en la que se mantiene el músculo pectoral mayor, reemplazó a la anterior al no detectarse cambios en la supervivencia y producir menor morbilidad.
La mastectomía simple consiste en extirpar únicamente la mama con cáncer (en algunos casos puede preservarse la areola y el pezón).
La cirugía conservadora de mama consiste en la tumorectomía o cuadrantectomía.
En cuanto a la BSGC, consiste en la inyección de un radiotrazador en la zona peritumoral que permite identificar al primer ganglio de drenaje del tumor. Es la primera estación ganglionar que comunica con el tumor, de modo que si el ganglio centinela no está afectado por metástasis no es necesario realizar una linfadenectomía axilar.
La cirugía oncoplástica consiste en combinar la cirugía oncológica pura con técnicas de cirugía plástica de reconstrucción, pudiéndose realizar tras la extirpación del tumor o de forma diferida. La reconstrucción mamaria puede llevarse a cabo con prótesis (expansores temporales o implantes de suero salino fisiológico) o colgajos miocutáneos autólogos. Si la paciente va a recibir radioterapia suele recomendarse la cirugía de reconstrucción diferida.
Posición quirúrgica
La mayoría de procedimientos se llevan a cabo con la paciente en decúbito supino con los brazos pegados. A veces es necesario que los brazos estén en abducción a 90º, sobre todo en los procedimientos bilaterales. Hay que vigilar la posición de la paciente para evitar la lesión del plexo braquial por sobredistensión y mala alineación del cuello con las articulaciones de los hombros.
A veces, al finalizar la cirugía mamaria se valoran asimetrías en sedestación.
Profilaxis antibiótica
Cefazolina 2 g o amoxicilina/clavulánico 2 g. Si existe alergia a betalactámicos: vancomicina 1 g i.v.
Técnica anestésica en cirugía oncológica de mama: diferentes opciones
Anestesia general
Se puede realizar anestesia general balanceada o intravenosa (TIVA). En nuestro servicio, preferimos utilizar la TIVA para disminuir la incidencia de náuseas y vómitos postoperatorios puesto que la cirugía de mama es una cirugía emetógena. Es de elección frente a los anestésicos halogenados por sus efectos sobre la enfermedad tumoral, ya que el uso de anestésicos volátiles podría favorecer la expresión génica en células tumorales.
Para el manejo de la vía aérea, pueden utilizarse tanto dispositivos supraglóticos como la intubación orotraqueal (IOT). La IOT se prefiere en cirugías con cambios posturales, procedimientos largos o si la posición quirúrgica requiere hiperextensión y lateralización de la cabeza hacia el lado contralateral.
Bloqueos regionales
La gran variedad de técnicas regionales para la cirugía mamaria, en auge debido a su gran efectividad, implica que, a día de hoy, no exista una técnica que pueda considerarse de elección. Las técnicas anestésicas regionales disminuyen el consumo de opioides, mejoran el dolor postoperatorio, atenúan la respuesta neuroendocrina a la cirugía, disminuyen las náuseas y vómitos postoperatorios y mejoran la recuperación postoperatoria. También permiten la inserción de catéteres para infusión continua de medicación en el perioperatorio.
Debido a su inervación, es complicado conseguir una analgesia completa de la mama, por lo que se aplicarán uno o varios tipos de bloqueos según el tipo de cirugía que se realice.
Los bloqueos regionales más utilizados son el bloqueo de las ramas cutáneas anteriores de los nervios intercostales en línea medioaxilar (BRILMA), bloqueo interpectoral (PEC), bloqueo del plano del erector de la espina (ESP) y bloqueo epidural, en caso de bilateralidad.
Los bloqueos miofasciales son dependientes de volumen y no de concentración del AL (anestésico local, por lo que necesitaremos entre 15-40 ml por bloqueo. En nuestro servicio, solemos utilizar la levobupivacaína 0.25% o 0.125%. La técnica puede aplicarse bilateralmente calculando la dosis tóxica de AL previa realización.
Bloqueo interpectoral (PEC)
El bloqueo PEC I consiste en depositar AL entre el músculo pectoral mayor y músculo pectoral menor a nivel de la tercera costilla para bloquear los nervios pectorales lateral y medial. El bloqueo PEC II se trata de una modificación del PEC I donde se inserta AL entre el músculo serrato anterior y pectoral menor. Se consigue anestesiar así el nervio intercostobraquial, el torácico largo y ramas cutáneas laterales de los nervios intercostales. No permite cubrir las ramas anteriores de los intercostales pero aporta analgesia axilar.
Indicaciones PEC I: cirugía reconstructiva de mama limitada al pectoral mayor (implante subpectoral o colocación de expansores de mama).
Indicaciones PEC II: similar al PEC I y en mastectomías, BSGC o tumorectomías.
Bloqueo BRILMA
Se deposita el AL entre el músculo serrato anterior y músculo intercostal externo. Con esta técnica, se consigue bloquear las ramas cutáneas laterales y anteriores de los nervios intercostales. Siempre debe realizarse bajo visión ecográfica (por riesgo de neumotórax y lesión de la arteria torácica lateral) y puede realizarse con seguridad bajo sedación o bajo anestesia general (de elección en nuestro servicio). En mastectomías, lo ideal es realizar el bloqueo en el sexto espacio intercostal y, en tumorectomías, un espacio intercostal por debajo de la localización del tumor.
Indicaciones BRILMA: cirugía de mama no reconstructiva (mastectomía con o sin vaciamiento axilar, tumorectomía y BSGC).
Bloqueo epidural
En cirugía mayor bilateral (mastectomía bilateral, cirugía de colgajo bilateral etc). Suele realizarse a nivel torácico T4 – T7.
Bloqueo del plano del erector de la espina (ESP)
Se deposita el AL entre el plano fascial del músculo erector espinal y entre la apófisis transversa torácica de T4.
Indicaciones ESP: mastectomía radical.
Bloqueo paravertebral
A pesar de ser el bloqueo de referencia para este tipo de cirugía, en la actualidad se encuentra en desuso y no lo utilizamos en nuestro servicio para proporcionar analgesia postoperatoria.
Monitorización
Estándar no invasiva. Los electrodos deben adaptarse al campo quirúrgico. Es útil colocarlos en la espalda y en la parte posterior de los hombros, vigilando posibles lesiones por decúbito.
Es importante la venoclisis en el brazo contralateral a la cirugía, sobre todo si incluye linfadenectomía, para evitar linfedema. Si la cirugía es bilateral, hay que valorar la venoclisis en miembros inferiores. También es recomendable evitar compresiones y la toma de presión arterial en el brazo ipsilateral al vaciamiento ganglionar axilar.
La monitorización hemodinámica —incluyendo la monitorización de la presión arterial invasiva— debe individualizarse según comorbilidades y técnica quirúrgica. Debe considerarse en cirugías de larga duración, reintervenciones o pacientes que hayan recibido quimioterapia neoadyuvante o terapia hormonal, ya que puede asociar complicaciones cardiacas por cardiotoxicidad (sobre todo inducida por antraciclinas o trastuzumab).
Es importante mantener la normotermia y monitorizar la temperatura en aquellos procedimientos mayores de 30 minutos de duración. Se pueden utilizar fluidos calientes, mantas de calor o aumentar la temperatura ambiente.
Es prudente la aplicación de medias de compresión en procedimientos cortos y añadir medias neumáticas intermitentes a los procedimientos más largos, ya que reduce el riesgo de tromboembolismo pulmonar.
Fluidoterapia
Aporte de cristaloides 3-5 ml/kg/h.
Analgesia
La analgesia postoperatoria estará influenciada por la realización de bloqueos regionales. Las pautas analgésicas más frecuentemente empleadas se basan en la combinación de antiinflamatorios no esteroideos y opioides. En nuestra reanimación, pautamos paracetamol 1 g c/8 h con dexketoprofeno 50 mg c/8 h y, de rescate, dejamos metamizol 2 g y cloruro mórfico 2 mg.
Sangrado
Varía según el tipo de cirugía, pero en principio no es una cirugía con alto riesgo de sangrado. Aún así habrá que prestar atención a los aspiradores del campo quirúrgico.
Duración
Varía según el tipo de procedimiento.
Complicaciones intraoperatorias específicas
- Lesiones pleurales: se deben a la ligadura o electrocoagulación de algún vaso intercostal que se encuentre adherido a la pleura. Es más frecuente al extirpar la cadena ganglionar de la mama interna. La lesión pleural debe ser suturada. Dependiendo de la extensión de la misma y del grado de neumotórax y colapso pulmonar, puede ser necesaria la colocación de un tubo endotorácico con aspiración bajo el agua.
- Lesiones vasculares: tanto sangrado como trombosis o tromboflebitis postoperatoria.
- Linforragia: se debe a la sección de los vasos linfáticos colectores, aparece en casi todas las linfadenectomías axilares. Puede producir infecciones o alteraciones en la cicatrización.
- Lesiones nerviosas: pueden ser temporales o definitivas. Aparecen por compresión o por sección de los troncos nerviosos. No es infrecuente que las pacientes sufran hipoestesias en la cara interna del brazo debido a la sección del nervio intercostohumeral. Los síntomas suelen ceder en 3 a 6 meses.
Observaciones
En algunas cirugías (como en la BSGC o las tumorectomías) se realizan biopsias intraoperatorias para aproximar el diagnóstico de las lesiones y precisar el mejor abordaje terapéutico durante el mismo acto quirúrgico. No se debe proceder a la educción anestésica antes de conocer el resultado intraoperatorio de las lesiones.
En la cirugía oncoplástica con colgajos, es importante evitar la hipotermia, la hipovolemia y la vasoconstricción ya que pueden alterar la perfusión del colgajo. También debemos evitar la administración excesiva de fluidos intravenosos para disminuir el edema postoperatorio.
Las lesiones sospechosas de malignidad no palpables suelen marcarse con arpón o aguja previamente en el área de radiodiagnóstico. Las pacientes llegan a quirófano con la aguja colocada y es importante no modificar la posición de la misma. Puede producirse un neumotórax por lo que si la paciente acude a quirófano con disnea, dolor torácico, desaturación de oxígeno o inestabilidad hemodinámica debemos sospecharlo.
Bibliografía
- A. Shah, M. Rowlands, N. Krishnan, A. Patel, A. Ott-Young. Thoracic intercostal nerve blocks reduce opioid consumption and length of stay in patients undergoing implant-based breast reconstruction. Plast Reconstr Surg., 136 (2015), pp. 584e-591e (PubMed)
- Peral Sánchez D, Porcar Rodado E. El cáncer de mama desde Anestesia. Revista de Senología y Patología Mamaria 2021. https://doi.org/10.1016/j.senol.2020.08.003
- – G.S. Cheng, B.M. Ilfeld. An Evidence-Based Review of the Efficacy of Perioperative Analgesic Techniques for Breast Cancer-Related Surgery. Pain Med., 18 (2017), pp. 1344-1365 http://dx.doi.org/10.1093/pm/pnw172
- García Delgado, J., Morales Chaucalá G., García Arana, A. (2020). Cáncer de mama: una revisión para el cirujano general. RECIMUNDO, 4(2), 236-249. doi: 10.26820/recimundo/4.(2).mayo.2020.236-249