Pretus Rubio S, Díaz Campanero P, Iglesias Guitián R
FEA del Servicio de Anestesiología y Reanimación del Hospital Universitario de Getafe. Madrid. España.
Cómo citar este artículo: Pretus Rubio, S., Díaz Campanero, P., & Iglesias Guitián, R. (2024). Cirugía de carótida: endarterectomía y angioplastia carotídea. Revista Electrónica AnestesiaR, 16(4). https://doi.org/10.30445/rear.v16i4.1194
Introducción
Las enfermedades cardiovasculares presentan una elevada morbimortalidad. Las lesiones vasculares pueden tener una etiología isquémica o hemorrágica. El 80% de los accidentes cerebrovasculares (ACV) son isquémicos y, dentro de estos, un 20-25% se deben a estenosis de la arteria carótida. La causa fundamental de los ACV isquémicos es la aterosclerosis mediante un mecanismo embólico tras rotura de una placa de ateroma.
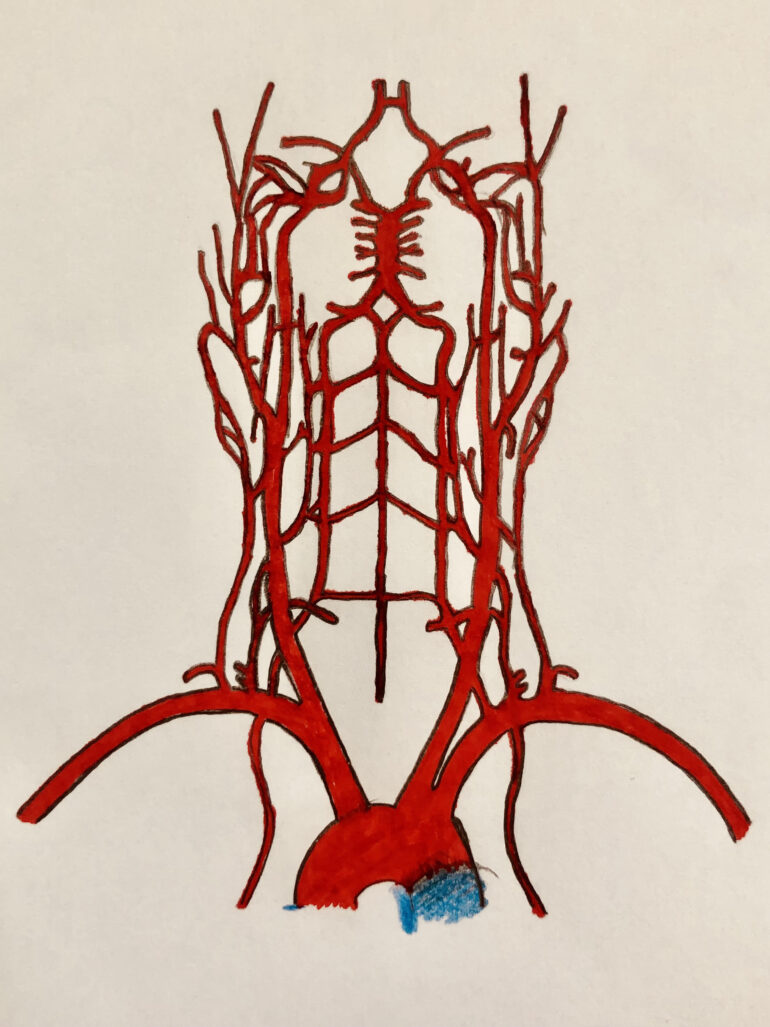
El 80-90% del flujo sanguíneo cerebral depende de las dos arterias carótidas internas (ACI) y el resto proviene en su mayoría del sistema vertebro-basilar. Las arterias carótidas y la arteria basilar forman el polígono de Willis en la base del cerebro. Esta compleja disposición ofrece la protección adecuada para mantener de manera constante el aporte sanguíneo cerebral.
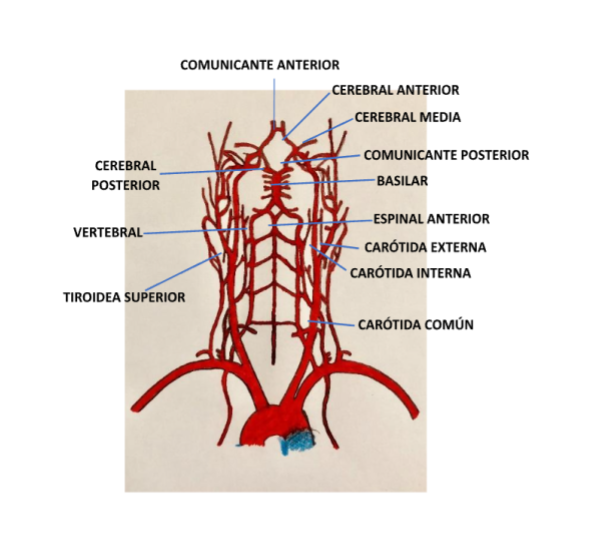
Aparecen señaladas las arterias principales.
Indicaciones de la cirugía de carótida
Las indicaciones generales para la cirugía de carótida, por lo tanto, se definen según la presencia de síntomas y el grado de estenosis.
Pacientes asintomáticos
- La cirugía está indicada en todos los casos cuando la estenosis de la ACI es mayor del 70%.
- En estenosis del 60-69% se debe individualizar según las características de cada paciente.
Pacientes sintomáticos
En los pacientes sintomáticos, la cirugía se debe realizar de manera precoz cuando esté indicada. Cuando la estenosis de la ACI es mayor del 70%, la cirugía de carótida supone una disminución del 16% del riesgo de muerte y de ACV en 5 años. En las estenosis entre el 50% y el 69%, reduce la mortalidad y el riesgo de ACV en 5 años un 4,6%. Por debajo del 50%, no se recomienda la cirugía.
Procedimiento
Endarterectomía carotídea (EAC)
Constituye el tratamiento de elección en la estenosis ateromatosa crítica de la bifurcación carotídea.
El procedimiento consiste en retirar la placa de ateroma de la arteria carótida interna.
Se realiza un abordaje ventroyugular mediante una incisión cervical oblicua a lo largo del borde interno del músculo esternocleidomastoideo, desde el lóbulo de la oreja hasta la base del cuello.
Para la retirada de la placa de ateroma se realiza una incisión longitudinal de la bifurcación carotídea. El cierre posterior de la arteriotomía se puede realizar con sutura directa o mediante un parche sintético o injerto de vena.
Requiere la exposición de la arteria carótida común y sus ramas externa e interna. Una vez lograda, se procede a la administración de un bolo de heparina sódica no fraccionada (HNF) por vía intravenosa a dosis de 1 mg/kg (100 UI/kg).
Posteriormente, tras 3-5 minutos para lograr el efecto de la heparinización, se realiza el clampaje secuencial de las arterias tiroidea, ACI, arteria carótida común y arteria carótida externa.
El desclampaje debe seguir el orden inverso, dejando siempre en último lugar a la ACI para evitar cualquier embolización a su través.
Aproximadamente 10 minutos tras el desclampaje y comprobada la ausencia de sangrado, se procede a la administración de un bolo lento intravenoso de protamina a dosis de 1 mg por cada 100 UI de HNF.
Angioplastia transluminal percutánea (PTA) carotídea y colocación de stent carotídeo
Esta técnica quirúrgica ha demostrado tener resultados clínicos similares a la EAC. Constituye una alternativa en pacientes con elevado riesgo quirúrgico por comorbilidad asociada grave, estenosis localizadas en lugares inaccesibles, reestenosis tras EAC previa y pacientes con antecedentes de cirugía o radiación a nivel cervical.
Se realiza de manera endovascular mediante un acceso inguinal a través de la arteria femoral guiado por radiología y con uso de contraste yodado.
Se requiere mecanismos de protección cerebral como balones oclusivos o filtros de protección, colocados más allá de la estenosis, que eviten la migración proximal de émbolos mientras se hincha el balón intraluminal y se coloca el stent.
También es necesaria la heparinización, pero sin reversión posterior con protamina porque podría causar la trombosis del stent.
Posición quirúrgica
El paciente se coloca en decúbito supino con los brazos pegados al cuerpo y el cuello extendido y girado hacia el lado contrario al de la cirugía. En este punto es muy importante evitar la hiperextensión cervical, así como la rotación lateral excesiva que podría comprimir la arteria carótida y disminuir la perfusión cerebral del lado contralateral.
Profilaxis antibiótica
Se trata de una cirugía limpia.
En la PTA carotídea, está indicada la profilaxis antibiótica con cefazolina (2 gramos).
En la EAC, únicamente está indicada la profilaxis antibiótica cuando se va a implantar material protésico. En pacientes con alergia a antibióticos β-lactámicos se administrará teicoplanina.
Técnica anestésica: diferentes opciones
La EAC se puede realizar con anestesia general o con anestesia regional (bloqueo del plexo cervical superficial) con el paciente despierto. No existe evidencia de superioridad de una técnica respecto a otra.
En el Hospital Universitario de Getafe (HUG), se realiza actualmente anestesia general, combinada en algunos casos con el bloqueo ecoguiado del plexo cervical superficial como técnica analgésica.
En cirugía endovascular, el procedimiento se realiza bajo anestesia general.
Una alternativa en la PTA carotídea sería la anestesia local con sedación, especialmente en pacientes con gran comorbilidad.
| ANESTESIA GENERAL | ANESTESIA REGIONAL |
Mayor comodidad del paciente(ansiedad, incapacidad para colaborar o comunicarse, deterioro cognitivo). Mayor comodidad para el cirujano. Potencial efecto neuroprotector. Control de la vía aérea. Evita reconversiones urgentes a anestesia general. | Paciente despierto o con mínima sedación. Dexmedetomidina. Gold standard para la monitorización neurológica. Mantenimiento de la autorregulación cerebral. Mayor estabilidad hemodinámica. Menos complicaciones cardiorrespiratorias. Menor deterioro cognitivo postoperatorio. Menor tiempo de ingreso hospitalario |
El objetivo del anestesiólogo durante el intraoperatorio es garantizar la protección miocárdica y cerebral, controlando los factores que puedan contribuir al riesgo de isquemia.
La mayoría de los ACV perioperatorios tiene un origen embólico; únicamente un 15% se pueden atribuir a la isquemia cerebral durante el pinzamiento carotídeo.
Durante la anestesia general, se recomienda el uso de fármacos de acción corta que permitan un despertar precoz y extubación en el quirófano seguida de una valoración neurológica inmediata, como el remifentanilo.
No existen diferencias estadísticamente significativas entre las técnicas de anestesia general total intravenosa y anestesia general balanceada. La autorregulación cerebral está preservada tanto con el uso de propofol como con sevoflurano a dosis ≤ 1 CAM. Además, el uso de mayores concentraciones de sevoflurano se debe evitar por la potencial interferencia con la neuromonitorización.
Es muy importante la profilaxis de náuseas y vómitos, así como evitar la tos y la hipertensión arterial durante la extubación por el riesgo de desarrollar un hematoma cervical que pueda comprometer la vía aérea.
Puntos críticos del procedimiento quirúrgico
El primer punto crítico de la cirugía, por la gran labilidad hemodinámica que produce generalmente con bradicardia e hipotensión, es la manipulación de la zona del seno carotídeo durante la EAC (se puede administrar lidocaína al 2% sobre la zona del seno carotídeo para disminuir la estimulación de sus barorreceptores) o el inflado del balón en la PTA (se recomienda la administración previa de atropina).
El segundo punto crítico de la cirugía es el clampaje de la arteria carótida que puede producir isquemia cerebral ipsilateral, con riesgo de daño neurológico irreversible, debido a mecanismos como la disminución del flujo sanguíneo carotídeo y/o rotura de la placa de ateroma con embolización cerebral.
Medidas de protección cerebral
- La primera medida es el mantenimiento de la normocapnia (límite superior de la hipercapnia). No se recomienda la hipercapnia permisiva con el objetivo de inducir vasodilatación cerebral ya que puede producirse un fenómeno de «robo», en el que el aumento del flujo sanguíneo se dirija hacia la zona de tejido cerebral que está siendo perfundida normalmente. Además, aumenta el riesgo de embolización.
- Control estricto de la tensión arterial. Durante el pinzamiento carotídeo, es fundamental evitar la hipotensión arterial manteniendo unos valores un 20% por encima de los basales. Por el contrario, durante la restauración del flujo es muy importante que no exista hipertensión arterial para evitar un síndrome de hiperperfusión.
- Incremento de la fracción inspirada de oxígeno antes del pinzamiento carotídeo y durante el clampaje (según monitorización neurológica).
- Normoglucemia.
- Hipotermia leve.
- Colocación de un shunt vascular entre la arteria carótida común y la arteria carótida interna: su indicación debe ser selectiva (ante alteraciones significativas en la oximetría cerebral o aparición de nuevo déficit neurológico en el paciente despierto).
Monitorización
- Electrocardiograma y pulsioximetría.
- Monitorización invasiva de la presión arterial: es necesaria su monitorización continua. Canalizaremos la arteria radial del lado contrario a la lesión antes o después de la inducción anestésica en función de la patología cardiovascular del paciente.
- Monitor de índice biespectral (BIS).
- Monitorización neurológica mediante oximetría cerebral no invasiva:
- Mide la saturación venosa de oxígeno.
- Se deben establecer los valores basales (antes de preoxigenar y de premedicar).
- Valores normales 60 – 70%.
- Es patológico cuando existe una asimetría > 10 puntos entre ambos hemisferios o cuando el valor basal es 50 %.
- Un descenso se considera significativo cuando es ≥ 20 % del valor basal.
- Sondaje vesical.
- Accesos vasculares: canalizaremos dos vías venosas periféricas (18G/16G).
Fluidoterapia
La cirugía de carótida no suele estar asociada a una pérdida excesiva de líquidos por lo que rara vez se requiere reanimación con volumen en grandes cantidades. Administraremos en torno a 1000 ml de soluciones cristaloides balanceadas. En la cirugía endovascular, debemos tener en cuenta la hidratación como medida de prevención de la nefropatía inducida por contraste.
Analgesia
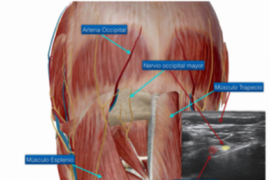
Se recomienda realizar un bloqueo ecoguiado del plexo cervical superficial (ramas sensoriales de las raíces nerviosas C2, C3 y C4). Las raíces forman las cuatro ramas terminales (nervios occipital menor, auricular mayor, cervical transverso y supraclavicular) y emergen por detrás del borde posterior del músculos esternocleidomastoideo (ECM). El plexo se puede visualizar como una pequeña colección de nódulos hipoecoicos inmediatamente profundo o lateral al borde posterior del ECM.
El objetivo es colocar la punta de la aguja en la capa fascial debajo del ECM adyacente al plexo cervical, que está contenido dentro del espacio de tejido entre la fascia cervical y la vaina posterior del ECM. Suele ser suficiente un volumen de 5-10 mililitros de anestésico local.
Sangrado
En ausencia de complicaciones intraoperatorias, la pérdida sanguínea estimada es escasa en torno a 100-200 ml.
Por la posibilidad de complicaciones durante la manipulación arterial, siempre es necesario disponer de pruebas cruzadas y una vía venosa periférica de gran calibre.
En la cirugía endovascular debemos vigilar el sangrado oculto.
Duración
La duración total aproximada de la cirugía es de 90 minutos y el tiempo de clampaje en torno a 30 minutos.
Complicaciones intraoperatorias específicas
- Complicaciones neurológicas de origen isquémico durante el pinzamiento carotídeo, sobre todo si está afectada la circulación contralateral o vertebral.
- Embolización ateromatosa o aérea.
- Disección carotídea.
- Hemorragia intracraneal.
- Vasoespasmo de la arteria carótida.
- Isquemia miocárdica.
- Hematoma cervical y daño de estructuras nerviosas por tracción quirúrgica en la EAC.
- Hematoma femoral, nefropatía por contraste y trombosis de la luz del stent en la PTA carotídea.
Observaciones
En el Hospital Universitario de Getafe, se realiza actualmente anestesia general combinada en algunos casos con el bloqueo ecoguiado del plexo cervical superficial como técnica analgésica. De cara al futuro, se podría valorar la realización de EAC únicamente con anestesia regional y con el paciente despierto, ya que es el gold standard para la monitorización neurológica.
El objetivo del anestesiólogo durante el intraoperatorio es garantizar la protección miocárdica y cerebral controlando los factores que puedan contribuir al riesgo de isquemia. Presentan especial importancia los puntos críticos de la cirugía: manipulación de la zona del seno carotídeo y tiempo de isquemia.
Es fundamental disponer de una monitorización neurológica lo más precisa posible y establecer durante el intraoperatorio las medidas de protección cerebral.
Bibliografía
- Allain R, Marone LK, Meltzer J, Jeyabalan G. Carotid endarterectomy. Int Anesthesiol Clin. 2005; 43(1): 15-38. doi: 10.1097/01.aia.0000150279.00355.6c. PMID: 15632515. (PubMed)
- GALA Trial Collaborative Group; Lewis SC, Warlow CP, Bodenham AR, Colam B, Rothwell PM, Torgerson D, Dellagrammaticas D, Horrocks M, Liapis C, Banning AP, Gough M, Gough MJ. General anaesthesia versus local anaesthesia for carotid surgery (GALA): a multicentre, randomised controlled trial. Lancet. 2008 Dec 20; 372(9656): 2132-42. doi: 10.1016/S0140-6736(08)61699-2. Epub 2008 Nov 27. PMID: 19041130. (PubMed)
- John Augoustides, MD, FASE, FAHA, Jacob T Gutsche, MD, FASE, FCCM, Jared W Feinman, MD, FASE. ANESTHESIA FOR CAROTID ENDARTERECTOMY AND CAROTID STENTING. UpToDate. 2022. (PDF)
- Writing Group a, A.R. Naylor, J.-B. Ricco, G.J. de Borst, S. Debus, J. de Haro, A. Halliday, G. Hamilton, J. Kakisis, S. Kakkos, S. Lepidi, H.S. Markus, D.J. McCabe, J. Roy, H. Sillesen, J.C. van den Berg, F. Vermassen, ESVS Guidelines Committee b, P. Kolh, N. Chakfe, R.J. Hinchliffe, I. Koncar, J.S. Lindholt, M. Vega de Ceniga, F. Verzini, ESVS Guideline Reviewers c , J. Archie, S. Bellmunt, A. Chaudhuri, M. Koelemay, A.-K. Lindahl, F. Padberg, M. Venermo. Management of Atherosclerotic Carotid and Vertebral Artery Disease: 2017 Clinical Practice Guidelines of the European Society for Vascular Surgery (ESVS). Eur J Vasc Endovasc Surg. 2017: 1-79. http://dx.doi.org/10.1016/j.ejvs.2017.06.021. (PubMed)