Lamarca Mendoza, M.P. (1), Flores Herrero, A (1), Orgaz Pérez Grueso, A. (2), Paz Martín, D. (3)
(1) Médico Interno Residente. Servicio de Angiología y Cirugía Vascular. Complejo Hospitalario de Toledo
(2) Jefe de Servicio de Angiología y Cirugía Vascular. Complejo Hospitalario de Toledo
(3) Médico adjunto. Servicio de Anestesiología y Reanimación. Complejo Hospitalario de Toledo
Cómo citar este artículo: Lamarca Mendoza, M. P., & Paz Martín, D. (2015). Paraplejia asociada a la cirugía aórtica. Revista Electrónica AnestesiaR, 7(9), 2. https://doi.org/10.30445/rear.v7i9.187
La paraplejia tras la cirugía aórtica es una complicación devastadora. La nueva era de la cirugía endovascular disminuye la morbimortalidad perioperatoria pero no es capaz de evitar el riesgo neurológico. La médula espinal recibe irrigación de la arteria espinal anterior, que se encarga aproximadamente de dos tercios de ella (la porción motora), y de 2 arterias espinales posteriores, que se encargan del tercio restante. La arteria espinal anterior se forma a partir de la confluencia de las 2 arterias vertebrales, y suple la parte más craneal de la médula. Recibe múltiples colaterales: las arterias radiculomedulares, lumbares e intercostales, la arteria hipogástrica, la arteria sacra media y la arteria mesentérica inferior. La arteria radiculomedular más importante es la de Adamkiewics, que tiene un curso anatómico variable y suele originarse entre T8 y L1. Tradicionalmente se creía que la mayoría de la perfusión medular dependía de esta arteria, pero actualmente se cree que corresponde a una red de colaterales que conectan numerosas pequeñas arterias entre ellas y con las principales arterias de la médula.
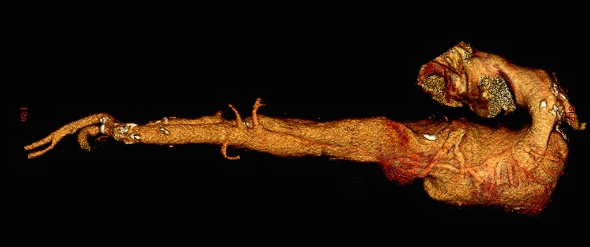
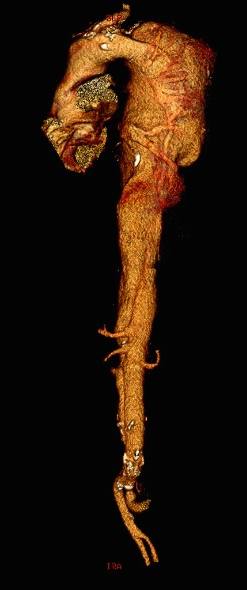
Figura 1.-Aneurisma de aorta torácica
Las arterias espinales posteriores se originan también en las arterias vertebrales, y reciben, a su vez, sangre de las arterias radiculomedulares posteriores.
La paraplejia en la cirugía aórtica torácica y toracoabdominal se explica principalmente a causa de la oclusión de las arterias segmentarias: el principal predictor de paraplejia es la extensión de arteria espinal anterior sacrificada. Este riesgo se presenta tanto en la cirugía abierta como en las intervenciones endovasculares, presentando menor riesgo esta última, con un 14% y un 5“™4% respectivamente. La médula es especialmente vulnerable durante las primeras 24-48 horas tras un sacrificio extenso de la espinal anterior, hasta que ocurre una adaptación del sistema de colaterales. Por ello la cirugía en varios tiempos ha demostrado que disminuye el riesgo de complicaciones neurológicas. En base a esto está surgiendo una nueva hipótesis para la prevención de la paraplejia: la embolización de arterias segmentarias semanas antes de la intervención para favorecer la apertura de nuevas colaterales. Todavía se encuentra en experimentación.
Los principales factores que influyen en el riesgo de paraplejia son: la extensión mayor del aneurisma, la hipotensión, la cirugía emergente, la cirugía abierta, la rotura aórtica aguda, la disección de aorta, la mayor duración del clampaje aórtico, la no reimplantación de las arterias segmentarias, la enfermedad vascular severa, la oclusión de la arteria subclavia izquierda y las arterias hipogástricas, la cirugía de aorta abdominal previa, el fallo renal y la anemia.
Mecanismos de prevención de la isquemia medular
Se han descrito varios mecanismos para prevenir la isquemia medular durante estas intervenciones:
– La disminución del tiempo de isquemia medular, que puede realizarse con una reconstrucción segmentaria de la aorta o con un shunt para perfundir la aorta distal.
– El aumento de la tolerancia a la isquemia, mediante maniobras como la hipotermia, que puede ser incluso selectiva medular con el enfriamiento epidural. También está descrita la neuroprotección farmacológica con acetazolamida o glucocorticoides, que inhiben la producción de LCR, pero lo estudios no han sido concluyentes.
– La reimplantación de las arterias segmentarias y de la arteria subclavia
– En el postoperatorio es importante evitar la hipovolemia, la hipertermia y las presiones venosas elevadas
– El aumento de la perfusión medular, basándose en la fórmula: Presión de Perfusión Medular (PPM) = Presión Arterial Media (PAM) – Presión Intramedular (PIM).
Drenaje de LCR
La producción de LCR tiene lugar en los plexos coroideos (70%) y en el epéndimo (30%), y es de 0“™2-0“™7 ml./min. (400-600 ml./24 h.), aproximadamente. El LCR circula libremente y de forma continua desde el cerebro al canal medular, reabsorbiéndose en los senos venosos. La reabsorción de LCR es proporcional a la presión de LCR, comenzando a 5 mmHg. y elevándose linealmente hasta 20 mmHg. Se interrumpe a los 60 mm. de agua, que corresponde a la presión de los senos venosos Un adulto presenta aproximadamente 150 ml. circulando, y se renueva cada 3-4 horas.
La colocación de drenaje lumbar probablemente sea la maniobra más útil a la hora de disminuir el riesgo de paraplejia en las intervenciones de aorta torácica, ya que ayuda a mantener presiones medulares controladas durante la cirugía y las 48 horas siguientes, facilitando la perfusión medular. Como previamente ya se ha comentado, durante las primeras 48 horas tras el sacrificio de parte de la circulación medular, ocurre una adaptación de la red de colaterales a la isquemia.
En la literatura pueden encontrarse únicamente 3 estudios randomizados y 1 metanálisis de éstos, en el que se objetiva una reducción absoluta de riesgo de paraplejia del 9% con el uso de drenaje de LCR en centros con experiencia en el tratamiento de aneurisma de aorta torácica.
Cuando se utiliza un drenaje lumbar con control manual e irregular, el débito y la presión se controla por la altura de éste. Esto puede conllevar el drenaje excesivo de líquido, que puede originar hipotensión intracraneal, que hasta en el 10% de los casos asocia un sangrado intracraneal agudo. Esto se explica por el desplazamiento caudal del cerebro y el alargamiento de los senos venosos, en los cuales pueden producirse roturas, originando un sangrado subdural. Los pacientes con malformaciones arteriovenosas, aneurismas cerebrales, historia previa de traumatismo craneal, alteraciones de la coagulación o hematoma subdural crónico tienen mayor riesgo de presentar complicaciones hemorrágicas a causa de la hipotensión intracraneal. Si se objetiva débito hemático o aparece clínica neurológica se deberá realizar un TAC craneal para descartar patología intracraneal asociada. Esto ocurre más frecuentemente si se drena abundante LCR durante la intervención y con aumento de la presión venosa central previamente al clampaje aórtico.
Figura 2. Sistema de drenaje lumbar controlado Liquoguard.
Actualmente existe un sistema de drenaje lumbar controlado (Liquoguard), (Figura 2), que monitoriza la presión intramedular, combinando, si el paciente lo precisa, el drenaje de LCR a una velocidad constante y máxima para evitar el drenaje excesivo, y siempre que la PIM sobrepasa el límite fijado por el operador. Permite, por lo tanto, conocer en todo momento la presión de perfusión medular, para así manejar el drenaje de LCR y la PAM en base a ello. Generalmente la presión medular ideal debe ser menor de 10 mmHg.
Conclusión
La paraplejia es una complicación temida en la cirugía de aorta torácica y toracoabdominal. Por el momento hay suficiente evidencia que apoya el uso de drenaje lumbar de LCR para el control de la presión intramedular. Se recomienda especialmente el sistema de drenaje Liquoguard, ya que permite monitorizar con exactitud la presión intramedular y controlar el drenaje de LCR a una velocidad premarcada y a unas presiones previamente establecidas, evitando el drenaje excesivo de LCR.
Además, conociendo la presión intramedular puede modificarse la PAM para mejorar la presión de perfusión medular.
Lecturas recomendadas
1.- Sinha AC, Cheung AT. Spinal cord protection and thoracic aortic surgery. Curr Opin Anaesthesiol. 2010;23(1):95-102: Explica las distintas técnicas que existen actualmente en la prevención de paraplejia. PubMed
2.- Ciní CS, Abouzahr L, Arena GO, et al. Cerebrospinal fluid drainage to prevent paraplegia during thoracic and thoracoabdominal aortic aneurysm surgery: a systematic review and meta-analysis. J Vasc Surg. 2004;40(1):36-44. Presenta los tres estudios randomizados que hay por el momento. PubMed
3.- Geisbí¼sch S, Schray D, Bischoff MS, et al. Imaging of vascular remodeling after simulated thoracoabdominal aneurysm repair. J Thorac Cardiovasc Surg. 2012;144(6):1471-8. Artículo interesante en el que se demuestra la apertura de nuevas colaterales para la irrigación medular tras la oclusión aguda de alguna rama. En base a esto surgirán nuevas técnicas para prevenir la paraplejia en la cirugía aórtica, como la embolización de arteria segmentarias. PubMed
4.- Linsler S1, Schmidtke M, Steudel WI, Kiefer M, Oertel J. Automated intracranial pressure-controlled cerebrospinal fluid external drainage with LiquoGuard. Acta Neurochir (Wien). 2013 Aug;155(8):1589-94; discussion 1594-5. doi: 10.1007/s00701-012-1562-3. Epub 2012 Nov 28. PubMed