Aliaño Piña, M. Arastey Aroca, S. Vélaz Dominguez S. Vázquez Vicente, B.
FEA Anestesiología y Reanimación. Complejo Hospitalario de Toledo.
Cómo citar este artículo: Aliaño Piña, M., & Arastey Aroca, S. (2016). Síndrome de hiperperfusión cerebral tras revascularización carotídea. Revista Electrónica AnestesiaR, 8(8), 1. https://doi.org/10.30445/rear.v8i8.123
Introducción
El síndrome de hiperperfusión cerebral (SHC) entraña una complicación poco frecuente pero devastadora de la revascularización carotídea, ya sea tras endarterectomía o stent carotídeo.
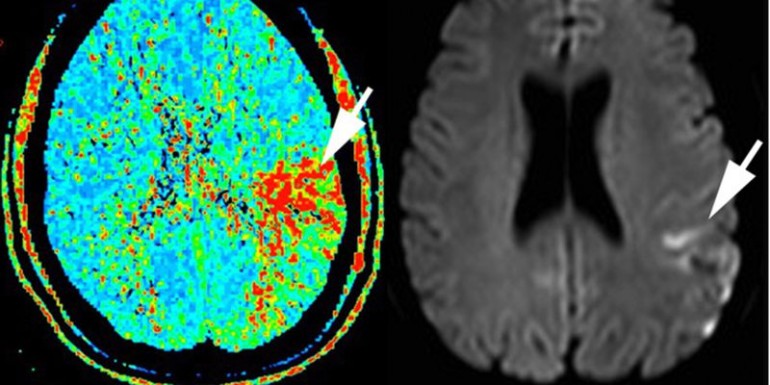
Esta entidad fue descrita por primera vez en 1981 por Sundt (1) como la combinación de hipertensión arterial con la triada clínica de cefalea de características migrañosa, convulsiones y síntomas neurológicos focales en ausencia de isquemia cerebral. Posteriormente, se han descrito como criterios diagnósticos el incremento del flujo sanguíneo cerebral (FSC) respecto a valores basales preoperatorios, la demostración de hiperperfusión mediante técnicas de neuroimagen (TAC o RM) y el debut en los 30 días post-revascularización carotídea. El SHC es más frecuente en pacientes con un aumento del FSC del 100%, aunque también ha sido descrito en otros con un aumento del FSC más modesto. Por ello, algunos autores sugieren la posibilidad de llamarlo síndrome de reperfusión cerebral en aras de reflejar el daño generado por la reperfusión.
La incidencia del SHC tras cirugía de revascularización carotídea se sitúa entre el 1-2,1% (2), variando notablemente según los trabajos consultados, probablemente debido a los criterios de inclusión y a la multiplicidad de definiciones. No contamos con clara evidencia para discernir si la revascularización mediante stent carotídeo se asocia a un mayor riesgo de SHC respecto a la endarterectomía, pero parece que los intervenidos mediante stent presentan más factores de riesgo.
Fisiopatología
La alteración de los mecanismos de autorregulación cerebrovascular junto con el aumento de la presión arterial sistólica postoperatoria son los dos mecanismos causantes del aumento del FSC. El FSC depende de la presión de perfusión cerebral, que es igual a la presión arterial media menos la suma de la presión intracraneal y la venosa.
En condiciones normales, la circulación cerebral se mantiene constante gracias a la autorregulación cerebral. El principal mecanismo de autorregulación es la reactividad arteriolar, que en respuesta a distintos factores como la variación del flujo sanguíneo o la hipercapnia produce vasoconstricción o vasodilatación.
En pacientes con una estenosis carotídea significativa la disminución del flujo produce una vasodilatación arteriolar compensatoria cuyo objetivo es mantener el FSC adecuado. Tras la revascularización existe un aumento del flujo sanguíneo y una falta de respuesta del sistema arteriolar que se encuentra exhausto. Esta alteración de los mecanismos de autorregulación representa el papel principal del SHC.
La causa del aumento de la presión arterial sistólica postoperatoria parece multifactorial, y afecta entre el 19 y el 64% de los pacientes (3). La pérdida del reflejo barorreceptor y la liberación de neuropéptidos vasoactivos pueden contribuir al incremento de la presión arterial. Tras la revascularización, el aumento de la presión arterial puede aumentar la presión de perfusión cerebral produciendo una hiperperfusión y edema intracraneal. El sustrato patológico del SHC es el edema en astrocitos precapilares e intersticiales especialmente en el territorio cerebrovascular.
Clínica
Los síntomas pueden aparecer hasta varias semanas después de la revascularización, siendo más frecuente la presentación en los primeros días postoperatorios. Los síntomas más frecuentes son el deterioro del nivel de conciencia 37%, la cefalea 30%, y las crisis epilépticas 25%. La hemorragia intracraneal ocurre en el 4.8% de los casos y es el evento más devastador.
Los factores de riesgo del SHC se pueden dividir en:
- Preoperatorios: edad avanzada, DM, HTA, endarterectomía contralateral reciente, oclusión carotídea contralateal, pobre circulación colateral, polígono de Willis incompleto.
- Perioperatorios: presión carotídea distal >40 mmHg., isquemia intraoperatoria, infarto cerebral, hiperperfusión cerebral postoperatoria refractaria.
- Postoperatorio: HTA, anticoagulantes, antiagregantes plaquetarios.
Diagnóstico
Es fundamental documentar la presencia de hiperperfusión y la ausencia de isquemia. El Doppler transcraneal es la herramienta más extendida para detectar cambios en el FSC, puesto que permite la identificación precoz del SHC. El predictor de SHC más frecuentemente utilizado es un aumento de la velocidad media >100% a los tres minutos del desclampaje carotídeo, con respecto a la velocidad media antes del camplaje (3).
La perfusión cerebral puede valorarse mediante PET, RM y SPECT. La oximetría con infrarrojos (NIRS) es útil para detectar la hiperperfusión, un aumento mayor del 24% a los tres minutos de la revascularización se asocia con SHC.
Moulakakis, Mylonas, Sfyroeras y Andrikopoulos (3) proponen el siguiente algoritmo diagnóstico:
Debemos tener en cuenta que en los casos de cirugía endovascular hay que hacer un diagnóstico diferencial con el síndrome de neurotoxicidad por contraste. Éste representa una entidad rara asociada a la exposición de contrastes angiográficos en relación con exposiciones prolongadas y a altas dosis. La hipertensión arterial crónica representa el factor de riesgo más importante, puesto que favorece la alteración de la autorregulación cerebral y de la barrera hematoencefálica, produciéndose la salida de contraste. La clínica aparece inmediatamente tras la administración del contraste, y consiste en convulsiones, ceguera cortical transitoria y déficit neurológico focal. Se resuelve en horas o días, y el TAC sin contraste es muy útil en el diagnóstico (hiperdensidad cortical difusa y ocupación de los surcos de la convexidad) (4).
Tratamiento
La prevención es crucial, y se lleva a cabo con el reconocimiento de los pacientes potencialmente en riesgo de padecer el SHC basándonos en la presencia de factores de riesgo. En aquellos pacientes con alta sospecha de SHC debemos realizar un diagnóstico y tratamiento apropiado lo más rápido posible.
Para la prevención del SCH se han propuesto como medidas más importantes el uso del Doppler transcraneal para el diagnóstico de hiperperfusión y la monitorización invasiva de la tensión arterial.
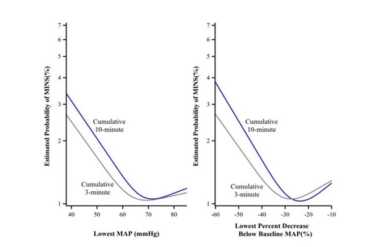
Se ha sugerido que las cifras de tensión arterial deben de mantenerse normales o ligeramente bajas (presión sistólica <120-140 mmHg.), aunque las guías no establecen valores diana. No debemos olvidar que se han descrito casos con TAS <160 mmHg., lo que refleja el papel de los mecanismos de autorregulación alterados (3,5).
En cuanto a la indicación de los fármacos antihipertensivos, no hay evidencia que apoye el uso de un fármaco determinado pero se desaconseja el uso de vasodilatadores (hidralacina, nitratos o calcio antagonistas), puesto que causan aumento del FSC e intensifican el edema cerebral. Por tanto, serían de elección aquellos antihipertensivos sin efecto sobre la circulación cerebral. Se ha propuesto la utilización de clonidina por su efecto simpaticolítico central (alfa 2 adrenérgico). El labetalol (antagonista alfa y beta) reduce la presión arterial sin efecto directo sobre la circulación cerebral, aunque debemos ser cuidadosos con los betabloqueantes porque potencian la bradicardia.
La edaravona, barredor de radicales libres de oxígeno, ha demostrado en algún estudio prevenir la incidencia de hiperperfusión tras la endarterectomía carotídea. Actúa inhibiendo la peroxidación lipídica y previene el daño endotelial disminuyendo el edema (60 mg. en 100 ml. de salino fisiológico 30 min. antes del camplaje carotídeo). También se ha sugerido que la profilaxis con dipiridamol puede prevenir el estrés oxidativo cerebral (3).
No hay evidencia para recomendar el uso de anticonvulsivantes de manera profiláctica, pero sí estarían indicados en la presencia de crisis convulsivas.
El tratamiento del edema cerebral que incluye una sedación adecuada, hiperventilación, manitol y salino hipertónico podría ser eficaz. Los corticoides y barbitúricos también han sido utilizados, pero su efectividad no está clara, si bien podrían estar indicados en caso de hiperperfusión grave para prevenir la hemorragia intracraneal.
Las guías clínicas más actualizadas aconsejan períodos de hospitalización cortos (24-48h.), por lo que se espera que haya casos de SHC que debuten en casa. Por este motivo, se debe explicar a los pacientes que deben volver al hospital ante la presencia de cefalea y se debe monitorizar la presión arterial durante la primera semana postoperatoria.
Bibliografía
- Sundt TM, Sandok BA, Whisnant JP. Carotid endarterectomy. Complications and preoperative assesment of risk. Mayo Clin Proc 1975;50:301-6. (PubMed)
- Hayashi K, Horie N, Suyama K, Nagata I. Incidence and clinical features of Symptomatic Cerebral Hyperperfusion Syndrome after Vascular Reconstruction. World Neurosurg. 2012 Nov;78(5):447-54. (PubMed) (PDF)
- Moulakis KG, Mylonas SN, Sfyroeras GS, Andrikopoulos V. Hyperperfusion síndrome after carotid revascularization. J Vasc Surg 2009;49:1060-8. (PubMed) (PDF)
- Potsi S, Chourmouzi D, Moumtzouoglou A, Nikiforari A, Gkouvas K, Drevelegas A. A transient contrast encephalopathy after carotid angiography mimiking diffuse subaracnoid hemorrage. Neurol. Sci 2012;33:445-8. (PubMed)
- S. Bouri S, Thapar A, Shalhoub J et al . Hypertension and the Post-carotid Endarterectomy Cerebral Hyperperfusion Syndrome. Eur J Vasc Endovasc Surg 2011;41:229-237. (PubMed) (PDF)