Montero Caballero S (1), Gómez Martínez ML (2), García Sáiz I (2)
(1) MIR Anestesiología y Reanimación. Hospital Universitario del Río Hortega, Valladolid.
(2) FEA Anestesiología y Reanimación. Hospital Universitario Río Hortega, Valladolid.
Cómo citar este artículo: Montero Caballero, S., Gómez Martínez, M. L., & García Sáiz, I. (2020). Anestesia intradural en la Enfermedad de Charcot-Marie-Tooth: A propósito de un caso. Revista Electrónica AnestesiaR, 12(9). https://doi.org/10.30445/rear.v12i9.777
Resumen
La neuropatía sensitivo-motora hereditaria, también conocida como Enfermedad de Charcot-Marie-Tooth, es una de las enfermedades hereditarias más frecuentes en nuestro país. Engloba un espectro de trastornos causados por mutaciones específicas en genes que codifican la mielina y que ocasionan defectos en su estructura, formación y mantenimiento.
Existe escasa evidencia clínica disponible en relación al uso de anestesia regional en pacientes con esta enfermedad, lo que pone de manifiesto la necesidad de documentar los casos en los que se hayan empleado técnicas de anestesia locorregional con el fin de establecer estrategias de actuación.
Introducción
La Neuropatía Sensitivo-Motora Hereditaria (Hereditary Motor Sensory Neuropathy, HMSN), también conocida como Enfermedad de Charcot-Marie-Tooth (ECMT) es una de las enfermedades hereditarias más frecuentes en nuestro país (1), afectando a 4 de cada 10.000 habitantes. Engloba un espectro de trastornos causados por mutaciones específicas en genes que codifican la mielina y que ocasionan defectos en su estructura, formación y mantenimiento. La ECMT se clasifica en siete tipos. La duplicación del gen PMP-22 causa la Enfermedad de Charcot-Marie-Tooth 1A (ECMT 1A), un trastorno desmielinizante de los nervios periféricos que constituye el tipo más común de esta enfermedad. (1)
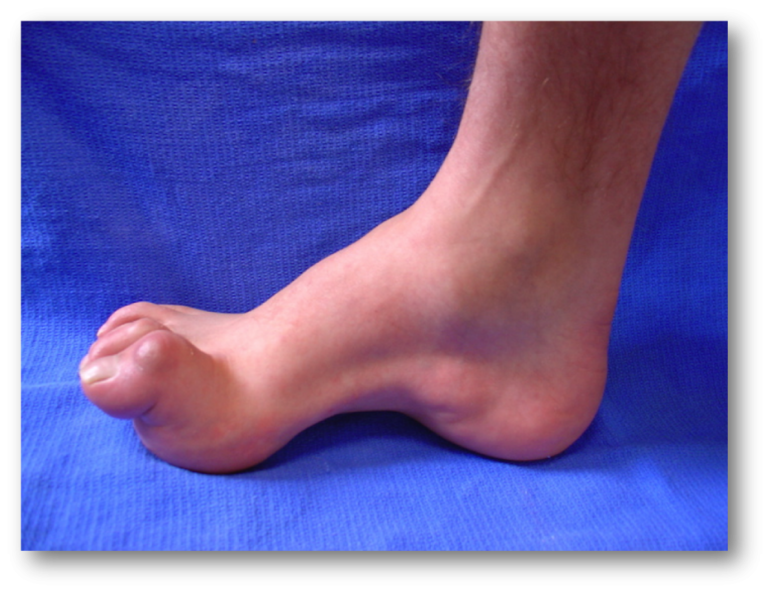
Las manifestaciones clínicas más tempranas suelen ser la debilidad muscular distal, con dificultad para correr, así como la pérdida de reflejos, desarrollo de pie cavo y dedos en martillo. La atrofia distal de los músculos gemelos ocasiona una deformidad “en pata de cigüeña”, con dificultad para caminar tanto por la debilidad muscular intrínseca como por la abolición progresiva de la sensibilidad propioceptiva y vibratoria. Manifestaciones más tardías incluyen atrofia muscular de extremidades y palpación del trayecto de nervios periféricos secundaria al desarrollo de hipertrofia nerviosa. También son frecuentes la cifosis y la escoliosis. Además, los pacientes con ECMT 1A suelen asociar apnea del sueño. (1)
Aunque su diagnóstico definitivo es genético, los estudios de conducción nerviosa pueden mostrar una disminución importante de la velocidad de conducción en nervios sensitivos y motores. No obstante, la correlación entre la electromiografía y los hallazgos clínicos es escasa. En microscopía electrónica, los “bulbos de cebolla” son un hallazgo característico que refleja ciclos repetidos de desmielinización-remielinización nerviosa. (1)
No existe tratamiento específico para la enfermedad, tan sólo medidas de soporte. Practicar ejercicio diario cuando comienzan a aparecer las primeras manifestaciones clínicas ayuda a prevenir el desarrollo de contracturas musculares, y el calzado ortopédico se suele utilizar para estabilización de la extremidad inferior. (1)
Descripción del caso
Presentamos el caso de una paciente de 72 años, sin alergias medicamentosas conocidas, diagnosticada de ECMT 1A y dislipemia, con intervenciones quirúrgicas previas de colesteatoma de oído izquierdo, histerectomía con anexectomía derecha, prótesis de ambas rodillas y recambio de rótula izquierda, todas ellas bajo anestesia general sin complicaciones perioperatorias.
La paciente refería síntomas de HMSN desde la infancia y era seguida por Neurología en nuestro hospital. Presentaba discapacidad progresiva para la marcha, con necesidad de apoyo y ortesis antiequino para caminar, así como arreflexia global, atrofia leve de la musculatura intrínseca de ambas manos y dorsiflexora de ambos pies con estepagge importante de la marcha, sin déficit sensitivo significativo.
Acude a consulta preoperatoria para corrección de prolapso de órganos pélvicos de compartimento anterior mediante implante de malla. Se realiza examen clínico exhaustivo y se revisan informes de diferentes especialidades. En la exploración física no se evidencian predictores de vía aérea difícil (clase II de la clasificación de Mallampati, distancia tiromentoniana mayor de 7 cm y distancia interincisiva mayor de 3 cm) ni Síndrome de Apnea-Hipopnea del Sueño (SAHS). Tampoco existen antecedentes de vía aérea difícil en anestesias generales previas. No se evidencian obesidad o cifoescoliosis, ni otros hallazgos sugestivos de dificultad técnica previsible de anestesia neuroaxial. Las pruebas complementarias preoperatorias no muestran alteraciones significativas. Se explican a la paciente los beneficios que existen en su caso derivados de la realización de anestesia regional respecto a la anestesia general, dado el carácter leve de afectación clínica y la ausencia de contraindicaciones absolutas, que entiende y acepta.
A su llegada a quirófano, se monitoriza a la paciente mediante electrocardiograma, pulsioximetría y presión arterial no invasiva. Posteriormente, se coloca a la paciente en posición de sedestación para realización de anestesia subaracnoidea a nivel L3-L4 con 13 mg de Bupivacaína Hiperbárica 0.5%, con punción única, atraumática, mediante una aguja espinal punta de lápiz 25 G Whitacre® (Vygon, Ecouen, Francia, Europa), alcanzando un nivel sensitivo final de T7. Se le administra oxígeno a través de gafas nasales con capnógrafo a 3 litros/minuto, se colocan colchón y manta térmica para garantizar la normotermia y se monitoriza su temperatura central mediante SpotOn® (3M™, Canadá, EEUU).
Durante todo el procedimiento, la paciente mantiene presiones arteriales medias > 70 mmHg con frecuencias cardíacas rítmicas entre 60-65 latidos/minuto y saturaciones arteriales de oxígeno en torno al 98%, con temperatura central mantenida de 36˚C. La intervención transcurre sin incidencias intraoperatorias y posteriormente es trasladada a la Unidad de Recuperación Post-Anestésica (URPA), donde recupera la movilidad y sensibilidad de miembros inferiores una hora y cuarenta minutos después de la realización de la técnica neuroaxial, sin déficits neurológicos sobreañadidos a los basales.
Un mes después de la intervención nos ponemos en contacto con la paciente con el fin de evaluar de manera indirecta un posible empeoramiento secundario de su función neuromuscular. Refiere ser capaz de realizar movimientos con ayuda y mantener posturas de forma similar a su estado previo.
Discusión
El empleo de anestesia y/o analgesia regionales en pacientes con enfermedades del sistema nervioso central y periférico ha sido evitado históricamente por presuponer una causa de empeoramiento neurológico derivado del uso de anestésicos locales.(2) Sin embargo, la literatura existente al respecto, limitada y con pequeñas series de casos, no ha constatado deterioro a este nivel en pacientes con ECMT, ni tampoco exacerbación de la enfermedad, con el uso de anestesia locorregional (ni en bloqueos nerviosos periféricos ni en bloqueos neuroaxiales). (1-4) Si bien en algunos casos se ha reportado prolongación del tiempo de bloqueo. (4, 5)
Es desconocido el mecanismo por el que la alteración axonal en pacientes con ECMT se puede ver afectada por exposición directa a los anestésicos locales. (4) No obstante, se asume que tienen mayor susceptibilidad a los mismos debido a disminución y, en algunos casos, ausencia de mielina. Por ello, existen una serie de recomendaciones encaminadas a disminuir el posible riesgo derivado de estas técnicas. Se aconseja, por ejemplo, minimizar la manipulación con aguja para evitar lesiones, uso de ecografía para facilitar la identificación nerviosa (apenas existe respuesta a la neuroestimulación) y empleo de la menor dosis y concentración posibles de estos agentes. (4)
Además, en pacientes con ECMT 1A suelen aparecer deformidades de columna que pueden dificultar la realización de técnicas neuroaxiales.
En el caso de anestesia general, la ECMT se asocia con alteraciones clínicas específicas que condicionan el manejo anestésico.La prolongación de la conducción del nervio frénico, la disfunción diafragmática y las deformidades de columna ya comentadas, contribuyen al desarrollo de una alteración pulmonar restrictiva que puede progresar hasta fracaso respiratorio. (6) Se ha postulado que la presencia de debilidad muscular proximal de miembros superiores podría emplearse como predictor de debilidad de musculatura respiratoria. (7) Asimismo, es frecuente la asociación de dicha enfermedad con el SAHS y con la disfunción de cuerdas vocales secundaria a la afectación del nervio vago y sus ramas laríngeas, que puede progresar a una disfunción bilateral con aumento del riesgo de aspiración, o simular asma. (6)
En cuanto al uso de bloqueantes neuromusculares, se debe tener en cuenta que estos pacientes tienen denervación crónica, uno de los principales factores predisponentes para la liberación de potasio tras su exposición a la succinilcolina. (5, 7) Aunque se han descrito casos con síntomas crónicos en los que se ha empleado sin incidencias, cualquier exacerbación aguda de la ECMT puede alterar la cantidad de músculo afecto y, por lo tanto, variar la sensibilidad a la succinilcolina (8) con alta probabilidad de respuesta adversa. Por otro lado, el empleo de bloqueantes musculares no despolarizantes podría prolongar el bloqueo por la pérdida de unidades motoras, aunque existe evidencia de respuesta normal a estos fármacos. (5, 7) Deben emplearse con cautela, valorando cuidadosamente el grado de afectación clínica del paciente en el momento de la intervención.
También ha sido descrita una posible asociación entre la ECMT y la hipertermia maligna, aunque sin clara evidencia sobre la misma. (8) De hecho, en algún caso se han empleado agentes desencadenantes (5, 7) sin evidenciar aparición de este síndrome. Se recomienda, no obstante, la monitorización intraoperatoriade la temperatura.
Conclusiones
Existe cierta controversia a la hora de decidir la técnica anestésica más apropiada para pacientes con ECMT. La escasa evidencia clínica disponible en relación a la realización de procedimientos neuroaxiales en estos pacientes pone de manifiesto la necesidad de documentar los casos en los que se hayan empleado estas técnicas, con el fin de establecer estrategias de actuación.
Una exhaustivarevisión clínica de sus antecedentes, así como una correcta exploración clínica y anamnesis en la consulta preoperatoria serán muy útiles a la hora de valorar el potencial beneficio derivado del empleo de anestesia general o regional de manera individualizada.
Recomendamos realizar una estrecha vigilancia postoperatoria en URPA y al alta, para asegurar el correcto restablecimiento de la función neuromuscular. Además, consideramos positivo realizar un seguimiento a largo plazo de estos pacientes para garantizar que no se haya acrecentado el déficit neurológico tras la realización de técnicas locorregionales.
Bibliografía
- Cruse RP. Hereditary primary motor sensory neuropathies, including Charcot-Marie-Tooth disease. [Monografía en Internet]. Walthman (MA): UpToDate; 2016 [acceso abril de 2017]. Disponible en: http://www.uptodate.com/
- Fernández AB, Quesada C, Rodríguez O, Besada JC. Charcot-Marie-Tooth y analgesia epidural obstétrica, una opción segura. Rev Esp Anestesiol Reanim. 2011; 58: 254-63.
- Miller C, Yacsich M, Valenzuela P, Jans J. Manejo anestésico en enfermedad de Charcot-Marie-Tooth. A propósito de un caso. Rev Chil Anestesia. 2006; 35: 187-90. (HTML)
- McSwain JR, Doty JW, Wilson SH. Regional anesthesia in patients with pre-existing neurologic disease. Curr Opin Anesthesiol. 2014; 27: 538-43. (PubMed)
- Vallés J, Martínez-Ubieto J, Colás A, Abengoechea JM. Anestesia general con mascarilla laríngea en paciente con enfermedad de Charcot-Marie-Tooth de larga evolución. Rev Esp Anestesiol Reanim. 2009; 56: 194-5.
- Aboussouan LS, Lewis RA, Shy ME. Disorders of pulmonary function, sleep, and the upper airway in Charcot-Marie-Tooth disease. Lung. 2007; 185: 1-7. (PubMed)
- Antognini JF. Anaesthesia for Charcot-Marie-Tooth disease: a review of 86 cases. Can J Anesth. 1992; 39: 398-400. (PubMed)
- Soto D, Bermejo MA, Rubio P, García MJ. Consideraciones anestésicas en la enfermedad de Charcot-Marie-Tooth. Rev Esp Anestesiol Reanim. 2011; 58: 254-63.