Díaz Campanero P (1), Pretus Rubio S (1), Morales Cayuela MA (2), Mariscal Flores ML (3)
(1) FEA del Servicio de Anestesiología y Reanimación del Hospital Universitario de Getafe. Madrid. España.
(2) FEA del Servicio de Anestesiología y Reanimación del Hospital Universitario de La Princesa. Madrid. España.
(3) Jefa de Sección del Servicio Anestesiología y Reanimación del Hospital Universitario de Getafe. Madrid. España.
Cómo citar este artículo: Díaz Campanero, P., Pretus Rubio, S., Morales Cayuela, M. A., & Mariscal Flores, M. L. . (2022). Actualización en náuseas y vómitos postoperatorios. Revista Electrónica AnestesiaR, 14(3). https://doi.org/10.30445/rear.v14i3.1069
Introducción
Las náuseas y los vómitos postoperatorios (NVPO), complicaciones tan antiguas como la propia historia de la anestesia, constituyen aún a día de hoy un problema significativo y pendiente de resolver. Se ha estimado que afectan en torno al 30% de los pacientes quirúrgicos. Su incidencia llega a elevarse hasta el 80% en el caso de aquellos pacientes con factores de riesgo que no reciben una adecuada profilaxis antiemética. Frente al creciente desarrollo y éxito de la cirugía ambulatoria y de los programas ERAS (Enhanced Recovery After Surgery), las NVPO suponen un freno para los procesos de recuperación y un incremento en los costes hospitalarios asociados, además de una notable pérdida de la calidad asistencial percibida de manera subjetiva por parte de los usuarios del sistema de salud (1).
Por este motivo, durante los últimos años se ha observado un renovado interés en la elaboración de mejores protocolos de profilaxis y de tratamiento de las NVPO, así como en la implementación de métodos más fiables para estratificar el riesgo de los pacientes. A día de hoy, la clave del éxito parece residir en el empleo de abordajes multimodales, basados en el empleo simultáneo de varios fármacos pertenecientes a familias distintas. Además, se ha continuado la investigación y el desarrollo de nuevos fármacos antieméticos con una mayor eficacia y un mejor perfil de efectos secundarios, así como el estudio de las causas genéticas y fisiopatológicas subyacentes al problema de las NVPO. A lo largo de los siguientes apartados se lleva a cabo una revisión narrativa acerca de las últimas actualizaciones en el conocimiento y manejo de dichas complicaciones, tan frecuentes como inoportunas. Toda la bibliografía empleada puede consultarse a través del ejemplar de Diciembre de 2020 de la revista Best Practice & Research Clinical Anaesthesiology. Las tablas y figuras empleadas han sido modificadas a partir de la bibliografía original.
Desarrollo
Carga económica y asistencial que suponen las náuseas y los vómitos postoperatorios
Algunos estudios llevados a cabo durante los últimos años han permitido comparar los costes de una profilaxis generalizada de las NVPO frente al tratamiento “reactivo” de aquellos pacientes ya sintomáticos. Desde el punto de vista económico, los resultados favorecen significativamente el tratamiento profiláctico de todos los pacientes. En algunos casos la reducción de costes estimada supone en torno al 50%. Gran parte de los citados estudios se llevaron a cabo en el periodo previo a la comercialización de preparados genéricos para medicamentos como el Ondansetron, lo cual hace suponer que la reducción actual de costes podría ser aún más notable (2).
Gran parte del incremento en los costes asociado a los episodios de NVPO deriva del tiempo adicional de ingreso en Unidades de Reanimación Postanestésica, con la inversión de recursos materiales y humanos que ello supone. Los reingresos a causa de las NVPO también suponen otra fuente importante de gasto sanitario, y además causan la ocupación de un espacio y unos recursos que no se encuentran disponibles temporalmente para otros pacientes.
Desde el punto de vista de la calidad de vida percibida subjetivamente durante el proceso de recuperación, hasta el 94% de los pacientes que no sufrieron NVPO reportaron datos positivos al ser encuestados, mientras que dicho porcentaje se redujo a un 49% en aquellos que sufrieron esta clase de complicaciones (2).
Por último, merece la pena destacar que el coste total de prescribir opioides durante el periodo postoperatorio puede llegar a reducirse prácticamente a un tercio cuando se prescriben antieméticos de manera simultánea. Lamentablemente, una revisión reciente desveló que dicha combinación de prescripciones se lleva a cabo únicamente en un 10% de los casos (2).
Fisiopatología y factores de riesgo de las náuseas y los vómitos postoperatorios
Los factores etiológicos de las náuseas y los vómitos son múltiples: infecciones, trastornos gastrointestinales, patología intracraneal, hipotensión, afecciones vestibulares o laberínticas, embarazo, desequilibrios metabólicos, ansiedad, dolor o exposición a sustancias emetógenas. Existen numerosas áreas a nivel del sistema nervioso central (SNC) capaces de reaccionar a estímulos procedentes de vías neurales periféricas: el centro del vómito, el área postrema, la zona gatillo quimiorreceptora, el núcleo del tracto solitario (NTS), el cerebelo o el cuarto ventrículo. El sistema vestibular también se relaciona con la posible alteración del equilibrio y desarrollo de cinetosis por parte de los pacientes. El nervio vago juega un importante papel a la hora de transmitir hasta estos centros la estimulación generada a nivel visceral. Por último, en lo que se refiere a la neurotransmisión de todas estas señales, existe una amplia diversidad de receptores implicados: opioides (Mu), dopaminérgicos (D2), de sustancia P (NK1), serotoninérgicos (5-HT3), colinérgicos muscarínicos (M1) e histaminérgicos.
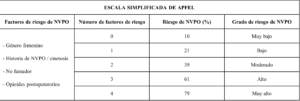
En lo que se refiere a la administración de cuidados anestésicos, existen diversos factores emetógenos a tener en cuenta. A nivel clínico, la escala de Apfel (tabla 1) constituye la principal herramienta validada para predecir la futura aparición de NVPO. En primer lugar, los opioides aumentan considerablemente la incidencia de NVPO por sus efectos a nivel central y visceral. Actúan sobre el área postrema, NTS, tronco cerebral, zona gatillo quimiorreceptora y sistema vestibular, entre otros. Además, afectan de manera directa la mecánica gastrointestinal. Todo ello puede desembocar de manera directa o indirecta en la génesis de NVPO. Por otro lado, los anestésicos inhalados como sevoflurano, isoflurano o desflurano también generan NVPO mediante la estimulación del área postrema, NTS y aferentes vagales.
El tiempo quirúrgico tiene una correlación directa con la exposición a agentes anestésicos. Por esta causa, es un factor más a tener en consideración para la posible génesis de NVPO, cuya incidencia podría aumentar desde un 2.8% para procedimientos menores de 30 minutos hasta un 27.7% en aquellos de duración superior a 3 horas. La evidencia disponible en la actualidad demuestra que el empleo de anestesia regional junto a la anestesia total intravenosa (TIVA), eliminando el uso de anestésicos volátiles, reduce de manera eficaz la aparición de NVPO (3).
Por otro lado, la administración de una anestesia espinal o epidural genera hipotensión a causa del bloqueo simpático consiguiente. Dicha hipotensión puede dar origen a náuseas y vómitos por disminución del flujo sanguíneo en los centros del vómito del SNC. En general, cualquier episodio de hipotensión (independientemente de la etiología del mismo), ya sea en quirófano o en las áreas de recuperación anestésica, puede potencialmente provocar náuseas y vómitos por medio de la vía comentada anteriormente. La reposición adecuada del volumen intravascular de los pacientes y la administración oportuna de vasopresores contribuyen de manera efectiva a la prevención y tratamiento de estos episodios de hipotensión, disminuyendo con ello la incidencia de NVPO asociados.
Diversos procedimientos quirúrgicos se han vinculado tradicionalmente con la aparición de náuseas y vómitos en el periodo postoperatorio. Estos incluyen cirugías de la vía aérea superior, nasales, orales, faríngeas o gastroesofágicas, en las cuales puede tragarse sangre o producirse un sangrado en el propio tracto gastrointestinal. También las técnicas laparoscópicas con insuflación intensa del abdomen o las cirugías en posición de Trendelemburg prolongada pueden producir un aumento de la presión intraabdominal que fomente el desarrollo de NVPO. En la población pediátrica, las cirugías del estrabismo o las amigdalectomías resultan especialmente emetógenas.
En la tabla 2 se presentan los principales factores de riesgo conocidos, divididos en tres categorías: aquellos relacionados con el propio paciente, con el cuidado anestésico proporcionado y con el procedimiento quirúrgico practicado.

Por último, existen algunos factores genéticos capaces de condicionar la incidencia y gravedad de las NVPO. Dichos factores se relacionan con la susceptibilidad individual a este tipo de complicaciones y con la efectividad que un determinado tratamiento farmacológico pueda tener en un paciente concreto. Algunos cambios en determinados receptores moleculares o en el metabolismo de los agentes antieméticos pueden resultar en respuestas interindividuales variables. Todo ello se aborda más adelante, en el apartado “implicación de la genética en la génesis y manejo de las náuseas y vómitos postoperatorios”.
¿Cuál es la combinación ideal de antieméticos?
A pesar de la extensa evidencia existente, que describe el empleo de múltiples y muy variados protocolos de profilaxis antiemética, la combinación ideal de fármacos está aún por definir. A lo largo de las últimas décadas han sido empleadas muy diversas familias de fármacos antieméticos. La tabla 3 recoge la dosificación, pauta de administración y principales efectos secundarios de aquellos que se utilizan con más frecuencia.

Actualmente se recomienda la aplicación de un abordaje multimodal en la profilaxis de las NVPO, con administración de dos o más fármacos de familias distintas en aquellos pacientes con factores de riesgo. Dicho enfoque se ha demostrado significativamente superior a la monoterapia. Sin embargo, por el momento no se dispone de ningún fármaco o combinación de fármacos capaz de prevenir por completo la aparición de NVPO, especialmente en individuos de alto riesgo. Los regímenes más estudiados han sido aquellos que combinan un antagonista del receptor de serotonina 5-HT3 con dexametasona o antagonistas del receptor de dopamina (droperidol). Sin embargo, el empleo de este último se ha visto limitado a causa de una razonada preocupación por aparición de arritmias (prolongación del intervalo QT). Por tanto, la combinación más segura y más estudiada continúa siendo la de ondansetron 4mg con dexametasona. A lo largo de los últimos años, muchas otras combinaciones se han empleado, especialmente ante la necesidad de añadir un tercer antiemético en aquellos casos de especial riesgo. Así, podemos citar ejemplos como: ondansetron + dexametasona + aprepitant u ondansetron + dexametasona + haloperidol. En cuanto a la dosis de dexametasona recomendada, algunos trabajos han señalado que la dosis de 4-5mg de dexametasona posee una eficacia similar a la de 8-10mg a la hora de prevenir las NVPO (4).
¿Estrategias basadas en el riesgo o abordaje multimodal para todos?
Una vez establecida una estratificación del riesgo para el desarrollo de NVPOalgunos algoritmos tradicionales recomendaban el empleo preventivo de antieméticos únicamente en aquellos pacientes de riesgo moderado o alto. Sin embargo, análisis posteriores han demostrado que dicho enfoque a menudo se vinculaba con la administración de una profilaxis insuficiente. Esto podría deberse a varios motivos. Por un lado, la aplicación de una estratificación del riesgo puede estar sujeta a errores de interpretación y confusiones. Por otro, se ha demostrado que aquellos pacientes considerados de riesgo bajo pueden presentar una variabilidad interindividual que escape de una clasificación ordinaria del riesgo de NVPO, como es el caso de la predisposición genética. Esto podría privar de un tratamiento preventivo a pacientes que indudablemente se beneficiarían del mismo. El bajo perfil de riesgo de los tratamientos de profilaxis antiemética es, por último, un dato más a favor de su aplicación más generalizada. En los últimos años se ha comenzado a abogar por un enfoque más liberal del problema de las NVPO, con la realización de una mínima prevención en todos los pacientes quirúrgicos, y con especial refuerzo para aquellos con presencia de uno o más factores de riesgo. Un ejemplo de este tipo de enfoque sería el esquema propuesto en la tabla 4, según el cual incluso los pacientes considerados de bajo riesgo se beneficiarían, por lo menos, de 2 intervenciones de profilaxis antiemética (5).

Manejo de las náuseas y los vómitos postoperatorios en el contexto de un programa ERAS
Con el desarrollo de los programas ERAS (Enhanced Recovery After Surgery), desde el inicio del presente siglo, se atribuye una importancia cada vez mayor a la recuperación funcional del enfermo y a la implementación de los mejores estándares de calidad a través de todo el proceso quirúrgico. Todo ello sitúa a los protocolos de profilaxis antiemética como un pilar más para el sustento de una recuperación optimizada, a causa de su demostrada influencia sobre el curso del periodo postoperatorio.
La interrelación entre la aplicación de programas ERAS y la reducción de las NVPO queda patente cuando se enumeran todas las prácticas asociadas a estos primeros que tienen una repercusión sobre la incidencia de éstas últimas: la minimización del ayuno preoperatorio, la carga preoperatoria con carbohidratos, el empleo de técnicas mínimamente invasivas, la utilización de protocolos de TIVA (Total Intravenous Anesthesia), la aplicación de programas de analgesia multimodal y técnicas de anestesia regional, el mantenimiento de la euvolemia y la fluidoterapia guiada por objetivos, la evitación del sondaje nasogástrico rutinario o la prevención multimodal del íleo postoperatorio.
En lo que respecta a los programas ERAS subespecíficos, la cirugía colónica electiva fue pionera en la implementación de los mismos. Dichas guías clínicas recomiendan la aplicación de un régimen multimodal para la prevención de NVPO en aquellos pacientes con 2 o más factores de riesgo conocidos. Si las NVPO ocurrieran, sugieren el manejo de las mismas con un nuevo agente terapéutico de una familia distinta a las previamente empleadas. En estos mismos textos se subraya la conveniencia de aplicar una analgesia multimodal con ahorro de opioides, con el paracetamol como elemento central de la estrategia analgésica. En cuanto a la posible aplicación de anestesia regional, se sugiere el empleo de un catéter epidural para aquellos procedimientos que impliquen una laparotomía y una anestesia espinal con una pequeña dosis de morfina para procedimientos de carácter laparoscópico. Por otra parte se aboga por una fluidoterapia guiada por objetivos que, entre otros resultados positivos, también contribuye a reducir la incidencia de NVPO. Además existe una recomendación fuerte para el empleo de chicle y Alvimopan en la profilaxis contra el íleo postoperatorio. El Alvimopam es un antagonista de los receptores mu-opioides con potencial para acelerar la recuperación gastrointestinal, incluyendo una reducción en las NVPO, especialmente para aquellos pacientes que reciban una analgesia basada en opioides. Sin embargo, su empleo se ha vinculado a efectos secundarios potencialmente graves y, por tanto, su utilización permanece restringida. Por último, dichas guías clínicas mencionan el posible papel de la minimización del ayuno preoperatorio y la carga preoperatoria con carbohidratos, así como la adecuada hidratación, en la reducción de complicaciones perioperatorias como las NVPO, entre otras (6).
El catéter epidural también se recomienda como método analgésico principal para las cirugías rectales abiertas en los protocolos ERAS correspondientes, debido a una eficacia más modesta de los catéteres incisionales y de los bloqueos de pared abdominal. De manera similar a las guías previamente mencionadas para cirugía colónica, se recomienda una carga preoperatoria de carbohidratos en todos los pacientes no diabéticos, con el objetivo de reducir la incidencia de complicaciones postoperatorias como náuseas, vómitos, dolor, diarrea o mareo. Finalmente, se desaconseja el sondaje nasogástrico rutinario para una recuperación más precoz de la función intestinal y una menor incidencia de neumonía postoperatoria (6).
Las guías clínicas para la aplicación de protocolos ERAS en cirugía hepática subrayan la importancia de la profilaxis multimodal de las NVPO, destacando de manera especial el papel de la dexametasona como adyuvante. Más allá de su efecto antiemético, la dexametasona en dosis bajas podría favorecer los procesos de regeneración hepática. En cuanto a la aplicación de anestesia regional, se advierte contra la colocación rutinaria de un catéter epidural por el potencial riesgo de coagulopatías postoperatorias que pospongan o compliquen la retirada del catéter, y también por el posible desarrollo de una lesión renal aguda en respuesta a la hipotensión inducida por el bloqueo epidural. Los opioides intratecales y los catéteres incisionales sí podrían servir como alternativas analgésicas en dicho contexto. Por otro lado, la fluidoterapia dirigida por objetivos podría resultar beneficiosa en el periodo posterior a la hepatectomía, sin embargo hasta completar la misma se prefiere el mantenimiento de una presión venosa central baja (<5cmH2O) para prevenir el sangrado (6).
En cuanto a la pancreatoduodenectomía, sus guías específicas siguen las líneas generales de la cirugía colorrectal, aunque con una mención especial al papel de la anestesia total intravenosa (TIVA) frente a los anestésicos volátiles en el tratamiento de los pacientes de alto riesgo de NVPO. Dichas guías, al igual que algunas de las anteriores, mencionan el controvertido potencial de los corticoides a la hora de favorecer la dehiscencia de suturas. Sin embargo, la evidencia es muy controvertida al respecto y, a día de hoy, no existen motivos sustanciales para abogar en contra de su empleo (6).
Según los protocolos específicos para la cirugía bariátrica, el empleo de corticoides (8mg de dexametasona, concretamente) se recomienda como intervención independiente a la hora de mitigar el estrés fisiológico perioperatorio y, de manera secundaria, prevenir las NVPO. Se sugiere asimismo la utilización de la TIVA para reducir dichas complicaciones. En lo que respecta a la analgesia, los protocolos de analgesia multimodal con ahorro parcial o completo de opioides se encuentran ampliamente avalados por la bibliografía existente (6).
Para los pacientes intervenidos de gastrectomía, en caso de acumular al menos tres factores de riesgo de NVPO, las guías actuales recomiendan el empleo de protocolos de anestesia TIVA, la administración de dexametasona en dosis de 4-8mg y la administración también de un antagonista 5-HT3 o de droperidol. En cuanto a la analgesia, cabe destacar la mención que se hace de las infusiones de lidocaína a la hora de disminuir los requerimientos de opioides y la incidencia de NVPO (6).
Los programas ERAS para cirugía urológica se han centrado fundamentalmente en la cistectomía radical y recomiendan la anestesia epidural torácica como parte de un régimen analgésico multimodal. De igual manera, mencionan la validez de alternativas como las infusiones de lidocaína, los bloqueos de pared abdominal o los catéteres incisionales. También resaltan la importancia de las técnicas quirúrgicas mínimamente invasivas, además del empleo de chicle y Alvimopan, para prevenir el íleo postoperatorio (6).
Las guías específicas para la cirugía mayor de cabeza y cuello recomiendan el empleo de un corticoide asociado a otro antiemético como profilaxis de primera línea para las NVPO. En muchas de estas cirugías los vómitos constituyen una complicación potencialmente desastrosa para la viabilidad de los colgajos practicados. Por otra parte, para la cirugía de mama, las guías destacan la utilización de antagonistas 5-HT3 y regímenes TIVA para la prevención de NVPO. Además mencionan el papel fundamental de los antiinflamatorios no esteroideos (AINES) como parte de un plan analgésico multimodal, sin haberse detectado riesgos adicionales asociados a su empleo (6).
En resumen, el surgimiento de los programas ERAS ha dado lugar a un nuevo contexto para la prevención de NVPO, poniendo énfasis en el origen multifactorial de este tipo de complicaciones, así como sucede con la disfunción gastrointestinal postoperatoria. Muchos de los componentes de los programas ERAS actúan de manera indirecta sobre la incidencia de NVPO, y esto sucede por el enfoque colectivo hacia la reducción del dolor y con ello, la reducción del consumo de opioides en el curso perioperatorio. Por otro lado, el éxito en la prevención de NVPO conlleva un mejor retorno de la actividad fisiológica normal del individuo (menor disfunción visceral) y, con ello, una incorporación más precoz a sus actividades habituales. Todos estos factores convierten la prevención de las NVPO en parte central e ineludible de cualquier programa ERAS para la optimización del proceso quirúrgico.
Manejo óptimo de las náuseas y vómitos asociados a la cesárea
Hasta el 80% de las pacientes sometidas a una operación cesárea bajo anestesia neuroaxial sufren náuseas o vómitos durante el periodo intraoperatorio o el postoperatorio (7). Se trata de una amplia población en riesgo de sufrir eventos adversos asociados a dichas complicaciones. En lo que se refiere al periodo intraoperatorio, concurren diversos factores de riesgo asociados al cuidado anestésico (hipotensión inducida por la propia anestesia o administración de opioides, uterotónicos y antibióticos intravenosos) con otros factores de tipo quirúrgico (estimulación visceral, exteriorización del útero o irrigación peritoneal).
Un 75% de las pacientes que reciben anestesia espinal para la cirugía de cesárea desarrollan hipotensión intraoperatoria (7). La isquemia resultante a nivel del tronco cerebral produce la activación del centro del vómito. Además, la reducción del flujo sanguíneo esplácnico induce la liberación de diversas moléculas emetógenas desde el tracto gastrointestinal, como es el caso de la serotonina. La evitación de la hipotensión materna reduce de manera significativa la incidencia de náuseas y vómitos.
La fenilefrina se considera actualmente como el agente de primera línea para el manejo de los cuadros de hipotensión vinculados a la anestesia espinal, ya que su empleo se asocia a una menor incidencia de náuseas y vómitos intraoperatorios (NVIO) y un mejor perfil del equilibrio ácido-base neonatal en comparación con la efedrina. Las guías de consenso más recientes recomiendan comenzar una infusión de fenilefrina profiláctica inmediatamente tras depositar el anestésico espinal, comenzando con una dosificación de 25-50μg/min y titulando la dosis para mantener un objetivo de presión arterial sistólica por encima del 90% de la basal (7). La administración simultánea de cristaloides o coloides tiene el potencial de disminuir los episodios de hipotensión y los requerimientos de fenilefrina, mientras que la precarga con cristaloides se ha demostrado inefectiva para prevenir la hipotensión y no se recomienda (7). Por último, el desplazamiento uterino izquierdo se utiliza de rutina para minimizar la compresión de la vena cava inferior.
Para el control del dolor, se ha demostrado que la administración neuroaxial de opioides lipofílicos como fentanilo o sufentanilo mejora la calidad del bloqueo y reduce las NVIO. Particularmente, la adición de fentanilo intratecal reduce hasta un 82% la necesidad de suplementación analgésica y un 59% las NVIO. La dosis recomendada de fentanilo intratecal es de 10-15μg, mientras que por vía epidural es de 50μg (7).
Entre los agentes uterotónicos actualmente empleados, la ergonovina es el más emetógeno a causa de su interacción con receptores dopaminérgicos, serotoninérgicos y α–adrenérgicos. La oxitocina y la carbetocina también pueden producir NVIO debido a su efecto hipotensor, lo cual puede minimizarse mediante una administración lenta de la mínima dosis efectiva. Finalmente, algunos antibióticos comúnmente utilizados, como la cefazolina, se han asociado también a la producción de NVIO y por ello se recomienda asimismo su administración lenta.
En cuanto al estímulo quirúrgico, se conoce que la exteriorización del útero y la irrigación intraabdominal con suero salino producen un significativo aumento en la incidencia de NVIO por medio de la estimulación de fibras vagales y fibras C viscerales. Por este motivo se recomienda una adecuada técnica quirúrgica, que minimice la manipulación visceral en la medida de lo posible.
Durante el postoperatorio, las náuseas y los vómitos son fundamentalmente estimulados por el efecto emetógeno de los opioides y del dolor severo. Actualmente se recomienda un abordaje multimodal del dolor, con un enfoque orientado hacia el ahorro de opioides. En este sentido, el empleo de la morfina a nivel neuroaxial goza también de popularidad, con una dosis intratecal óptima de 100μg y de 3-4mg por vía epidural. La disyuntiva entre empleo de morfina o fentanilo neuroaxiales deriva fundamentalmente de la lentitud de la primera a la hora de establecer su efecto, lo cual potencialmente puede producir una analgesia inicialmente insuficiente y NVIO. Sin embargo, su efecto mantenido durante el postoperatorio deriva en una menor administración de opioides intravenosos y por tanto un mejor resultado durante dicho periodo. Por otro lado, las pautas de paracetamol en combinación con AINES disminuyen significativamente el empleo de opioides y se asocian a una reducción de las NVPO. En cuanto a los bloqueos de la pared abdominal, como es el caso del bloqueo TAP (Transversus Abdominal Plane Block), cuentan aún con un nivel de evidencia limitado en lo que se refiere a la reducción de NVPO. A pesar de ello, su papel como rescate analgésico, especialmente en pacientes sometidas a anestesia general, sí que resulta de gran interés (7).
En cuanto a la medicación antiemética empleada en la población obstétrica, conviene destacar algunas particularidades. Como antagonista serotoninérgico, el ondansetron ha sido ampliamente utilizado para tratar las náuseas asociadas al embarazo. No se han detectado efectos adversos fetales asociados. La pauta más habitual es de 4mg, no habiéndose demostrado mejores resultados con el incremento de las dosis profilácticas. Reduce de manera significativa la incidencia de náuseas y vómitos durante los periodos intraoperatorio y postoperatorio. Además, se ha demostrado efectivo en el tratamiento del prurito secundario a la administración intratecal o epidural de opioides. No debe olvidarse su posible asociación con la prolongación del intervalo QT (7, 8).
En lo que se refiere a los corticosteroides, la dexametasona en dosis desde 2.5 hasta 10mg ha demostrado reducir de manera significativa las NVPO. El tardío establecimiento de su efecto antiemético (2h) convierte la dexametasona en un fármaco apropiado para reducir la incidencia de NVPO, especialmente en pacientes que hayan recibido opioides neuroaxiales de larga duración, como la morfina. No se ha demostrado la asociación de su administración con retraso en la cicatrización de la herida quirúrgica, ni con el incremento de las infecciones de la misma. Sí que debería contemplarse el posible desarrollo de hiperglucemia, especialmente en pacientes susceptibles. Las últimas guías de consenso recomiendan una dosis única de 8mg (7).
Entre los antagonistas dopaminérgicos, la metoclopramida se ha mostrado efectiva a la hora de reducir la incidencia de NVIO y NVPO, ya sea por sí sola o en combinación con otros antieméticos como ondansetron. A pesar de su capacidad para atravesar la barrera placentaria y secretarse con la lecha materna, su utilización no se ha vinculado con efectos adversos fetales o neonatales. Del droperidol cabe destacar su asociación con el riesgo de prolongación del intervalo QT y desarrollo de torsión de puntas, lo cual provocó la emisión de una alerta (blackbox warning) por parte de la FDA en el año 2001. Por último, la eficacia y seguridad de la amisulprida en la población obstétrica no ha sido aún evaluada (7).
Antihistamínicos como la difenhidramina o el dimenhidrinato se han empleado de manera segura durante el embarazo. Este último puede utilizarse en dosis de 25-50mg. En lo que se refiere a los anticolinérgicos, los parches de escopolamina de 1,5mg se han mostrado eficaces a la hora de reducir la incidencia de NVPO tras la cirugía de cesárea. Además el efecto de estos puede prolongarse hasta 24h. Entre sus efectos secundarios más frecuentes se encuentra la visión borrosa o la xerostomía. Finalmente, no existen estudios aún que hayan valorado la eficacia y seguridad de aprepitant (antagonista del receptor NK1) en la población obstétrica (7).
En cuanto al régimen farmacológico más apropiado, al igual que sucede con la población no obstétrica, actualmente se aboga por el empleo de una terapia antiemética multimodal. Esto se traduce en combinar distintos agentes, actuando en receptores diversos, especialmente en aquellos pacientes de mayor riesgo. A causa de las características que ya se han comentado, la población obstétrica sometida a intervención cesárea acumula múltiples factores de riesgo emético. Por ello, sería razonable emplear en este contexto una combinación farmacológica de 2-3 agentes. Se precisa mayor investigación en este campo para establecer cuál es la combinación de mayor eficacia y seguridad. Por el momento, el empleo de un antagonista serotoninérgico junto con dexametasona parece una opción razonable. La adición de metoclopramida podría reforzar aún más la eficacia de dicho tratamiento. Como ejemplo de práctica clínica, podríamos administrar durante el intraoperatorio metoclopramida 10mg (reducción de NVIO) y ondansetron 4mg (reducción de NVIO/NVPO), así como dexametasona 8mg (reducción de NVPO) (7).
Ya en el periodo postoperatorio, los antagonistas serotoninérgicos se recomiendan como la primera opción a administrar en aquellas pacientes que padezcan NVPO y no recibieran profilaxis previa. En aquellas que sí la hubieran recibido, se recomienda el tratamiento con un agente de una familia distinta al previamente empleado. Una vez han transcurrido más de 6h desde la administración de la profilaxis antiemética hasta el momento en el que se manifiestan las NVPO, sí que resulta razonable la repetición de los mismos agentes en caso de necesidad. En este contexto, se desaconseja utilizar fármacos con una demora considerable en el inicio de acción, como la dexametasona o la escopolamina. En casos refractarios, bajas dosis de naloxona o propofol (20mg) se han demostrado útiles. También se han empleado con eficacia inhalaciones de alcohol isopropílico (7).
Manejo de las náuseas y vómitos postoperatorios en el paciente pediátrico
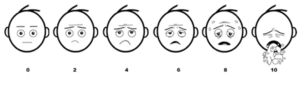
Las náuseas, definidas como una sensación de malestar con tendencia al vómito, constituyen un síntoma difícilmente identificable en el caso de pacientes pediátricos de corta edad. Sin embargo, se calcula que la incidencia de NVPO podría llegar a alcanzar en torno a un 80% en la población pediátrica, un dato muy superior al que se registra en pacientes adultos (9). Las escalas de riesgo descritas para estos últimos no son aplicables en el caso de los niños. Eberhart et al. desarrollaron un score pediátrico considerando los siguientes factores de riesgo: edad mayor de tres años, duración de la cirugía, cirugía de estrabismo e historia personal o familiar de NVPO (tabla 5). Otras investigaciones han incluido también la cirugía de amigdalectomía como factor de riesgo de NVPO.

Desde el punto de vista anestésico, la administración de opioides se considera un factor dominante en la génesis de las NVPO. Aquellos fármacos de vida media más larga (morfina, hidromorfona) acentúan el riesgo de NVPO en comparación con otros de vida media más corta como el fentanilo. Los AINES y el paracetamol se emplean habitualmente como herramienta analgésica para fomentar el ahorro de opioides. Sin embargo, existe un fundamentado recelo para el empleo de los AINES en el contexto de las cirugías de adenoidectomía o amigdalectomía por el potencial riesgo de favorecer un sangrado postoperatorio. Por otro lado, los anestésicos volátiles mantienen una profunda asociación con la incidencia de NVPO, motivo por el cual muchos clínicos abogan por el empleo preferente de la anestesia total intravenosa (TIVA) en pacientes de riesgo. Por último, la fluidoterapia intravenosa intraoperatoria, con administración de volúmenes de hasta 30mL/kg para procedimientos menores, ha demostrado reducir la incidencia de NVPO en pacientes pediátricos sometidos a cirugía ambulatoria (9).
En cualquier caso, y dada la elevada incidencia de NVPO descrita en la población pediátrica, parece que sí estaría indicado el empleo sistemático de una profilaxis antiemética farmacológica. Entre los diversos antagonistas serotoninérgicos, ondansetron se ha utilizado de manera segura en dosis de 0.1mg/kg hasta un máximo de 4mg. Dado que posee una vida media de 4h, ha de administrarse preferiblemente hacia el final del procedimiento practicado. Granisetron (40μg/kg) y tropisetron (0.1mg/kg) constituyen alternativas disponibles. En general, este grupo de fármacos se considera de primera línea en el tratamiento y profilaxis de las NVPO pediátricas, aunque siempre teniendo en cuenta su potencial prolongación del intervalo QT.
La eficacia del ondansetron en niños se incrementa al emplearse de manera conjunta con dexametasona (0.1mg/kg hasta un máximo de 5mg). Esta última debería administrarse al principio del acto anestésico debido a su perfil farmacocinético. Aquellos pacientes con algún tipo de proceso tumoral activo deberían tratarse con especial precaución por el riesgo de desarrollar un síndrome de lisis tumoral vinculado a la administración de corticoterapia. En cuanto a los fármacos antagonistas del receptor de neurokinina-1 (aprepitant, fosaprepitant), los datos aún son escasos en lo que se refiere a su empleo en la población pediátrica. Sí que existe amplia experiencia con la utilización de droperidol (antagonista dopaminérgico) en dosis de 0.05–0.075mg/kg hasta un máximo de 1.25mg. A pesar de ello, suscita una especial preocupación su riesgo de prolongación del intervalo QT, y por este motivo ha caído en desuso. Tampoco la metoclopramida parece que tenga un perfil muy favorable para su empleo en niños, población en la que presenta una menor eficacia clínica a la vez que una mayor tasa de efectos adversos extrapiramidales asociados (9).
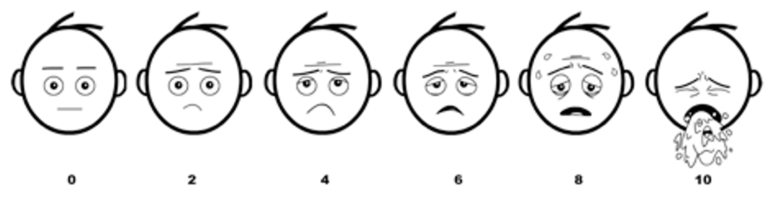
Existen herramientas disponibles, como la escala de BARF (Baxter Retching Faces, figura 1) para facilitar el diagnóstico de las NVPO en niños. A pesar de ello, a menudo las náuseas pueden pasar desapercibidas en el paciente pediátrico. Más allá del periodo postoperatorio temprano, las náuseas y vómitos posteriores al alta hospitalaria también suponen una complicación relevante a tener en cuenta. Al igual que sucede con los pacientes adultos, se recomienda el tratamiento expeditivo de las NVPO con un agente de una familia distinta a las empleadas previamente durante la profilaxis. En todo caso, también tendrá que considerarse la velocidad de inicio de acción de cada opción terapéutica disponible y favorecer el empleo como rescate de aquellas que asocien una menor demora en este sentido.
Manejo de las náuseas y los vómitos más allá del alta hospitalaria
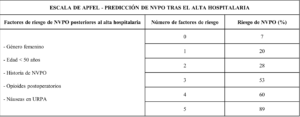
Se estima que las NVPO posteriores al alta hospitalaria afectan aproximadamente al 30% de los pacientes, especialmente a aquellos sometidos a cirugía ambulatoria. Un número significativo de estos casos se vincula al empleo de analgésicos (10). El periodo considerado para definir estas complicaciones varía en función de los estudios, aunque generalmente abarca hasta un máximo de 7 días postoperatorios. Distintos factores se han asociado con la posible aparición de NVPO durante esta fase. Existe una variante de la escala de Apfel validada específicamente para predecir la aparición de náuseas y vómitos posteriores al alta hospitalaria (tabla 6).
El dolor, así como el consumo de analgésicos (especialmente opioides), durante los primeros días postoperatorios podrían contribuir de manera significativa a la aparición de NVPAH (náuseas y vómitos posteriores al alta hospitalaria). La aparición de un “dolor de rebote” tras la aplicación de anestesia regional afecta al menos a un 40% de los pacientes sometidos a procedimientos ambulatorios. La prevención y el adecuado tratamiento del dolor postoperatorio influirán de manera indirecta en la posible aparición de NVPAH durante los primeros días. En este sentido, la educación de los pacientes a menudo es un factor pasado por alto. La administración de una información estructurada podría mejorar el abordaje y manejo tanto del dolor como de la aparición de NVPAH, factores ambos capaces de condicionar en gran medida la calidad de la experiencia percibida (10).
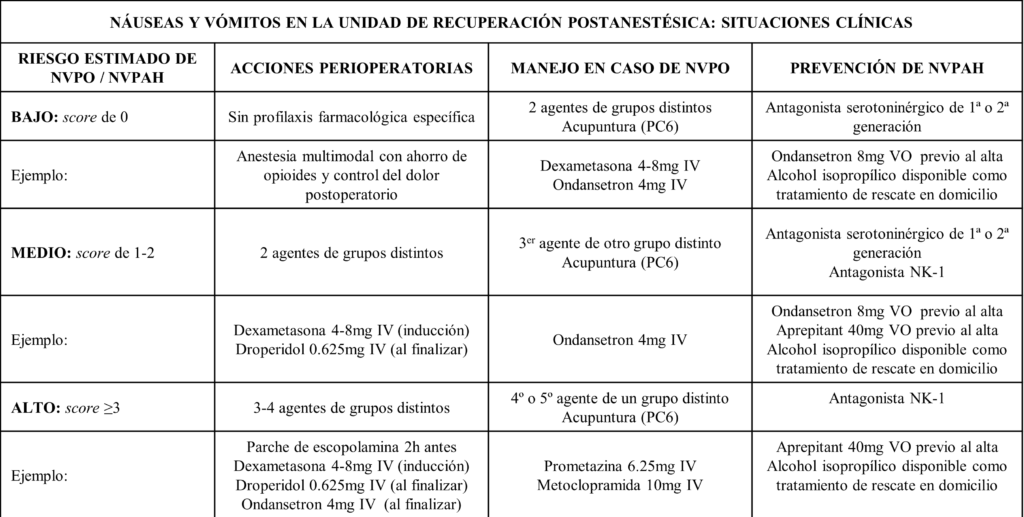
En cuanto al manejo de las NVPAH, en primer lugar se recomienda una nueva valoración del riesgo previa al alta hospitalaria. En este punto, el único factor adicional que podría haberse añadido desde el periodo preoperatorio es la aparición de un episodio de NVPO durante la estancia en URPA. Ello podría incrementar el riesgo de NVPAH y por tanto condicionar el manejo preventivo de futuros episodios. En caso de una profilaxis de NVPO fallida, la primera indicación es administrar un nuevo agente antiemético de una familia distinta a las empleadas con anterioridad. De cara al alta hospitalaria, la administración de 8mg de ondansetron por vía oral puede constituir una opción válida. Podría repetirse esta misma dosis en la mañana del primer y segundo día postoperatorios en caso de necesidad. De igual manera, puede considerarse como alternativa la administración de palonosetron intravenoso en dosis de 0.075mg o aprepitant 40mg por vía oral (ambos tienen una vida media de unas 40 horas). En el caso de pacientes clasificados como alto riesgo, en los que concurran 3 o más factores de riesgo de NVPAH, debería considerarse la administración conjunta de por lo menos 2 agentes de familias distintas. El empleo de terapias alternativas como las inhalaciones de alcohol isopropílico o la estimulación del punto de acupuntura PC6 en la muñeca cuentan con cierta evidencia de éxito y podrían complementar el tratamiento. En la tabla 7 se ejemplifica una hipotética pauta para el manejo de las NVPO y prevención de las NVPAH (10).
Perspectivas para el futuro: genética, medicina personalizada y nuevos antieméticos
Los modelos actuales para la estratificación del riesgo de náuseas y vómitos postoperatorios no tienen en cuenta el papel de los factores genéticos implicados. Dichos factores han demostrado ejercer una significativa influencia sobre la incidencia de NVPO y la respuesta a los distintos fármacos empleados. Es posible que la aparición de estas complicaciones en pacientes clasificados en el estrato de bajo riesgo obedezca a este tipo de susceptibilidad genética individual.
Diversos estudios genéticos han demostrado que algunos polimorfismos de un solo nucleótido, relacionados con los genes que codifican receptores como el de serotonina tipo 3 o el de dopamina tipo 2, juegan un importante papel en la génesis de las náuseas y vómitos o en el metabolismo de los fármacos antieméticos (11). Este concepto refuerza la necesidad de un abordaje multimodal para la profilaxis de NVPO, capaz de actuar simultáneamente sobre varios objetivos del sistema y evitando focalizarse de manera inadvertida sobre alguno de los puntos individuales de resistencia.
De igual manera, debe tenerse en cuenta la posible variación en la actividad de los citocromos hepáticos en los distintos pacientes. Así, por ejemplo, el metabolismo de Ondansetron se verá afectado por eventuales modificaciones de la actividad de los enzimas CYP450. Como ejemplo, se ha podido comprobar que los llamados metabolizadores ultra-rápidos de CYP2D6 sufren una incidencia mayor de NVPO respecto a otros pacientes tratados profilácticamente con antagonistas del receptor de serotonina, como Ondansetron (11).
En los próximos años, los biomarcadores farmacogenómicos probablemente definirán las pautas de tratamiento de los pacientes, en lo que se ha venido a denominar como una “medicina personalizada”. En el terreno de las NVPO, es posible que el estudio genético de los pacientes sirva de ayuda al clínico para definir mejor los distintos estratos de riesgo y, gracias a ello, lograr un mejor ajuste de los protocolos de profilaxis y tratamiento administrados. En cualquier caso, un escenario en el que se aplique un estudio genético pormenorizado a la totalidad de los pacientes quirúrgicos aún parece lejano. Mientras tanto, la conciencia de que una susceptibilidad genética individual es posible deberá mantener la alerta del médico prescriptor de terapias antieméticas.
Por otro lado, el creciente interés por la profilaxis multimodal de las náuseas y los vómitos postoperatorios ha favorecido el desarrollo de nuevos fármacos dentro de las diversas familias terapéuticas implicadas (antagonistas 5-HT3, antagonistas dopaminérgicos D2, antagonistas de la neurokinina NK1, corticosteroides, antihistamínicos y anticolinérgicos). A continuación se enumeran las características principales de algunos de los agentes más novedosos:
Palonosetron: se trata de un antagonista del receptor 5-HT3 de segunda generación aprobado por parte de la FDA (Food and Drug Administration) desde 2008. Sus características moleculares prolongan su capacidad inhibitoria alrededor de 24 horas. Debe administrarse al inicio de la cirugía, con una dosis intravenosa de 0.075mg. Comparado con Ondansetron, consigue una mayor reducción de la incidencia de vómitos tanto tempranos como tardíos. Además, Palonosetron ofrece una menor incidencia de mareos y menor prolongación del intervalo QT como efectos secundarios, comparado con otros antagonistas del receptor 5-HT3. En resumen, Palonosetron alcanza una mayor eficacia en la reducción de la incidencia de NVPO que otros antagonistas 5-HT3 de primera generación, con un perfil de efectos adversos más favorable y una cinética farmacológica que lo convierte en apto para la prevención de NVPO incluso más allá del alta hospitalaria (12).
Ramosetron: se trata de otro antagonista del receptor 5-HT3 de segunda generación. Comparado con sus predecesores, ofrece una tasa de disociación de los receptores más lenta, una mayor potencia y una mayor duración del efecto. Se emplea habitualmente en dosis de 0.3mg, siendo sus resultados superiores a los obtenidos con Ondansetron 4-8mg. Comparado con Palonosetron, aunque no se detectan diferencias significativas en el corto plazo, un análisis de subgrupos reveló una mayor eficacia de éste en la prevención de los vómitos más allá de las 24-48h (12).
Amisulprida: se trata de un antagonista de los receptores de dopamina con un amplio historial en el manejo de cuadros psicóticos. Desde 2020 se encuentra aprobado por parte de la FDA para la prevención y el tratamiento de las NVPO. Se aplica en dosis intravenosa de 5mg y es eficaz durante 24h. Como excepción, se recomienda una dosis de 10mg para el tratamiento de aquellos pacientes con NVPO tras una profilaxis previa fallida. Sus efectos adversos son infrecuentes y de carácter benigno, al contrario que sucede con otros miembros de su misma familia terapéutica (12).
Aprepitant y Fosaprepitant: se trata de los únicos antagonistas NK1 aprobados de momento por parte de la FDA para la prevención y tratamiento de las náuseas y vómitos postoperatorios o asociados a quimioterapia. La dosis recomendada de Aprepitant es de 40mg por vía oral 3 horas antes de la inducción de la anestesia. Fosaprepitant es un profármaco de Aprepitant, disponible en viales de 150mg para su administración intravenosa. A día de hoy se encuentra aprobado por la FDA únicamente para el manejo de las náuseas y vómitos asociados a la quimioterapia. Aprepitant ha demostrado un mejor perfil en la reducción de la incidencia de vómitos que en la reducción de la incidencia de náuseas. Tiene una larga duración de acción (vida media de 9-12h), lo cual podría resultar beneficioso para la prevención de NVPO más allá del alta hospitalaria. Sus efectos secundarios más frecuentes son: cefalea, hipotensión, bradicardia, estreñimiento, prurito, fiebre y mareo. De momento su precio es elevado, lo cual limita su utilización, pero es posible que en los próximos años tanto Aprepitant como Fosaprepitant, y otros fármacos actualmente en investigación dentro de esta misma familia, cobren una mayor relevancia en el manejo de las NVPO (12).
Conclusiones
Las náuseas y los vómitos postoperatorios (NVPO) constituyen una complicación frecuente y desagradable, con una amplia repercusión sobre la calidad asistencial percibida por parte de los pacientes. Suponen además una notable carga económica sobre el sistema de salud. El conocimiento de su fisiopatología resulta fundamental para comprender las dianas farmacológicas empleadas en su prevención y tratamiento. En este sentido, existen múltiples familias de fármacos en el arsenal terapéutico contra las NVPO. Algunos compuestos gozan de una dilatada experiencia de uso clínico, mientras que otros han tenido una introducción más reciente o se encuentran aún en fase de desarrollo. A día de hoy, la evidencia disponible parece apoyar con relativa fuerza el empleo de un abordaje farmacológico multimodal, sustentado también en la evaluación y estratificación del riesgo. Algunos grupos concretos de pacientes, como es el caso de la población pediátrica o de la paciente obstétrica, merecen consideraciones especiales en el abordaje de las NVPO. No debería infraestimarse la importancia de estas complicaciones más allá del momento del alta hospitalaria. En cuanto a las perspectivas actuales de cara al futuro, caben destacar tanto el desarrollo incipiente de algunas nuevas moléculas prometedoras, como el creciente papel de la medicina personalizada a través de la genética.
Bibliografía
- Dewinter G, Habib AS. Postoperative nausea and vomiting: State of the art. Best Pract Res Clin Anaesthesiol. 2020;34(4):663-665. doi:10.1016/j.bpa.2020.11.002 (PubMed)
- Gress K, Urits I, Viswanath O, Urman RD. Clinical and economic burden of postoperative nausea and vomiting: Analysis of existing cost data. Best Pract Res Clin Anaesthesiol. 2020;34(4):681-686. doi:10.1016/j.bpa.2020.07.003 (HTML)
- Stoops S, Kovac A. New insights into the pathophysiology and risk factors for PONV. Best Pract Res Clin Anaesthesiol. 2020;34(4):667-679. doi:10.1016/j.bpa.2020.06.001 (PubMed)
- Uribe AA, Bergese SD. What is the ideal combination antiemetic regimen?. Best Pract Res Clin Anaesthesiol. 2020;34(4):701-712. doi:10.1016/j.bpa.2020.10.009 (HTML)
- Kranke P, Meybohm P, Diemunsch P, Eberhart LHJ. Risk-adapted strategy or universal multimodal approach for PONV prophylaxis?. Best Pract Res Clin Anaesthesiol. 2020;34(4):721-734. doi:10.1016/j.bpa.2020.05.003 (PubMed)
- Schwartz J, Gan TJ. Management of postoperative nausea and vomiting in the context of an Enhanced Recovery after Surgery program. Best Pract Res Clin Anaesthesiol. 2020;34(4):687-700. doi:10.1016/j.bpa.2020.07.011 (PubMed)
- Tan HS, Habib AS. The optimum management of nausea and vomiting during and after cesarean delivery. Best Pract Res Clin Anaesthesiol. 2020;34(4):735-747. doi:10.1016/j.bpa.2020.04.012 (PubMed)
- Borgeat A, Stirnemann HR. Ondansetron is effective to treat spinal or epidural morphine-induced pruritus. Anesthesiology. 1999;90(2):432-436. doi:10.1097/00000542-199902000-00017 (HTML)
- Ames WA, Machovec K. An update on the management of PONV in a pediatric patient. Best Pract Res Clin Anaesthesiol. 2020;34(4):749-758. doi:10.1016/j.bpa.2020.05.007 (HTML)
- Dziadzko M, Aubrun F. Management of postdischarge nausea and vomiting. Best Pract Res Clin Anaesthesiol. 2020;34(4):771-778. doi:10.1016/j.bpa.2020.10.008 (HTML)
- Candiotti K, Shrestha C, Silva Ceschim MR. Is there a place for genetics in the management of PONV? Best Pract Res Clin Anaesthesiol. 2020;34(4):713-720. doi:10.1016/j.bpa.2020.05.002 (HTML)
- Tan HS, Dewinter G, Habib AS. The next generation of antiemetics for the management of postoperative nausea and vomiting. Best Pract Res Clin Anaesthesiol. 2020;34(4):759-769. doi:10.1016/j.bpa.2020.11.004 (HTML)



Dr Díaz buen día. Antes que nada lo felicito por tan ilustrativo artículo. Me dirijo a usted para solicitar su ayuda ya que estoy realizando un proyecto donde se emplean dos opioides a nivel peridural y en el que la prevención de la NVPO son primordiales ya que es cirugía de corta estancia. Soy nuevo en esto de las publicaciones y no encuentro como citarlo, por lo que agradezco de antemano su ayuda.
Reciba un cordial saludo.