Del Rey de Cabo C (1), Cocho Crespo S(1), López Herrero R (1), Rubio Babiano P (2)
(1) MIR Anestesia y Reanimación. Hospital Clínico Universitario de Valladolid.
(2) Adjunto Anestesia y Reanimación. Hospital Clínico Universitario de Valladolid.
Cómo citar este artículo: Del Rey de Cabo, C., Cocho Crespo, S., López Herrero, R., & Rubio Babiano, P. (2023). Guía anestésico-quirúrgica en el tratamiento de la cirugía de la aorta ascendente y del arco aórtico. Revista Electrónica AnestesiaR, 15(1). https://doi.org/10.30445/rear.v15i1.1019
Artículo original: López Gómez A, Rodríguez R. Zebdi N, Ríos Barrera R, Forteza A, Legarra Calderón JJ et al. Guía anestésico-quirúrgica en el tratamiento de la cirugía de la aorta ascendente y del arco aórtico. Documento de consenso de las Sociedades Española de Cirugía Cardiovascular y Endovascular y la Sociedad Española de Anestesiología, Reanimación y Terapéutica del Dolor. Cir Cardiov. 2020;27(2):47–74. (HTML)
Introducción
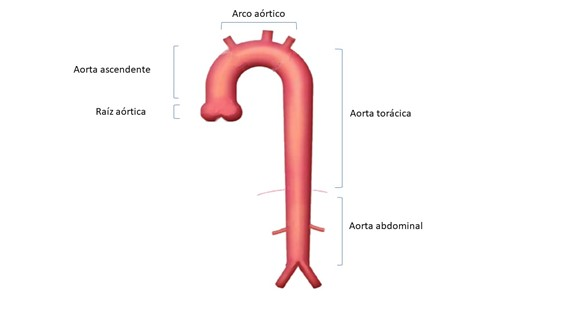
La patología de la aorta, desde sus inicios, ha supuesto siempre un reto para la medicina. Las enfermedades aórticas pueden diagnosticarse tras un largo período de evolución subclínica o tras una presentación aguda, precisando un diagnóstico y toma de decisiones rápidos a fin de reducir el mal pronóstico que tienen. Tanto a nivel diagnóstico como terapéutico, el volumen de variables implicado ha hecho que dicha patología sea abordada por una ingente cantidad de especialistas donde se implican cardiólogos, cirujanos cardíacos, cirujanos vasculares, anestesiólogos y radiólogos entre otros. Los tratamientos endovasculares tienen un papel cada vez más importante en el tratamiento de las enfermedades aórticas, pero la cirugía abierta sigue siendo necesaria en muchas situaciones.
Objetivo de la revisión: el presente trabajo propone explicar, estandarizar y difundir las diferentes recomendaciones de actuación y manejo desde el punto de vista anestésico, de esta intervención tan compleja, analizando la primera guía anestésico-quirúrgica en el tratamiento de la cirugía abierta de aorta ascendente y del arco aórtico.
Guía Clínica
1.- Preoperatorio
Aunque las técnicas empleadas en cirugía cardiaca han mejorado en la ultima década, los riesgos de morbimortalidad continúan presentes. La evaluación preoperatoria debe estar adaptada al grado de urgencia. Los pacientes propuestos para la intervención son, en general, pacientes con patología vascular, hipertensos, coronarios, insuficientes cardiacos, eventualmente con un compromiso de la función respiratoria, sin olvidar la patología renal o metabólica. Los objetivos de la evaluación en el período preoperatorio son los comunes a cualquier intervención, pero se debe hacer hincapié en revisar los factores de riesgo cardiovascular de la historia clínica junto con las pruebas complementarias para evaluar, minimizar y optimizar cualquier condición que presente el paciente. Ante cualquier alteración que se pueda mejorar se debe retrasar la operación, siempre y cuando la cirugía sea electiva y el riesgo de posponer la intervención sea menor que el beneficio de optimizar la condición del paciente. Se debe explicar el plan anestésico, así como riesgos derivados de la intervención a la vez que aliviamos la ansiedad del paciente. Siempre se debe obtener el consentimiento informado.
Entre los aspectos a destacar:
1. Control estricto de la presión arterial (PA). En caso de patología aórtica aguda el objetivo principal es normalizar la PA con bloqueantes intravenosos.
2. En caso de patología aórtica aguda es imprescindible la realización de una ecocardiografía transtorácica para descartar complicaciones.
3. Estrategias de ahorro de hemoderivados, protocolos de hemorragia masiva y guía del manejo de sangrado.
4. Inicio de técnicas de fisioterapia respiratoria/prehabilitación.
5. Adecuado manejo de los antiagregantes y anticoagulantes en el perioperatorio. Los autores recomiendan revisar la guía consenso de manejo perioperatorio y periprocedimiento del tratamiento antitrombótico (SEDAR)(1).
2.-Intraoperatorio
La técnica anestésica y la monitorización debe individualizarse y nunca ser motivo de retraso del tratamiento quirúrgico en caso de cirugía urgente. La monitorización debe ser lo más completa posible. Además de la monitorización estándar de la ASA (oxigenación, ventilación, circulación y temperatura), estas guías proponen incluir lo siguiente:
a) Monitorización cardiovascular
-La monitorización continua de la tensión arterial invasiva canalizada previa a la inducción anestésicase incluye por parte de los autores como recomendación IIA con un nivel de evidencia C. La monitorización debe ser invasiva y bilateral en las extremidades superiores. Una línea arterial única no es suficiente para la monitorización ininterrumpida de las presiones de perfusión de órganos vitales. La medición de la tensión arterial (TA) cruenta en ambas arterias radiales permite controlar la presión de perfusión cerebral (PPC) sin interrupción durante la canulación en arteria axilar directa o con injerto y durante la reparación. En la reparación quirúrgica del arco aórtico, se debe considerar la monitorización de la TA femoral(2).
–Catéter venoso central en vena yugular interna y 1-2 accesos intravasculares de gran calibre.
–Catéter de arteria pulmonar (si está indicado) para medir presiones pulmonares y en cuña.
-Dan un mayor protagonismo a la ecocardiografía transesofágica. Como recomendación clase IB, se incluye la ecocardiografía transesofágica (ETE) durante todos los procedimientos quirúrgicos de aorta torácica abierta(2)(3).
b) Monitorización neurológica
La neuromonitorización constituye una parte importante de la monitorización en este tipo de cirugías. Las modalidades de monitorización más empleadas son: electroencefalograma (EEG), índice biespectral para medir el grado de hipnosis (BIS), oximetría cerebral (NIRS), potenciales evocados somatosensoriales (PESS) y motores (PEM). La oximetría cerebral (NIRS/INVOS) no invasiva determina la saturación regional de oxígeno. Debe mantenerse a unos valores superiores a 40 y debe evitarse un descenso del 20% respecto al basal. Actualmente se aconseja la monitorización INVOS (esta guía la propone como recomendación I con un nivel de evidencia B) y es la más utilizada, así como el uso de un algoritmo en caso de desaturaciones (figura 1).
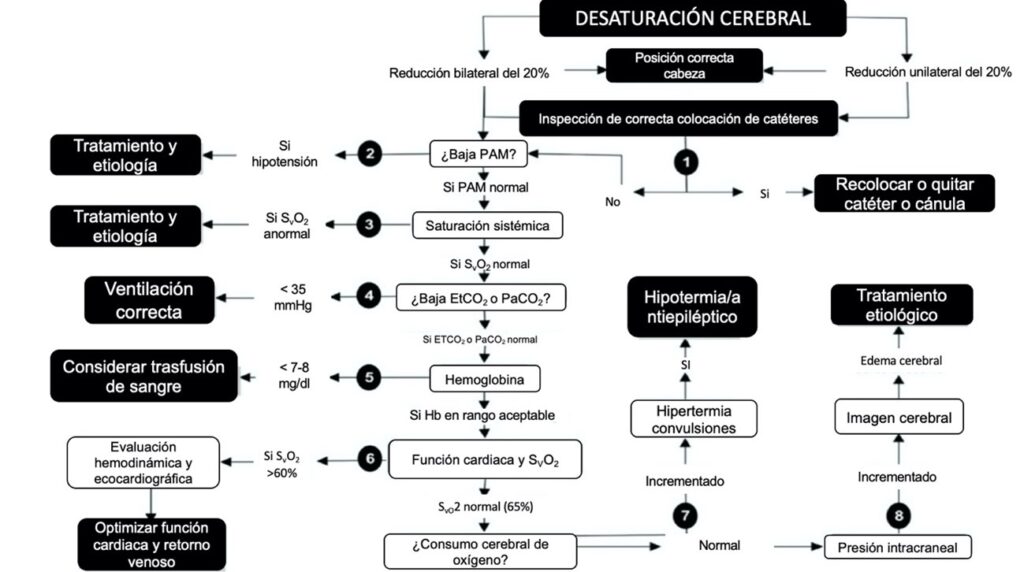
Modificado de Denault et al (4).
c) Monitorización de la temperatura
La monitorización de la temperatura durante la cirugía cardíaca es una parte habitual de la práctica clínica. Entre las recomendaciones para el control térmico propuestas por los autores se encuentra el uso de la temperatura arterial situada a la salida arterial del oxigenador, como una medición de la temperatura cerebral durante la circulación extracorpórea (CEC) (5). También recomiendan en las cirugías en las que sea necesaria la parada circulatoria la medición en múltiples sitios (nasofaríngea, timpánica, vesical o rectal) para monitorizar el enfriamiento durante la hipotermia y el recalentamiento. En la cirugía abierta del arco aórtico proponen controlar la temperatura nasofaríngea y timpánica para garantizar un enfriamiento adecuado del cerebro (2).
Los sitios habituales de monitorización son: nasofaríngeo, sangre a través del termistor (transductor que registra cambios de temperatura) del catéter de arteria pulmonar, vejiga (monitorización central de la temperatura, que proporciona información sobre la protección de las visceral riñones, extremidades inferiores y médula espina), rectal, canal auditivo y en el circuito de CEC.
2.1 Periodo pre-CEC
La inducción anestésica debe ser suave evitando picos hipertensivos. En líneas generales, el mantenimiento anestésico no es muy diferente al de otros procedimientos de cirugía cardiaca, con la peculiaridad de que suele ser necesario el empleo de parada cardiocirculatoria más o menos profunda en caso de afectación del arco. El control hemodinámico debe ser estricto durante la fase de disección y canulación para evitar la rotura de la aorta. La preparación para el inicio de la CEC es estándar al resto de cirugías.
Los autores siguen dando importancia a la utilidad del estudio ecocardiográfico intraoperatorio, no solo para la valoración inicial, sino también para confirmar y caracterizar el alcance de la patología aórtica y de las otras válvulas. Durante la canulación aórtica se utiliza para guiar la colocación de las cánulas aórticas y venosas.
2.2 CEC y parada circulatoria
En este tipo de cirugía es imprescindible la interrupción total de la circulación sistémica, incluida la circulación cerebral, durante un período de tiempo variable. En la parada circulatoria es importante el manejo de estrategias de protección cerebral, entre las que se incluyen: a) la hipotermia (medida de protección orgánica estándar durante el periodo de parada circulatoria), b) la perfusión cerebral retrógrada y c) la perfusión cerebral anterógrada.
Las estrategias de protección cerebral en cirugía abierta de aorta ascendente y arco aórtico se deben abordar de forma multidisciplinar (intervención, anestesiología, perfusionista) con el fin de evitar eventos isquémicos cerebrales transitorios o permanentes. La perfusión cerebral anterógrada selectiva es, según los autores, la técnica de elección en cirugía abierta del arco aórtico, y, en combinación con la parada circulatoria con hipotermia moderada la técnica elegida en muchos centros para este tipo de operación. El empleo de medidas de protección cerebral es una recomendación de las guías ESC/EACTS clase IB.
Las guías hacen referencia al empleo de la perfusión cerebral anterógrada (PCA) como recomendación IIa nivel de evidencia B, tanto en las guías americanas como en las europeas. En las guías americanas, del año 2010, se otorga el mismo nivel de evidencia y recomendación para otras técnicas de protección cerebral: parada circulatoria con hipotermia moderada (PCHM) y perfusión cerebral retrógrada (PCR).
Otras medidas/recomendaciones que destacan los autores son:
- Control de la hiperglucemia: Recomiendan mantener niveles < 180 mg/dl. Niveles de glucosa > 250 mg/dl empeoran el pronóstico neurológico. La Society of Thoracic Surgeons ha publicado unas guías cuya aplicación pueden ser de utilidad para el control perioperatorio de la glucemia en cirugía cardíaca(6).
- Hemodilución: para disminuir la viscosidad de la sangre y evitar la agregación de los hematíes.
- Equilibrio ácido-base: El método habitualmente empleado en cirugía cardíaca es el alfa-stat). Se debe mantener un PCO2 en torno a 45 mmHg (lectura de GAS a 37º).
- Monitorización a la cabecera del paciente, más conocido por “point-of-care clinical testing”: coagulación (tiempo de coagulación activado (ACT) y tromboelastografía (TEG)/ tromboelastometría rotacional (ROTEM).
- Medidas farmacológicas de protección cerebral como los corticoides (metilprednisolona 500 mg), barbitúricos (tiopental 10mg/kg), propofol, magnesio, bloqueadores neuromusculares o los anestésicos inhalados entre otros.
- Monitorización del gasto urinario mediante sondaje vesical.
2.3 Salida de CEC
Tras la reparación aórtica, se debe realizar un recalentamiento progresivo para evitar la hipertermia (en cirugía de aorta ascendente y/o arco la hipertermia cerebral perioperatoria no solo no está indicada, sino que puede ser perjudicial (recomendación IIIB)). Puede ser necesario el manejo inicial con fármacos inotrópicos y/o vasoactivos. Se debe mantener una buena presión de perfusión visceral, optimizando la precarga, aunque inicialmente no conviene una PAS > 100 mmHg para favorecer la hemostasia de las suturas.
Otro aspecto importante en la salida de circulación extracorpórea es la hemostasia y el manejo de la coagulopatía ya que la cirugía de arco aórtico se complica frecuentemente con sangrado excesivo y con elevados requerimientos de hemoderivados. Se deberá realizar según los protocolos de cada centro hospitalario, siendo necesario corregir los defectos de coagulación para favorecer la hemostasia primaria y minimizar el sangrado. Las guías hacen referencia a un estudio reciente, Hemostasis Registry of Patients in Cardiac Surgery (HEROES-CS) (7), que concluye que el uso de ROTEM para guiar las necesidades de transfusión mejora de manera significativa la pérdida de sangre y reduce el consumo de estos hemoderivados.
Por último, durante la salida de CEC no debemos olvidar el manejo analgésico.
3.- Postoperatorio
Los autores remarcan 3 aspecto claves:
- Control de la tensión arterial según necesidades del paciente para optimizar la precarga. Se deberá guiar por la monitorización escogida para mantener TAS <100-120 mmHg a fin de favorecer la hemostasia de suturas.
- Control de la hemostasia y del sangrado.
- Valoración neurológica precoz.
Comentario
El trabajo de estas guías resalta el valor que tiene un abordaje integral de diferentes especialidades en este tipo de dolencia. Los autores recomiendan que la toma de decisiones para el tratamiento de las patologías del arco aórtico y de la aorta ascendente sea por un equipo aórtico (grupo de expertos dentro de un Comité de aorta o “Aortic Team, término que surge del último documento de consenso de expertos de la EACTS y la ESVS), en el que se incluyen anestesiólogos, cirujanos cardiacos, vasculares y radiólogos, entre otros. Además, recomiendan centralizar la atención y que el tratamiento electivo se realice en centros especializados de referencia, con quirófanos híbridos que ofrezcan cirugía cardiovascular abierta y endovascular. Ésta es la única forma de comprender de manera correcta el curso natural de la enfermedad y proporcionar todas las opciones disponibles de tratamiento, así como tratar de forma efectiva las complicaciones que vayan surgiendo a lo largo del proceso.
Es muy importante que esta enfermedad sea tratada por un equipo dedicado exclusivamente a este tipo de patología y en centros de referencia. Existen estudios que demuestran que, en la mayoría de las cirugías aórticas, existe una relación directa entre el volumen de casos por hospital y los resultados, observándose una menor mortalidad en los centros donde se realiza con más frecuencia este tipo de intervención (8)(9).
Actualmente las guías de práctica clínica aconsejan la cirugía profiláctica (reemplazo aórtico programado) en función del diámetro aórtico. Los autores de las guías recomiendan que el tratamiento de los aneurismas aislados del arco aórtico deben considerarse quirúrgicos con un diámetro ≥ 55 mm(10). Si el paciente presenta una válvula aórtica bicúspide y factores de riesgo (coartación de aorta, hipertensión sistémica, antecedentes familiares de disección o aumento del diámetro aórtico > 3 mm/año) el diámetro pasa a ser >50 mm. Si el paciente muestra cualquier conectivopatía (síndrome Marfan, síndrome Loeys-Dietz, síndrome Ehlers-Danlos) este diámetro se reducirá hasta los 45 mm(5). También incluyen una serie de contraindicaciones. No estará indicada la cirugía abierta de aorta en pacientes que presenten una baja esperanza de vida debido a las comorbilidades que muestre. La edad la incluyen como contraindicación relativa, siempre valorando el riesgo beneficio de la intervención.
Comentario personal: Actualmente existe un buen número de guías sobre el diagnóstico y tratamiento de la patología de la aorta creadas por organizaciones y sociedades. Estas guías evalúan toda la evidencia disponible en el momento de redactarlas con el propósito de ayudar a los profesionales sanitarios a seleccionar las mejores estrategias durante todo el proceso, teniendo siempre en cuenta la afección de cada paciente e individualizando la toma de decisiones. No obstante, es responsabilidad de cada profesional sanitario tomar la decisión que más se ajuste a las necesidades de cada paciente. El trabajo de la guía ofrece un abordaje integrador anestésico-quirúrgico de la patología del arco aórtico a través de un conjunto de recomendaciones basadas en opiniones de expertos, documentos de consenso y guías internacionales con diferentes grados de recomendación. Con relativa frecuencia, la guía no tiene un nivel de evidencia A o B ni hace una indicación tipo I, por tanto, para su aplicación es importante considerar como hemos dicho antes, que cada paciente es único, así como la experiencia y resultados de cada centro. Estas guías suponen la primera propuesta de protocolo integrador que deberá ser evaluado en un futuro.
Bibliografía
- Vivas D, Rolda I, Ferrandis R, Marın F, Roldan V, Martı A, et al. Manejo perioperatorio y periprocedimiento del tratamiento antitrombótico: documento de consenso de SEC, SEDAR, SEACV, SECTCV, AEC, SECPRE, SEPD, SEGO, SEHH, SETH, SEMERGEN, SEMFYC, SEMG, SEMICYUC, SEMI, SEMES, SEPAR, SENEC, SEO, SEPA, SERVEI, SECOT y AEU. Rev Esp Cardiol. 2018;71:553—64. (HTML)
- Erbel R, Aboyans V, Boileau C, Bossone E, Di Bartolomeo R, Eggebrecht H, et al. 2014 ESC Guidelines on the diagnosis and treatment of aortic diseases: Document covering acute and chronic aortic diseases of the thoracic and abdominal aorta of the adult. The Task Force for the Diagnosis and Treatment of Aortic Diseases of the European Society of Cardiology (ESC). Eur Heart J [Internet]. 2014;35:2873—926 [citado 21 Nov 2019 Nov 21]. Disponible en: http://www.ncbi.nlm.nih.gov/pubmed/25173340.
- Carmona P, Pérez-Boscá JL, Marqués JI, Mateo E, De Andrés J. Papel de la ecocardiografía transesofágica perioperatoria en la patología de la aorta. Cir Cardiovasc. 2014;21:37—48. (Medes)
- Denault A, Deschamps A, Murkin JM. A proposed algorithm for the intraoperative use of cerebral near-infrared spectroscopy. Semin Cardiothorac Vasc Anesth. 2007;11:274—81. (HTML)
- Engelman R, Baker RA, Likosky DS, Grigore A, Dickinson TA, Shore-Lesserson L, et al. The Society of Thoracic Surgeons The Society of Cardiovascular Anesthesiologists, and The American Society of ExtraCorporeal Technology: Clinical Practice Guidelines for Cardiopulmonary Bypass – Temperature Management During Cardiopulmonary Bypass. Ann Thorac Surg. 2015;100:748—57. (PDF)
- Lazar HL, McDonnell M, Chipkin SR, Furnary AP, Engelman RM, Sadhu AR, et al. The Society of Thoracic Surgeons Practice Guideline Series: Blood glucose management during adult cardiac surgery. Ann Thorac Surg. 2009;87:663—9. (PubMed)
- Kuiper GJAJM, van Egmond LT, Henskens YMC, Roekaerts PM, Maessen JG, ten Cate H, et al. Shifts of transfusión demand in cardiac surgery after implementation of rotational thromboelastometry—Guided transfusion protocols: Analysis of the HEROES-CS (HEmostasis Registry of patiEntS in Cardiac Surgery) observational prospective open cohort database. J Cardiothorac Vasc Anesth. 2019;33:307—17. (HTML)
- Hughes GC, Zhao Y, Rankin JS, Scarborough JE, O’Brien S, Bavaria JE,Wolfe WG, Gaca JG, Gammie JS, Shahian DM, Smith PK. Effects of institutional volumes on operative outcomes fo aortic root replacement in North America. J Thorac Cardiovasc Surg. 2013;145:166–70. (HTML)
- Raimund Erbel, Victor Aboyans, Catherine Boileau, Eduardo Bossone, Roberto Di Bartolomeo et al. Guía ESC 2014 sobre diagnóstico y tratamiento de la patología de la aorta. Rev Esp Cardiol. 2015;68(3):242.e1-e69. (HTML)
- Anguita M, Fernández-Ortiz A, Worner F, Alonso A, Cequier A, Comin J, et al. La Sociedad Española de Cardiología y las guías de práctica clínica de la SEC: hacia una nueva orientación. Rev Esp Cardiol. 2011;64:795-6 (HTML)