Cómo citar este artículo:de Dios Tomás, E., Ramasco Rueda, F., García de Quinto, H., Quecedo, L., Planas Roca, A., Miró, M., Puchol, J., & Fernández Suárez, F. E. (2009). Caso clínico: Rabdomiolisis, shock y arritmia en paciente crítica sedada. Revista Electrónica AnestesiaR, 1(11), 5. https://doi.org/10.30445/rear.v1i11.593
A continuación presentamos un caso clínico abierto a discusión. Como siempre, en 2-4 semanas (dependiendo de lo animado del debate) completaremos el caso con su resolución. Mientras tanto, os animamos a participar.
Caso clínico:
Mujer de 29 años, sin antecedentes de interés, con estudio preoperatorio normal, sometida a colecistectomía laparoscópica. Se reinterviene a las 24 h por hematoma hepático y hemoperitoneo, colocándose un packing abdominal. En las 24 h siguientes persiste abundante débito por drenajes abdominales y es necesaria politransfusión de hemoderivados (concentrados de hematíes, plasma, plaquetas, fibrinógeno, factor VII activado). En la monitorización hemodinámica con catéter de Picco (Pulsion Medical System® ) destacan Indice cardiaco (IC) 3.71 (normal 3-5) L min-1 m-2 , Volumen global diastólico indexado (GEDI) de 352 ml m-2 (normal 680-800), Volumen de sangre intratorácico indexado (ITBI) 439 ml m-2 (normal 850-1000), Variación de volumen sistólico 16% (normal <10%), índice de resistencias vasculares sistémicas (IRVS) 1866 dyn seg cm-5 m-2 (normal 1700-2400), por lo que es necesaria nueva laparotomía a las 24 h de la segunda intervención. Ante la persistencia del hematoma hepático, se realiza nuevo packing, que es posible retirar 48 h después, tras evidenciarse ausencia de sangrado.
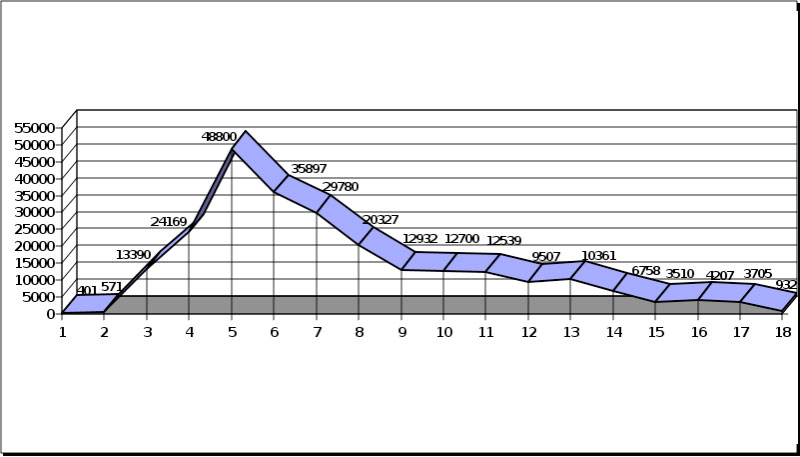
En Reanimación permanece sedada con perfusión de propofol al 2%, a una media de 5.3 (rango 2-8) mg kg-1 h-1 durante 87 h y analgesia con perfusión contínua iv de morfina a 1 mg h-1 (mantenimientos anestésicos intraoperatorios con sevoflurano). Hemodinámicamente continúa con parámetros de shock con componentes hipovolémico y, sobre todo, distributivo (IC 3.94- 5.7, GEDI 570-720, ITBI 710-890, IRVS 857-1400), a pesar de resucitación enérgica con volumen, requiriendo perfusión de noradrenalina a una media de 23 (rango 16-50) mcg min-1 durante 92 h. Se mantienen valores de presión arterial media ≥ 65 mmHg durante toda la evolución. Recibe perfusión iv de hidrocortisona durante 2 días (300 mg en 24 h); se inicia el tercer día de estancia en reanimación, al no poder descartar en este momento un componente séptico del shock distributivo. La creatinina fosfoquinasa (CPK) comienza a elevarse a las 48 h del inicio del cuadro , hasta un máximo de 48800 U L-1 el 5ºdía (figura 1), CPK-MB máxima 727 U L-1.

A las 87 h del ingreso en Reanimación , la paciente presenta bruscamente fibrilación auricular (FA) con respuesta ventricular rápida, bloqueo de rama izquierda y alteraciones secundarias de la repolarización compatibles con IAM anteroseptal (IC 2.4-5.35, IRVS 1100-1300, con noradrenalina a 15 mcg min-1, PA 105-110/40-60 mmHg). Alcanzó un pico de troponina T de 0.38 ng mL-1 (normal ≥0.1 ng mL-1). El ecocardiograma descartó defectos de la contractilidad ventricular.
Ante la sospecha de un cuadro clínico determinado se realiza una actuación (pregunta 1). Además se inicia bloqueo β1 adrenérgico, antiagregación, y amiodarona (bolo, seguido de perfusión continua -600mg/24 h-); tras 10 horas se normalizan el ECG y la troponina, permitiendo retirada de noradrenalina. Cuatro días después negativiza ondas T de V1 a V4, sin elevación enzimática, arritmias o necesidad de aminas.
En cuanto al estado ácido-base y electrolítico, la paciente presenta moderada acidosis metabólica (exceso de bases (EB) -7, pH 7.26). El K sérico y la función renal se mantienen normales y la acidosis revierte en el contexto de poliuria forzada para protección renal frente a la mioglobinuria (aporte de volumen iv, alcalinización de la orina y bajas dosis de furosemida).
Las pruebas de función hepática están alteradas (predominando citólisis, con GOT y GPT 12 veces el valor superior de la normalidad); bilirrubina hasta 2.7 mg dL-1.
La paciente permanece afebril y los cultivos microbiológicos seriados son negativos. Recibe tratamiento empírico con piperacilina-tazobactam durante 7 días.
La paciente presenta polineuropatía del paciente crítico, y que condiciona un destete prolongado de la ventilación mecánica. Se efectúa traqueostomía percutánea al 7º día de la intubación orotraqueal. El electromiograma y biopsia muscular realizados el día 8 de estancia en Reanimación (CPK 29780 U L-1, lentamente en descenso),no aportan resultados concluyentes. Se consigue la desconexión de la ventilación mecánica con éxito el día 14 y alta a la zona de hospitalización el día 20, con evolución posterior favorable.


1-Posible Sindrome de infusión prolongada de propofol con fallo cardiogénico??Retirada de propofol y paso a distinto hipnótico. Alcalinización de orina y aumento de fluidoterapia.
2-Diagnóstico diferencial con Shock Séptico, (si bien el fallo cardiogénico sería de una fase avanzada), Hepatitis tóxica , y creo que un analisis de trigliceridos en sangre podrían aportarnos datos.
3-Uhm..Debemos prestar atención a los signos de alarma, cambio del patrón hemodinámico, vigilar perfusiones de hipnóticos y valorar según el estado del paciente el tipo de sedación que debemos realizar.
Sorry creo que mi aportación es muy pobre.
Hola . No he contestado antes para no desvelar la respuesta a pocos días de publicado el caso .
Efectivamente se trataba de un síndrome de infusión por propofol .
Nos parecen muy acertados vuestros comentarios sobre el diagnóstico diferencial , pues es el mismo proceso que nos planteamos cuando sucedió el caso .
Me parece especialmente acertado el comentario de Miguel Miró , sobre todo en cuanto al uso del propofol como sedación .
La reflexión que queriamos hacer es que en muchos pacientes utilizamos dosis muy elevadas de propofol ( recordar que en la mayoría de las unidades se emplea al 2 % ) , y que en muchas ocasiones es la enfermeria la que manipula la sedación , subiendo el ritmo del fármaco si el paciente está desadapatado .
Muchas gracias por vuestros comentarios pues nos han enriquecido .
1.- El Síndrome de Infusión de Propofol (PRIS son las siglas en inglés) se define como bradicardia aguda resistente al tratamiento que puede progresar a asistolia asociado a la presencia de una infusión de propofol. La bradicardia se combina con aumento de los lípidos plasmáticos, esteatosis hepática, acidosis metabólica y rabdomiolisis o mioglobinuria. Otros síntomas y signos típicos del cuadro son: hipotensión, arritmia, fallo cardiaco, renal y circulatorio, elevación sérica de la CPK, lactato, urea y potasio.
Los hallazgos anatomopatológicos encontrados son citolisis de células musculares esqueléticas y cardiacas y la fisiopatología parece estar relacionada con una interacción del propofol con la cadena respiratoria mitocondrial.
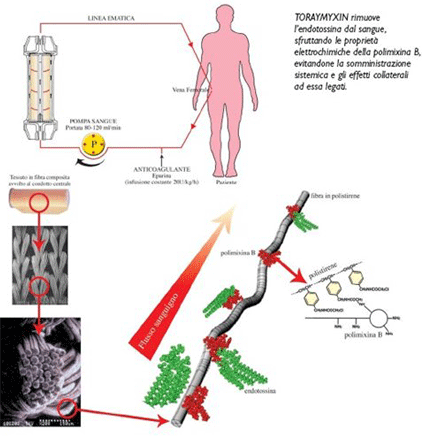
El tratamiento es suspender la perfusión de propofol, estabilización hemodinámica y aporte de carbohidratos. Se ha utilizado oxigenación con membrana extracorporea en dos casos con éxito. La hemodiálisis y la hemofiltración también están indicadas para eliminar el propofol y sus metabolitos.
2.- Las alteraciones en el ECG como el BRI y la elevación del ST en precordiales derechas (V1-V3) son típicas de este síndrome y se debe hacer diagnóstico diferencial con un IAM, la elevación de las troponinas en este contexto me parece poco específico para diagnosticar IAM y además el ecocardio descarta defectos segmentarios de la contractilidad por lo que en este caso no parece tratarse de un IAM.
El shock distributivo que presenta la paciente obliga a descarta un shock séptico, en este caso no hay signos de infección (no hay fiebre y los cultivos son negativos).
Hay que descartar otras causas de citolisis hepática y rabdomiolisis en el paciente crítico.
Los factores de riesgo que se han identificado para este síndrome son: infección respiratoria, TCE, dosis de propofol>5mg/kg/h durante más de 48 horas, niveles altos de catecolaminas y glucocorticoides en plasma y bajo aporte energético.
3.- La reflexión que yo haría es que hay que conocer la existencia de este síndrome, sus manifestaciones y su prevención (ya que una vez instaurado la mortalidad es elevada y el tratamiento poco efectivo). La prevención se basa en limitar la dosis de propofol a 4mg/kg/h en adultos no más de 7 días; combinar el propofol con otros fármacos sedantes para evitar escalar dosis (por ejemplo el remifentanilo); monitorizar pH, CPK y lactato durante su uso; asegurar una correcta oxigenación, estabilidad hemodinámica y aporte de glucosa.
Hay que recordar también que aunque es ampliamente utilizado, el uso del propofol para sedación en UCIs pediátricas no está aprobado y que existen recomendaciones de no usarlo en niños menores de 16 años para sedación.
Fudickar A, Bein B. Propofol infusion syndrome: update of clinical manifestation and pathophysiology.
Minerva Anestesiol. 2009 May;75(5):339-44
Miguel Miró
FEA del Servicio de Anestesiología y Reanimación
Hospital Universitario Fundación Alcorcón (Madrid)
1- Inicialmente parece un cuadro hipovolémico, seguido de un patrón hiperdinámico probablemente en el contexto de un SRIS por la politransfusión, cirugías repetidas, etc. Sin embargo, la aparicón de una rabdomiolisis y de un cuadro coronario en una mujer de 29 años debe hacernos pensar en otros diagnósticos y el síndrome por infusión de propofol encaja bastante, salvo quizás que no hubo una acidosis láctica importante, ni alteraciones renales, aunque no siempre aparece el cuadro completo
2- Cuando se objetivó un patrón hiperdinámico debería hacerse un diagnóstico diferencial con una sepsis.
El cuadro cardiaco es muy raro en una mujer joven y aunque de entrada en lo primero que se piensa es en un problema coronario debería tenerse en cuenta que podría ser compatible también con una miocarditis y que asociada a una alteración importante de las pruebas de función hepática debería obligarnos a descartar causas infecciosas, alérgicas, fármacos, etc
Los factores que favorecen el síndrome por infusión de propofol son:
Utilización durante mas de 2 ó 3 días de dosis > 5 mg/kg/h, uso cocomitante de catecolaminas y cortocoides (todo ésto aparece en el caso descrito)
3- La reflexión que puedo hacer es que cunado en un paciente crítico aparece un cuadro clínico abigarrado con síntomas que no parecen ser normales para el problema de base del paciente, sobre todo cuando se afectan órganos que no se relacionan con la agresión inicial, además de descartar infecciones y cuadros inflamatorios que son muy frecuentes, debemos pensar también en reacciones medicamentosas ya que son pacientes que habitualmente reciben gran cantidad de fármacos
Lo primero que quiero realizar es felicitar a los ponentes
En lo que refiere al diagnóstico inica me parecen acertados las opciones inciales de shock distributivo secundario a probable SIRS por poltransfusión El componente séptico no se puede descaratar de hecho a pesar de la ausencia de fiebre y leucocitosis dado que puede estar asociado a un estado de inmusupresión relativa. Los test de procalcitonina cualitativos y los valores de prot c reactiva nos ayudarían quizás a dilucidar el origen
Aunque presentan muchos de los factores de riesgo para presentar el síndromey creo que es la etiología más probable, pienso necesario descartar otras etiiologías más si cabe cuando no se medían triglicéridos plasmáticos y la biopsia es inespecífica ( reacciones medicamentosas, isquemia hepática transitora en contexto de bajo gasto,cirugía disfunción miocárdica asociada a sepsis … )
Quería añadir la necesidad de limitar a utilización de propofol en tiempo y la conveniencia de asociar otros sedantes. Cuando el paciente esté inestable hemodinámicamente en etapas precoces con dosis altas de aminas, una asocación con midazolam y morfina por ejemplo, puede condiconar mayor estabilidad hemodinámica y ser más útil que el propofol, si no se va a realizar una ventana neurológica En fases posteriores la isquemia muscular se minimiza y el propofol podría resultar muy úti entonces
Gracias y felices fiestas
,