Rey Vázquez, S. M. 1 , Marcos Vidal, J.M. 2, Echevarría Blasco, N. 1, Higuera Miguélez, E. 2, Ferrero de Paz, J. 1, Bermejo González J.C. 3
1 Médicos residentes de Anestesiología y Reanimación.
2 Facultativos especialistas en Anestesiología y Reanimación. en Complejo Asistencial Universitario de León.
3 Jefe de Servicio de Anestesiología y Reanimación.
Complejo Asistencial Universitario de León.
Introducción
La reparación abierta de aneurisma de aorta presenta alta mortalidad. La cirugía abierta de aneurisma toracoabdominal tiene una mortalidad del 6,6%, una incidencia de lesión medular del 4%, importante morbilidad y deterioro en la capacidad funcional (1).
En el año 1991, Parodi publicó el uso de endoprótesis para la corrección de patología aórtica aneurismática (2), y desde entonces los avances en las técnicas endovasculares han permitido ofrecerla como alternativa para aquellos casos con alto riesgo quirúrgico. Los datos presentados por The United Kingdom EVAR Trial Investigators (EVAR 1) en 2004 revelan una disminución de mortalidad a 30 días en la reparación endovascular de aneurisma abdominal de un 1,8% frente al 4,3% de la cirugía abierta (3).
Los abordajes híbridos de la patología aórtica toracoabdominal surgen tras el avance de los procedimientos endovasculares, con la intención de reducir la agresividad en cirugía abierta, asociando la revascularización extraanatómica y colocación de la endoprótesis. De esta forma, se garantiza flujo a áreas anatómicas que de otra manera quedarían sin vascularización como consecuencia del implante.
La coartación de aorta es una cardiopatía congénita con una incidencia del 6-8%, predominante en hombres, y que asocia hasta en un 40% válvula aórtica bicúspide. Habitualmente la coartación aparece inmediatamente distal a la salida de la arteria subclavia izquierda, opuesta al ductus arterioso y en otras ocasiones es una coartación circunferencial. Tras la corrección quirúrgica en la infancia, los pacientes pueden llegar a la edad adulta con HTA residual, disfunción ventricular izquierda, disfunción valvular aórtica, recoartación y aneurismas. La patología aneurismática tras reparación quirúrgica de la coartación tiene una incidencia entre 5-15% según las series publicadas, y es el resultado de una anormalidad estructural de la pared arterial. Sus indicaciones quirúrgicas fundamentales son: tamaño (diámetro >5,5 cm.), velocidad de crecimiento (>1 cm. anual), la presencia de síntomas compresivos como disfagia o disfonía, o datos de disección. Actualmente de acuerdo a las características anatómicas de la lesión, comorbilidad del paciente y experiencia del centro hospitalario, el abordaje puede ser abierto, híbrido o endovascular (4, 5).
Descripción del caso
Varón de 35 años con coartación de aorta, intervenido a los 13 años mediante parche de ampliación en diamante de Velour Dacron albuminado, con HTA secundaria tratado con Atenolol. Antecedente de hematoma intraparenquimatoso cerebral espontáneo, dos años antes, resuelto sin cirugía, con hemiparesia y hemihipoestesia leve de miembro superior izquierdo. Presenta en AngioTAC de control aneurisma sacular sobre coartación aórtica postductal de 49×53 mm. de diámetro máximo con datos de ulceración; el ecocardiograma muestra válvula aórtica trivalva normofuncionante y función sistólica conservada. Según estos datos, se programa para reparación endovascular y cierre de arteria subclavia izquierda con revascularización carótido-subclavia izquierda.
El estudio preoperatorio presenta una exploración normal, pruebas complementarias sin hallazgos patológicos y en AngioTAC cerebral se observa comunicante anterior, pero no demuestra con claridad comunicantes posteriores del Polígono de Willis, las arterias vertebrales son hipoplásicas y presenta una arteria basilar de pequeño calibre. Se premedica con Lorazepam 1 mg y Omeprazol 20 mg vo, y se realiza profilaxis antibiótica con Cefazolina 2 g iv al llegar a quirófano.
En el quirófano se monitoriza al paciente con ECG, Sat O2, ETCO2, índice biespectral, oximetría cerebral regional con INVOS„¢, y sondaje urinario para control de diuresis. Se canaliza en vena yugular interna derecha vía central trilumen e introductor de CAP por el que se introduce marcapasos endocavitario (MCPE); se canalizan ambas arterias radiales, con monitorización de la presión arterial para controlar la presión de perfusión cerebral en los momentos de clampaje carótido-subclavio y la perfusión sistémica a través de la presión en la arteria femoral izquierda. El cardiólogo hemodinamista canaliza la arteria femoral derecha para el procedimiento endovascular. La inducción se realiza con Etomidato 2 mg.Kg-1, MDZ 0,02 mg.Kg-1, Fentanilo 5 mcg.Kg-1 y Cisatracurio 0,2 mg.Kg-1. El mantenimiento se hace con Sevoflurano y Remifentanilo, según profundidad anestésica.
En la primera parte del procedimiento se realiza la revascularización carótida izquierda-subclavia izquierda mediante injerto de Dacron de 8 mm, con cierre de flujo proximal de la arteria subclavia mediante implante de tapón vascular Amplatzer ll de 14 mm. Durante los 20 minutos de clampaje de la arteria carótida izquierda la tendencia del INVOS„¢ se mantienen estable con respecto a las cifras basales. Posteriormente se implantan dos endoprótesis Gore de 21 mm x 10 cm superpuestas desde la salida de arteria carótida izquierda hasta 5 cm distales al aneurisma, con zona de solapamiento de 5 cm entre prótesis, mediante hipotensión controlada con MCP endocavitario, con una distancia total de endoprótesis en aorta descendente de 15 cm.
Durante todo el procedimiento el paciente se mantiene estable hemodinámicamente sin necesitar soporte inotrópico, vasopresor ni hemoterápico. Al finalizar la intervención se traslada a la Unidad de Reanimación sedado y en ventilación mecánica, donde es extubado a los 90 minutos, sin focalidad neurológica, función renal normal, sin sangrados ni hematomas a nivel de incisión cervical ni en punciones arteriales; a las 24 horas de su llegada es dado de alta a planta de hospitalización de Cirugía Cardiaca.
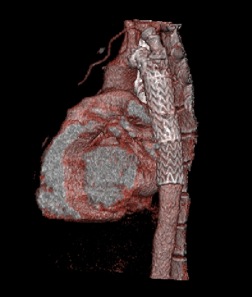
Figura 1: TAC (reconstrucción 3D) con endoprótesis aórtica y tapón vascular Amplatzer ll en arteria subclavia izquierda.
Discusión
El abordaje anestésico de la patología aneurismática postcoartación debe de abarcar todos los aspectos que son causa de complicaciones postoperatorias descritas en este tipo de intervenciones. La aparición de aneurismas tras reparación en esta cardiopatía es relativamente precoz, próxima a la cuarta década de la vida, en la que frecuentemente los pacientes conservan una adecuada reserva funcional, aunque la incidencia de HTA es de un 87% y la presencia de disfunción valvular es de un 12%, entre otros. Por tanto, debe de realizarse una valoración preoperatoria completa de acuerdo con la comorbilidad del paciente.
Las medidas de protección orgánica que incluyen actualmente las guías contemplan la profilaxis de la insuficiencia renal, protección cerebral y medular. La insuficiencia renal aparece en cirugía de aneurismas de aorta descendente en un 3-5% y puede verse agravada con el uso de contraste en el proceso endovascular, por lo que se recomienda hidratación con cristaloides y bicarbonato sódico a un ritmo de 100 ml.h-1. Los factores de riesgo de paraplejia en TEVAR incluyen la cirugía previa de aorta abdominal, aterosclerosis severa de aorta torácica, la hipotensión durante el procedimiento, lesión de la arteria iliaca externa, oclusión de la arteria subclavia izquierda durante el procedimiento y la longitud de la endoprótesis en la aorta torácica (>20 cm.); en nuestro caso la longitud de la prótesis no excedía los 15 cm. desde la raíz de la arteria subclavia izquierda, se usaron dos prótesis de 10 cm., con solapamiento de 5 cm., con una longitud total de 15 cm. En cuanto a la permeabilidad de la arteria subclavia izquierda, fue asegurada en el primer tiempo de la cirugía con el bypass carótido-subclavio, monitorizando el flujo en todo momento con la arteria radial izquierda y con un tiempo de clampaje de la arteria subclavia izquierda de 20 minutos. La monitorización de la oximetría cerebral se realizó con INVOS„¢, condicionados por su disponibilidad y experiencia de uso respecto a otros métodos, permitiendo evaluar en todo momento la integridad de la perfusión cerebral en un paciente con anomalías anatómicas y patología isquémica cerebral previa, no presentando ninguna incidencia durante el procedimiento (6). Para el implante de la endoprótesis se aplicó hipotensión controlada inducida por MCP endocavitario, generando una TV autolimitada, de corta duración recuperada en pocos segundos, garantizando una adecuada presión de perfusión en los tejidos inmediata. Existen fármacos hipotensores de vida media muy corta, como el nitroprusiato, nitroglicerina o la inducción de asistolia con adenosina a dosis altas, pero la recuperación de la presión arterial no es tan rápida como la observada tras el cese del estímulo del MCP.
Destacar la importancia de la planificación previa en estos procedimientos con abordaje multidisciplinar, para programar las actitudes a tomar, en previsión de posibles complicaciones durante el procedimiento, que obligarán al anestesiólogo a realizar estrategias altamente invasivas, a pesar de considerarse, desde el punto de vista quirúrgico procedimientos poco invasivos.
Bibliografía
1.- Coselli JS, Bozinovski J, LeMaire SA. Open surgical repair of 2286 thoracoabdominal aortic aneurysms. Ann Thorac Surg. 2007;83:S862-S64; discussion S90-S2. PubMed.
2.- Parodi JC, Palmaz JC, Barone HD. Transfemoral intraluminal graft implantation for abdominal aortic aneurysm. Ann Vasc Surg. 1991;5:491-99. PubMed.
3.- Greenhalgh RM, Brown LC, Kwong GP, Powell JT, Thompson SG EVAR Trial Participants. Comparison of endovascular aneurysm repair with open repair in patients with abdominal aortic aneurysm (EVAR trial 1), 30-day operative mortality results: randomised controlled trial. Lancet 2004;364:843-8. PubMed.
4.- Preventza O, Livesay JJ, Cooley DA, Krajcer Z. Coarctation-Associated Aneurysms: A Localized Disease or Diffuse Aortopathy. Ann Thorac Surg 2013;95:1961-7. PubMed.
5.- Roselli EE, Qureshi A, Idrees J, Lima B. Open, Hybrid, and Endovascular Treatment for Aortic Coarctation and Postrepair Aneurysm in Adolescents and Adults. Ann Thorac Surg 2012;94:751-8. PubMed.
6.- Hiratzka et al. 2010 Guidelines for the Diagnosis and Management of Patients with Thoracic Aortic Disease. Circulation 2010;121:e266-e369. PubMed.