Navarro Lago P (1), Fernández García A (2), Levstek M (2)
(1) Médico Residente Anestesiología y Reanimación en hospital 12 de octubre, Madrid.
(2) Médico Adjunto Anestesiología y Reanimación en hospital 12 de octubre, Madrid.
Cómo citar este artículo: Navarro Lago, P., Fernández García, A., & Levstek, M. (2020). Feocromocitoma: Cirugía urgente vs Cirugía programada. Revista Electrónica AnestesiaR, 12(10). https://doi.org/10.30445/rear.v12i10.861
Introducción
El manejo perioperatorio del feocromocitoma requiere un meticuloso plan anestésico debido a las complicaciones cardiovasculares potencialmente letales (IAM, fallo cardiaco, síndrome de takotsubo…), y precisa de la preparación del paciente al menos 2 semanas antes de la intervención pero ¿qué ocurre cuando el paciente no puede esperar ese tiempo?
La prevalencia de feocromocitomas y paragangliomas intraoperatorios incidentales es desconocida, pero históricamente se han asociado con una tasa de mortalidad de hasta el 40% (1). La incidencia de este tumor en población hipertensa es del 0.1% aproximadamente. (2)
El 90% de los feocromocitomas se producen espontáneamente y son benignos, mientras que en el 10% restante, el tumor suprarrenal es parte de un trastorno familiar. (3)
Caso Clínico
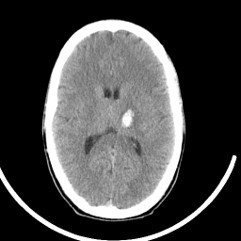
Se trata de un paciente de 24 años, sin alergias conocidas y sin antecedentes personales de interés que acude a urgencias por debilidad en extremidades derechas, a la exploración destaca tensión arterial (TA) de 167/90mmHg, sin otra focalidad neurológica además de la pérdida de fuerza. Se realiza TAC craneal donde se objetiva un hematoma de 20x13x15mm en ganglios basales izquierdos sin evidenciarse sangrado activo ni lesiones ocupantes de espacio (LOEs) ni malformaciones arteriovenosas (MAVs) (Imagen 1). Se decide ingreso en la Unidad de Ictus para monitorización y tratamiento. Rehistoriando al paciente y familiares, nos cuentan que desde hace unos meses presenta episodios de palpitaciones y cefalea sin rubor facial. Explica que tiene antecedentes familiares (su madre, su abuela y su bisabuela con sospecha de Neurofibromatosis tipo I, sin diagnóstico médico y prima materna con feocromocitoma intervenido.
Tras varias horas de ingreso, el paciente presenta deterioro neurológico (NIHSS 18) tras episodio de palpitaciones, se repite TAC craneal donde se evidencia aumento del hematoma de ganglios basales, con edema perilesional, apertura al sistema ventricular, y desviación de línea media hacia la derecha de 5 mm (Imagen 2), por lo que se decide intervención quirúrgica urgente para colocación de drenaje ventricular externo (DVE).
El paciente llega a quirófano con bajo nivel de conciencia (GCS 11), tendencia a HTA y taquicardia. Se canaliza arteria radial previa a la inducción, objetivándose TA:160/76mmHg, con taquicardia sinusal a 120lpm. Se administra lidocaína 1mg/kg, se realiza inducción de secuencia rápida y se inicia perfusión de remifentanilo y propofol para el mantenimiento, se inicia así mismo, perfusión de clevidipino a 4ml/h.
Tras la inducción presenta un pico hipertensivo de 220/82 mmHg por lo que se aumenta perfusión de clevidipino a 4 mg/h y se añade bolo de 1.5 gr de sulfato de magnesio. Tras esto, permanece estable hemodinamicamente hasta el final de la intervención donde vuelve a tener pico hipertensivo de hasta 210/90mmHg que se controla con bolo de urapidilo. Tras la intervención se traslada a UCI intubado y sedoanalgesiado.
El paciente precisa de 15 días de ingreso en UCI, con evolución favorable, TA de difícil control los primeros días, se inicia alfabloqueo. Se realiza TAC abdominal donde se objetiva masa adrenal derecha, se realiza también como parte del estudio un ecocardiograma trastorácico (ETT) en el que se describe Fracción de eyección del VI (FEVI) normal con hipertrofia moderada del ventrículo izquierdo (VI) y alteración de la relajación sin otros hallazgos significativos, por lo que se descarta miocardiopatía de estrés.
Al alta de la UCI el paciente mantiene hemiplejia derecha con afasia leve.
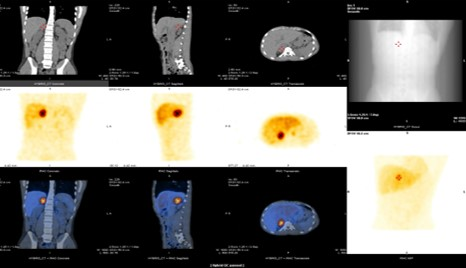
Se completa el estudio de feocromocitoma con RMN abdominal y del neuroeje (para descartar neurofibromas), Metanefrinas en orina (aumento en la cantidad de adrenalina, normetanefrina y metanefrina), Ratio renina/ aldosterona, doppler renal (sin hallazgos de estenosis de arterias renales), fondo de ojo (búsqueda de nódulos de Lisch) y rastreo con 123 I-MIBG donde se objetivó acúmulo patológico a nivel de glándula suprarenal derecha. (Imagen 3)
Se confirma el diagnóstico de feocromocitoma en el seno de neurofibromatosis tipo I (Diagnóstico clínico, pendiente de estudio genético).
Una vez confirmado el tumor, se propone para cirugía de resección vía laparoscópica.
Un mes y medio después, nos enfrentamos a una cirugía compleja con manipulación del tumor, pero conociendo el diagnóstico del paciente y habiendo realizado la preparación adecuada con doxazosina como alfabloqueador, amlodipino y betabloqueo con propanolol.
Con el paciente despierto se canalizó arteria radial, a continuación se realizó inducción con fentanilo, lidocaína, propofol, rocuronio y mantenimiento con sevofluorano. Se canalizó también vena yugular Interna. Tras la inducción y pneumoperitoneo presentó episodio de HTA de hasta 220/110 mmHg por lo que se administraron 25 mg de urapidilo y se inició perfusión de clevidipino a 2 mg/h, que se tuvo que aumentar hasta 6 mg/h para mantener una TA adecuada.
Durante el resto de la intervención se mantuvo con perfusión de clevidipino entre 2 – 6 mg/h, precisando 3 bolos de 20 mg de esmolol.
Tras la escisión de la glándula suprarrenal derecha se pudo retirar la perfusión de clevidipino y no precisó de fármacos vasoconstrictores permaneciendo con una TAM>65mmHg, diuresis adecuada durante toda la intervención y manteniendo glucemia en rango. El paciente se extubó en quirófano sin incidencias e ingresó en la Unidad de Reanimación, donde permaneció las 48 horas siguientes para vigilancia estrecha.
Discusión
Los feocromocitomas son tumores de tejido cromafín que sintetizan catecolaminas. Su manejo es siempre un reto para el anestesista, más aún cuando el paciente se encuentra en una situación de emergencia y ni el paciente ni el anestesista están preparados para la intervención.
Según algunas estimaciones del 25 al 50% de las muertes de pacientes con feocromocitoma desconocido o no preparado ocurrieron durante la inducción de la anestesia o durante intervenciones por otros motivos. (4)
La resección quirúrgica del tumor es el único procedimiento curativo, por lo que será inevitable el paso por quirófano.
Cirugía emergente
En este caso nos encontramos ante una neurocirugía urgente en un paciente con sospecha de feocromocitoma (crisis hipertensiva, historia de cefalea, palpitaciones e historia familiar), por lo que ante la sospecha debemos tratarlo como tal. Es la crisis hipertensiva lo que ha llevado a nuestro paciente a la situación actual, por lo que el control estricto de la tensión es obligatorio. Por este motivo se monitorizó la presión arterial continua con el paciente despierto ya que las crisis adrenérgicas que conducen a una situación de inestabilidad hemodinámica ocurren principalmente durante la inducción de la anestesia, intubación, instauración del pneumoperitoneo y durante el manejo del tumor (en la cirugía de resección). (5,6,7,8, 9). Se monitorizó también ECG, saturación periférica de oxígeno y profundidad anestésica con BIS.
Se administro lidocaína en la inducción para disminuir la respuesta hemodinámica a la intubación. Se eligió propofol como agente de mantenimiento ya que ayuda a reducir el flujo sanguíneo cerebral, la presión intracraneal, el volumen sanguíneo cerebral y el metabolismo cerebral, manteniendo así la autorregulación cerebral (10), por esto se ha considerado clásicamente el agente de elección en neurocirugía.
Pese a nuestras precauciones el paciente presentó crisis hipertensivas en el intraoperatorio. Hay que tener en cuenta que el bloqueo beta no debe instaurarse hasta que el bloqueo alfa esté completamente instaurado, debido al potencial riesgo de aparición de crisis hipertensivas por estimulación sin oposición de los receptores alfa. Como nuestro paciente no estaba premedicado con alfabloqueantes, iniciamos perfusión de clevidipino (bloqueante de los canales de calcio que muestra selectividad por la vasodilatación arteriolar, de rápido inicio y fácilmente titulable). Utilizamos así mismo un bolo de sulfato de magnesio (vasodilatador que actúa inhibiendo la liberación de catecolaminas e inhibe los receptores de catecolaminas).(11,12,13)
Cirugía programada
Antes de la intervención, es imperativo restaurar la volemia y controlar la presión arterial, la frecuencia cardíaca y las arritmias. El manejo médico preoperatorio disminuye drásticamente la morbimortalidad durante el manejo quirúrgico del feocromocitoma. La preparación preoperatoria se realiza convencionalmente con un bloqueo alfa adrenérgico durante un período de 10 a 14 días y, posteriormente, se requiere un bloqueo beta adrenérgico adicional para tratar cualquier taquiarritmia asociada. (3,14)
La sedación y la ansiolisis preoperatorias, preferiblemente con una benzodiazepina, disminuirán la ansiedad y prevendrán una marcada fluctuación hemodinámica en el período preoperatorio inmediato.
De nuevo debe monitorizarse la presión arterial de forma invasiva desde antes de la inducción, ya que se pueden presentar crisis hipertensivas en la misma. Además, en este caso, debe canalizarse un acceso venoso central, dado que tras la ligadura de la vena suprarrenal se puede producir una hipotensión que precise de drogas vasoactivas.
La resección del tumor se puede dividir en dos fases, la previa a la ligadura del flujo sanguíneo del tumor y la posterior, siendo en ambas indispensable una estrecha comunicación con el equipo quirúrgico para poder anticiparnos a los cambios hemodinámicos. La primera fase se caracteriza por episodios de hipertensión severa, especialmente en momentos como la intubación, insuflación del neumoperitoneo y durante la manipulación del tumor, mientras que en la segunda fase, prevalece la hipotensión arterial. (15,16)
Para el control de la hipertensión arterial previa a la resección del tumor se pueden utilizar distintos tipos de fármacos:
Clásicamente, tenemos el nitroprusiato de sodio, que es un potente arteriovenodilatador con una acción rápida y breve. Con la pequeña cantidad utilizada, la toxicidad por cianuro es improbable.
La fentolamina, también se puede usar intraoperatoriamente para controlar las crisis hipertensivas agudas porque actúa con rapidez y tiene una vida media corta. Su principal problema es la disponibilidad, ya que no se encuentra disponible en todos los centros. (1,3,14)
En este caso, se optó por el uso de clevidipino, un nuevo antagonista del calcio intravenoso con inicio de acción rápido y vida media corta que no tiene efecto residual y no causa hipotensión tras la resección tumoral, por lo que puede ser un fármaco de primera elección esta cirugía. (17)
El uso intraoperatorio de antagonistas beta adrenérgicos como el esmolol puede ayudar a controlar la taquicardia y las taquiarritmias. Su efecto rápido y corta duración lo hace fácilmente titulable, tanto para controlar la frecuencia cardíaca como la presión arterial.
Tras la ligadura de las venas suprarrenales, comienza la segunda fase de la cirugía, hay un descenso repentino en las catecolaminas circulantes que puede conducir a hipotensión arterial. En este punto, los vasodilatadores y los beta bloqueantes deben interrumpirse y puede ser necesario el inicio de vasopresores.
Una vez finalizada la intervención y tras la extubación, el paciente debe recibir una vigilancia estrecha en una Unidad de Reanimación.
Las tres complicaciones más importantes en el postoperatorio inmediato son la hipertensión, la hipotensión y la hipoglucemia. Aproximadamente el 50% de los pacientes permanecen hipertensos durante unos días, lo que probablemente esta en relación con niveles elevados de catecolaminas que pueden persistir hasta una semana después de la resección del feocromocitoma. Debe considerarse la persistencia de tumor residual en casos de hipertensión arterial persistente tras diez días desde la resección del mismo. La hipotensión arterial persistente puede deberse al efecto residual del bloqueo adrenérgico preoperatorio.
Tras la extirpación del tumor, desaparece la supresión de las células pancreáticas beta, por lo que aumentan los niveles de insulina. Igualmente, la lipólisis y gluconeogénesis están ausentes. Todo esto puede conducir a la aparición de hipoglucemias y al consecuente desarrollo de encefalopatía (18).
“Es por la posible aparición de estas complicaciones por lo que el paciente debe permanecer 48h en una Unidad de Reanimación. En nuestro caso, esta estancia transcurrió sin incidencias y el paciente se fue de alta a planta tras ese periodo.
Conclusiones
Dada la elevada morbi- mortalidad intraoperatoria, ante la mínima sospecha de la presencia de un feocromocitoma en un paciente, este debe tratarse como si así fuera.
Se debe hacer especial hincapié en la importancia de una meticulosa preparación preoperatoria. Introduciendo el alfabloqueo en el momento y durante el tiempo necesario, sin iniciar el betabloqueo hasta que el alfa esté completamente instaurado. Además, restaurar la volemia y controlar la presión arterial, la frecuencia cardíaca y las arritmias.
Es indispensable una estrecha comunicación con el equipo quirúrgico para poder anticiparnos a los cambios hemodinámicos en las diferentes fases de la cirugía.
Dada la variedad de antihipertensivos disponibles, es recomendable trabajar con aquellos con los que el equipo esté más familiarizado.
Bibliografía
1- Hariskov S, Schumann R. Intraoperative management of patients with incidental catecholamine producing tumors: a literature review and analysis. Journal of Anaesthesiology Clinical Pharmacology. 2013;29:41–46. (PMC)
2- Benowitz NL. Pheochromocytoma-recent advances in diagnosis and treatment. West J Med. 1988;148:561–7. (PubMed)
3- Ahmed A. Perioperative Management of Pheochromocytoma: Anaesthetic Implications. J Pak Med Association. 2007;57 :3. (PubMed)
4- Hayıroğlu M, Yıldırımtürk O, Bozbay M. Hypertensive emergency due to pheochromocytoma crisis complicated with refractory hemodynamic collapse. Turk Kardiyol Dern Ars 2015;43(8):727-729. (PubMed)
5- Kakoki K, Miyata Y, Shida Y, Hakariya T. Pheochromocytoma multisystem crisis treated with emergency surgery: a case report and literature review. 2015 8: 758. (PMC)
6- Abhijit L, Lakireddy V, Gorbachov S, Chaikittisilpa N, Krishnamoorthy V, Vavilala MS. A Narrative Review of Cardiovascular Abnormalities After Spontaneous Intracerebral Hemorrhage. Jorney of Neurosurgery Anesthesiology 2019;31:199–21. (PubMed)
7- Jean L. Joris, M, Etienne E, Hamoir, MD. Hemodynamic Changes and Catecholamine Release During Laparoscopic Adrenalectomy for Pheochromocytoma. Anesthesia and Analgesia. 1999;88:16–21. (HTML)
8- Kercher KW, Novitsky YW, Park A. Laparoscopic curative resection of phochromocytomas. Ann Surg 2005; 241:919. (PMC)
9- Rocha F, Faramazi – Roques R. Laparoscopic surgery for pheochromocytoma. Eur Urol 2004; 45: 226. (HTML)
10- Cenic A, Craen RA, Lee TY, Gelb AW. Cerebral blood volume and blood flow responses to hyperventilation in brain tumors during isoflurane or propofol anesthesia. Anesth Analg 2002; 94:661. (PubMed)
11- Houston M: The role of magnesium in hypertension and cardiovascular disease. J Clin Hypertens (Greenwich) 13:843-847, 2011. (PubMed)
12- Michael S. Perioperative Management of Pheochromocytoma: Focus on magnesium, clevidipine and vasopressin. Jornal of Cardiothoracic and vascular anesthesia. 202; 26: 526-531.
13- Siddiqi HK, Yang HY, Laird AM, Fox AC, Doherty GM, Miller BS et al. Utility of oral nicardipine and magnesium sulfate infusion during preparation and resection of pheochromocytomas. Surgery 2012; 152:1027. (PubMed)
14- Naranjo J, Dodd S, Martin YN. Perioperative Management of Pheochromocytoma. J Cardiothorac Vasc Anesth 2017; 31:1427.
https://www-uptodate-com.m-hdoct.a17.csinet.es/contents/anesthesia-for-the-adult-with-pheochromocytoma/abstract/43 (PubMed)
15- Weingarten TN, Welch TL, Moore TL, Walters GF, Whipple JL, Cavalcante A et al. Preoperative Levels of Catecholamines and Metanephrines and Intraoperative Hemodynamics of Patients Undergoing Pheochromocytoma and Paraganglioma Resection. Urology 2017; 100:131. https://www-uptodate-com.m-hdoct.a17.csinet.es/contents/anesthesia-for-the-adult-with-pheochromocytoma/abstract/44 (PubMed)
16- Wu S, Chen W, Shen L, Xu L, Zhu A, Huang. Risk factors for prolonged hypotension in patients with pheochromocytoma undergoing laparoscopic adrenalectomy: a single-center retrospective study. Sci Rep 2017; 7:5897. (PubMed)
17- García C, Arbonés E, Teixell C, Lorente-Poch L, Trillo-Urrutia L. Clevidipine for hypertension treatment in pheochromocytoma surgery. Revista Española de Anestesiología y Reanimación 2018; 65:225-228 (PubMed)
18- Fleisher L, Mythen M. Anesthetic implications of concurrent diseases. In: Miller’s Anesthesia, 8th ed, Miller RD, Cohen NH, Eriksson LI, et al (Eds), Elsevier, Philadelphia 2015. p.1170.






Muchas gracias por este aporte tan interesante.