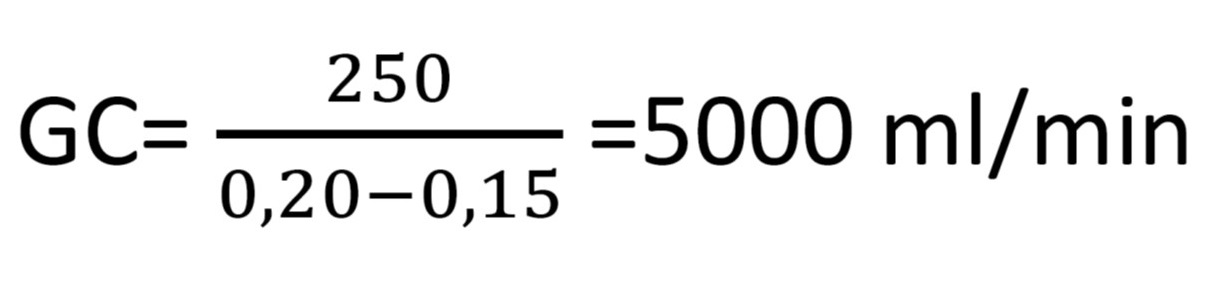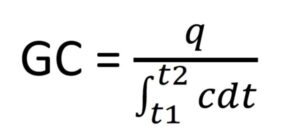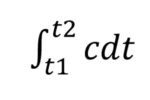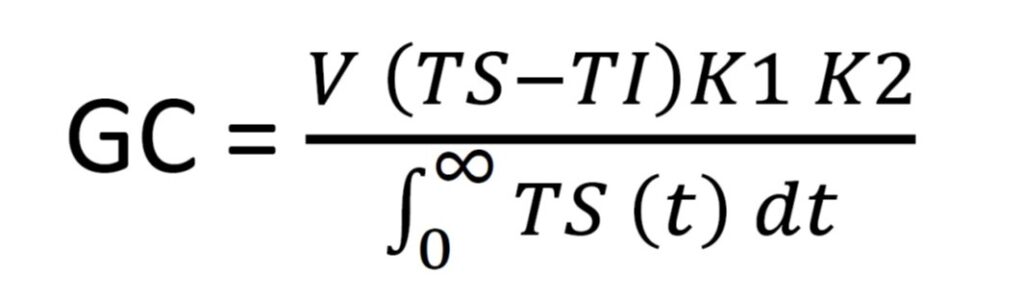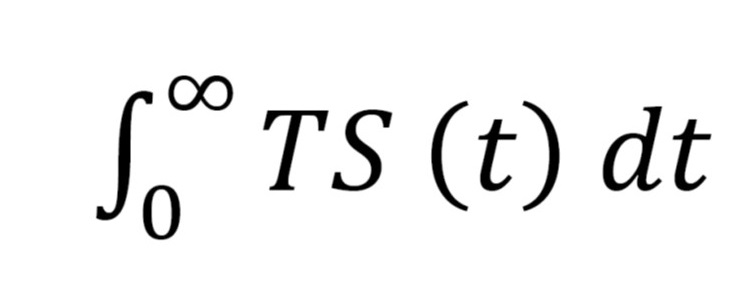Paz Martín D (1), Dalmau R (2), Rioja Corroto E (3), Castaño Moreira B (4)
(1) Jefe de Sección Anestesiología y Reanimación Complejo Hospitalario de Toledo.
(2) Departamento de Anestesiología, Hospital Español de Rosario, Rosario, Argentina
(3) Médico Interno Residente de Anestesiología y Reanimación, Hospital Universitario de Toledo, Toledo, España.
(4) Unidad de Cuidados Críticos Cardiacos, Hospital Universitario de Toledo, Toledo, España
Cómo citar este artículo: Paz Martín, D., Dalmau, R., Rioja-Corroto , E., & Castaño-Moreira , B. (2023). Principio de Fick en la determinación del Gasto Cardiaco. Revista Electrónica AnestesiaR, 14(12). https://doi.org/10.30445/rear.v14i12.1086
Introducción
Un aspecto clave en la evaluación del estado hemodinámico del paciente es la monitorización del gasto cardiaco (GC). Su determinación ofrece una aproximación al estado circulatorio global, por lo que es uno de los parámetros cardiovasculares estándar en el manejo de pacientes críticamente enfermos o de alto riesgo.
No obstante, la medición del GC en la medicina clínica (en especial en la medicina perioperatoria e intensiva), ya sea por métodos directos o indirectos, es y ha sido históricamente relegada por dos motivos principales.
El primero de ellos es el uso cotidiano y rutinario de la presión arterial (Pa), dada su evidente accesibilidad, datando la primera medición directa del año 1727 por el reverendo Stephan Hales (1). Sin subestimar la importancia de la Pa como variable hemodinámica, el principal problema de su uso en la clínica—y particularmente en relación a la interpretación de la perfusión de un paciente— es que podría llegar a asumirse que la Pa guarda una relación lineal, o directamente proporcional, con el GC, lo cual implicaría que una podría ser inferida en base a la otra. Esta interpretación es, en pocas palabras, errónea: no hay tal cosa como una relación «universal», y que pueda conocerse, entre ambas variables en la circulación intacta.
El segundo motivo es más contemporáneo y complejo, y tiene que ver con el lugar que esta variable ha ido adquiriendo en la práctica clínica tras el advenimiento y auge de diferentes metodologías para el manejo hemodinámico. El campo de la “hemodinamia funcional” con su vasto universo de variables conocidas como “dinámicas” (derivadas de la fluctuación respiratoria del volumen sistólico), ha crecido en atractivo dada su incorporación a tecnologías mínimamente o no invasivas, así como por su capacidad predictiva de la “respuesta a fluidos”, lo que ha llevado a algunos autores no sólo a olvidarse del GC, sino a recomendar su desuso (2).
Lo que estos dos motivos someramente presentados tienen en común es, como decíamos, el olvido y desplazamiento del GC del arsenal actual para la monitorización hemodinámica. En el primer caso, a través de su reemplazo «tácito» por la Pa, cuya relación con el GC en un paciente y momento dado nunca puede conocerse. Y en el segundo caso, por una cuestión de atractivo y desvío de la atención hacia otros fenómenos hemodinámicos.
Poco importa para los objetivos de este trabajo que el catéter de arteria pulmonar (CAP)—basado en el método de Fick—haya caído en desuso en quirófano y en el paciente crítico general (3,4), quedando restringido a pocas indicaciones como el paciente que requiere cuidados intensivos cardiacos. Sólo cuando se conoce un proceso se puede intervenir en él, por eso lo largo de las siguientes líneas se abordarán las bases biofísicas de la determinación del GC con CAP.
Principio de Fick
En 1870 Adolf Eugen Fick, un fisiólogo alemán, presentó en la Sociedad Físico-Médica de Würzburg el primer método para medir el GC. En la charla, el propio Fick, se asombraba de que no se hubiera desarrollado antes “Es sorprendente que nadie haya llegado al siguiente método obvio con el que (la cantidad de sangre eyectada por el corazón en cada sístole) podría ser determinado directamente…”.
Postuló que el oxígeno captado por los pulmones se transfiere íntegramente a la sangre, y que se puede calcular el GC conociendo el oxígeno consumido por el organismo y la diferencia de esta molécula entre la sangre arterial y la venosa mixta.
La base de este método es una aplicación de la Ley de Conservación de la Masa, según la cual la tasa de flujo volumétrico de entrada y salida en cierto volumen de control es constante para un fluido incompresible, como la sangre. La cantidad de fluido que entra por un conjunto de tuberías (por un punto A) debe ser igual a la que sale por un punto B, a menos, que se modifique la densidad del fluido o se pueda aumentar el volumen de los tubos a través de la expansión de unas paredes flexibles.
Esquemáticamente se puede explicar el principio de Fick de la siguiente forma: la sangre oxigenada fluye a los diferentes órganos. Estos órganos extraen un porcentaje del O2, por lo tanto, la sangre que vuelve de los mismos transporta menos cantidad que el sistema arterial, generando una diferencia arterio-venosa en la concentración de O2. Fick llegó a la conclusión de que, como se expresa en la siguiente ecuación, el oxígeno consumido por lo tejidos periféricos debe ser igual al producto del flujo sanguíneo (gasto cardiaco) y el cambio de concentración de oxígeno entre el sistema arterial y venoso. O dicho de otra manera, conociendo la cantidad de oxígeno consumido y el cambio de concentración en un volumen determinado de sangre (ej. 1 litro) se puede saber cuánto flujo debe dirigirse a los tejidos para alcanzar la diferencia observada.
Consumo de oxígeno (VO2) = Gasto cardiaco x diferencia arteriovenosa de oxígeno (ec. 1)
Este mismo principio puede ser aplicado con diferentes sustancias para determinar el gasto cardiaco:
- Usando el oxígeno o Método de Fick Directo
- Método de dilución de indicador
- Termodilución
Método de Fick Directo
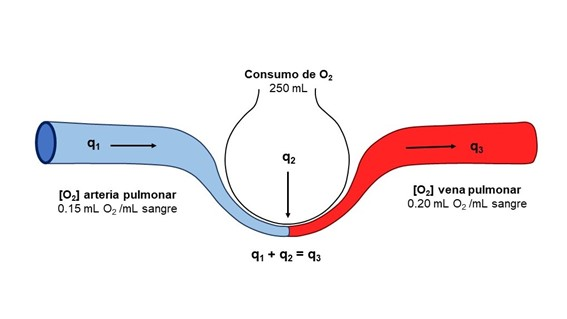
Para comprender este método hay que entender que todo el GC pasa por los pulmones (Fig. 2). El O2 que llega a los mismos por la arteria pulmonar, q1, es igual a la concentración de O2 a este nivel, (O2)ap, por el flujo pulmonar, Q, que como ya se ha dicho equivale a todo el GC.
Así,
q1= Q(O2)ap
(ec. 2)
Al atravesar los capilares pulmonares desde los alveolos se transfiere una cantidad extra de O2, q2, que en estado de equilibrio, y este es un aspecto muy relevante para entender una de las principales limitaciones de esta técnica, coincide con la cantidad de oxígeno que se consume por los tejidos (VO2).
El O2 que finalmente se transporta por las venas pulmonares hacia la circulación sistémica, q3, en virtud de la mencionada Ley de Conservación de Masas, sería la suma de q1 y q2.
Como el flujo por las venas pulmonares es también igual a todo el GC la fórmula quedaría
q3=Q(O2)vp (ec. 3)
Sabiendo que q1 + q2 = q3
Q (O2)ap + q2 = Q(O2)vp (ec. 4)
Despejando el flujo la ecuación quedaría:
Q= q2 / [(O2)vp – (O2)ap] donde, (ec. 5)
q2 en estado de equilibrio es el consumo de oxígeno (VO2). Este puede ser medido pidiendo al paciente que respire durante 1 minuto por un espirómetro que contenga un determinado volumen de O2 al 100% y un absorbedor de CO2. La medición de la cantidad de O2 que queda al final de la prueba permite conocer el consumo producido (5).
En un intento de simplificar la medición del VO2, diferentes autores han propuesto distintas fórmulas para valorarlo (6-8). Sin embargo, cuando se han comparado con mediciones directas del VO2, el 50% de las estimaciones difería en más del 10% y el 35% de las mismas en más de un 25% (9). También se ha sugerido considerar un consumo alrededor de 125 ml/min/m3 aunque, como era de esperar, se han demostrado importantes diferencias con los valores reales (10).
(O2)ap o concentración venosa de O2 (CvO2) debe ser medido de una mezcla de sangre venosa mixta a través de un catéter de arteria pulmonar.
(O2)vp equivale a la concentración arterial de O2 (CaO2) y puede determinarse de una gasometría arterial.
Sabiendo que q2 es VO2, (O2)ap es CvO2 y (O2)vp es CaO2. La fórmula podría expresarse de un modo que al lector probablemente le resulte más familiar:
En un sujeto en reposo un ejemplo del cálculo del GC con un consumo de O2 de 250 ml/min, un CaO2 de 0,20 ml de O2/ml de sangre y un contenido de O2 en sangre venosa mixta de 0,15 ml de O2/ml de sangre seguiría la siguiente fórmula:
Entre las principales limitaciones de este método se encuentran
- La medición directa del VO2 requiere de aparataje especializado y no resulta práctica en la clínica habitual. La determinación de este factor a través de las diferentes fórmulas descritas es, sin duda, la mayor fuente de error.
- Errores en la toma de muestras arteriales o venosas, o en la medición de la concentración de oxígeno de las mismas. Si la diferencia arteriovenosa es estrecha, pequeños errores de medida serían amplificados por la ecuación. Es interesante comprender este aspecto, porque esta es la razón por la que el método de Fick es más preciso en estados de bajo gasto. En estas condiciones las diferencias entre la saturación de oxígeno entre el sistema arterial y el venoso son importantes, lo que minimizaría el impacto de pequeños errores de medición.
- La existencia de shunt intracardiacos prácticamente invalidaría los resultados. En este caso la diferencia arteriovenosa de O2 no se debería a la tasa de extracción tisular del mismo.
- Por último, el modelo asume el estado de equilibrio, por el cual el O2 captado por los tejidos es igual al captado por los pulmones. En la práctica, es difícil mantener unas condiciones hemodinámicas o respiratorias estables, sobre todo en pacientes críticos, y el VO2 medido a nivel pulmonar podría no ser un fiel reflejo del consumo de oxígeno tisular.
Este último punto es especialmente relevante, y de hecho podría llegar a dudarse acerca de la idoneidad de la medición del GC con un método que precisa de un estado hemodinámico estable; precisamente es más relevante conocer este parámetro en aquellos pacientes inestables.
Método de dilución de indicador
Con este método se administra en arteria pulmonar o en una vena central una determinada cantidad de una sustancia de baja toxicidad y baja vida media (habitualmente verde de indocianina o litio) y se miden los cambios de concentración a nivel arterial en función del tiempo.
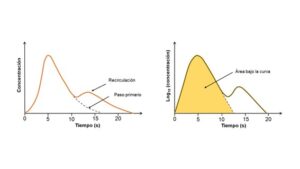
Esquemáticamente, dado un flujo Q ml/s por un tubo, se administra una cantidad q mg de indicador por un punto A. En un punto B más alejado se realizan pequeñas determinaciones de forma continua que se analizan con ayuda de un densiómetro. Los cambios en la concentración del indicador a lo largo del tiempo se expresan gráficamente (Fig. 3).
En este caso el GC se calcula a partir de la integral de esta curva (área bajo la curva) y la cantidad de indicador administrado usando una modificación de la ecuación de Fick:
donde,
q es la cantidad de indicador
es el área bajo la curva de la concentración del indicador entre t1 y t2.
Resulta esencial en este método que el indicador no debe presentar pérdidas entre los puntos A y B. Así mismo, es relevante entender cómo podría afectar el fenómeno de recirculación del indicador a la medición. Un segundo paso del mismo originaría un pico adicional en la gráfica de concentración-tiempo que dificultaría el análisis. Este problema se solventa, al menos en parte, realizando una transformación logarítmica en base 10 de la concentración, lo que sin duda facilita la lectura de la curva (Fig. 4).
Termodilución
Desde que fue descrita por Fegler en 1954 (11), probablemente es la técnica de dilución de indicador más empleada. En este caso el indicador es suero salino frío. Cuanta menor temperatura tenga, mayor será la diferencia con respecto a la sangre y, por tanto, mejora la relación señal/ruido (proporción existente entre la potencia de la señal que se transmite y la del ruido que la corrompe)
La termodilución se popularizó con el uso del CAP. Se administraba rápidamente una cantidad entre 10-15 ml de salino frío a través de la luz más proximal del catéter. Un termistor localizado en el extremo distal del dispositivo permitía representar gráficamente la variación de temperatura en función del tiempo.
donde,
V es el volumen inyectado
TS temperatura inicial de la sangre
TI temperatura inicial del suero inyectado
K1 constante de densidad
K2 constante de computación
área bajo la curva de la temperatura en función del tiempo.
Entre las fuentes de error de este método encontramos:
- Calentamiento del suero frío durante su administración a través del catéter.
- Arritmias como la fibrilación auricular.
- Regurgitación tricúspidea, pulmonar o shunt intracardiacos que producen recirculación de la sangre. Parece existir una relación directa entre el grado de insuficiencia tricúspidea y la variación en la medida del GC con respecto al valor real. De hecho, hasta la ventilación mecánica podría empeorar la insuficiencia tricúspidea, infraestimándose el valor real del GC.
- La temperatura de la sangre en las arterias pulmonares varía con el ciclo respiratorio y cardiaca lo que sería otra fuente de inexactitudes.
La termodilución presenta una serie de ventajas:
- Es un método más preciso que el de Fick en estados hiperdinámicos con elevación del GC.
- No son necesarias las punciones arteriales. Aunque esto no es del todo cierto. Con la caída en desuso del catéter de arteria pulmonar se desarrollaron nuevos sistemas de monitorización del GC menos invasivos basados en la termodilución, en los que la inyección se realiza en una vena central y el termistor se localiza en un catéter que se inserta en arteria femoral o radial.
- No se produce segundo pico de recirculación que es una de las principales causas de error con los métodos de dilución de indicador.
- El pequeño volumen inyectado en cada determinación es inocuo, lo que permite mediciones repetidas.
- Puede realizarse en presencia de dispositivos como el balón de contrapulsación.
- Las inexactitudes se minimizan realizando 3-4 mediciones y tomando para el análisis los valores medios.
Con el tiempo se desarrollaron sistemas de monitorización del GC de forma continua con CAP Una fuente de calor localizada en el VD calienta de forma intermitente la sangre. Los cambios de temperatura de la sangre son detectados por un termistor localizado en el extremo distal del dispositivo.
Aunque se ha criticado de estos sistemas que presentan un tiempo lento de respuesta para detectar cambios en el GC (12,13), lo cierto es que siempre serán más rápidos que los bolos intermitentes, además de más precisos (14).
Bajo condiciones ideales, la termodilución permite determinar el valor del GC con un rango de error de 5-20%.
Conclusión
A lo largo de las últimas dos décadas, diversos métodos menos invasivos han desplazado al CAP en la monitorización del GC. Sin embargo, este dispositivo sigue empleándose y es necesario que el anestesista-intensivista conozca los principios en los que se basa esta monitorización, así como sus ventajas e inconvenientes
Bibliografía
- Sette P, Dorizzi RM, Azzini AM. Vascular access: An historical perspective from Sir William Harvey to the 1956 Nobel prize to André F. Cournand, Werner Forssmann, and Dickinson W. Richards. J Vasc Access 2012; 13:137–44. (PubMed)
- Vincent JL, Fagnoul D. Do we need to monitor cardiac output during major surgery? Anesthesiology 2012; 117:1151-1152. (PubMed)
- Harvey S, Young D, Brampton W, Cooper AB, Doig G, Sibbald W et al Pulmonary artery catheters for adult patients in intensive care. Cochrane Database Syst Rev 2006:(3):CD003408. (PubMed)
- Sandham JD, Hull RD, Brant RF, Knox L, Pineo GF, Doig CJ et al A Randomized, Controlled Trial of the Use of Pulmonary-Artery Catheters in High-Risk Surgical Patients N Engl J Med 2003; 348:5-14 (PubMed)
- Pappano AJ, Wier WG. The cardiac pump. En Cardiovascular physiology, 11ª ed. Philadelphia: Elsevier 2019:71-73.
- Krovetz LJ, Goldbloom S. Normal standards for cardiovascular data. I. Examination of the validity of cardiac index. Johns Hopkins Med J 1972;130:174–186. (PMC)
- LaFarge CG, Miettinen OS. The estimation of oxygen consumption. Cardiovasc Res 1970;4:23–30. (PubMed)
- Bergstra A, van Dijk RB, Hillege HL, Lie KI, Mook GA. Assumed oxygen consumption based on calculation from dye dilution cardiac output: an improved formula. Eur Heart J 1995;16:698–703. (PMC)
- Kendrick AH, West J, Papouchado M, Rozkovec A. Direct Fick cardiac output: are assumed values of oxygen consumption acceptable? Eur Heart J 1988;9:337–342. (HTML)
- Wolf A, Pollman MJ, Trindade PT, Fowler MB, Alderman EL. Use of assumed versus measured oxygen consumption for the determination of cardiac output using the Fick principle.Cathet Cardiovasc Diagn 1998;43:372–380. (PubMed)
- Fegler G. Measurement of cardiac output in anesthetized animals by thermodilution method. QJExpPhysiol 1954;39:153 (PubMed)
- Burchell SA, Yu M, Takiguchi SA, Ohta RM Myers SA. Evaluation of a continuous cardiac output and mixed venous oxygen saturation catheter in critically ill surgical patients. Crit Care Med 1997;25:388-391. (PMC)
- Poli de Figueiredo LF, Malbouisson LM, Varicoda EY, Carmona MJ, Auler JO Jr, Rocha e Silva M. Thermal filament continuous thermodilution cardiac output delayed response limits its value during acute hemodynamic instability. J Trauma 1999;47:288-293. doi: 10.1097/00005373-199908000-00011. (PMC)
- Mihaljevi T, vonSegesser LK, Tonz M Leskosek B, Seifert B, Jenni R, et al. Continuous versus bolus thermodilution cardiac output measurements: a comparative study. Crit Care Med 1995;23:944-949. (HTML)