Castell Jimeno C (1), Peñas Palomo C (1), Pretus Rubio S (2), Mariscal Flores M (3)
(1) MIR. Servicio Anestesiología y Reanimación del Hospital Universitario de Getafe. Madrid. España
(2) FEA Servicio Anestesiología y Reanimación del Hospital Universitario de Getafe. Madrid. España.
(3) Jefa de Sección Servicio Anestesiología y Reanimación del Hospital Universitario de Getafe. Madrid. España.
Cómo citar este artículo: Castell Jimeno, C., Mariscal Flores, M., Peñas Palomo, C., & Pretus Rubio, S. (2023). Cefalea postpunción. Factores de riesgo, diagnóstico y tratamiento. Revista Electrónica AnestesiaR, 15(3). https://doi.org/10.30445/rear.v15i3.1137
Introducción
La cefalea postpunción dural (CPPD) se define como un dolor de cabeza que empeora en bipedestación y mejora con el decúbito, apareciendo dentro de los 5 primeros días tras perforar la duramadre al realizar una anestesia espinal o tras puncionar accidentalmente la duramadre durante una anestesia epidural.
Se trata de la complicación mas frecuente tras la anestesia neuroaxial, con una incidencia de hasta el 25% según la bibliografía.
La mayoría se resuelve en menos de una semana, aunque puede durar mas tiempo.
Los factores de riesgo pueden ser modificables y no modificables. Y entre otras causas posibles nos encontramos con: punción lumbar diagnóstica, drenaje de LCR, dispositivos intratecales, quimioterapia intratecal, estudios radiológicos (mielografia)…1
Si se sospecha una complicación intracraneal o intramedular, debe solicitarse de inmediato una prueba de imagen, siendo de elección la resonancia magnética.
Desarrollo
1. Fisiopatología.
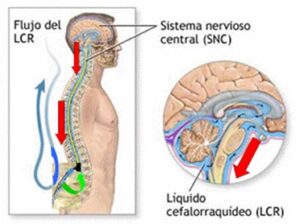
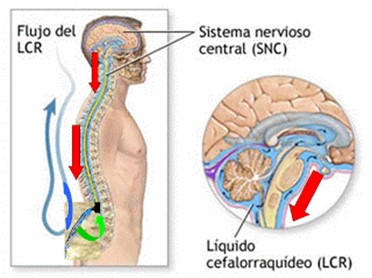
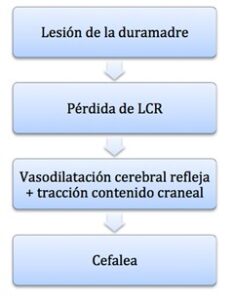
La fisiopatología no se conoce con precisión. La teoría mas aceptada es que tras la punción de la duramadre se produce pérdida de líquido cefalorraquídeo (LCR), causando bajada de presión de dicho líquido, lo cual, provoca hipotensión intracraneal con vasodilatación meníngea refleja y tracción de las estructuras craneales, como meninges o nervios craneales (figura 1 y 2).
La cefalea postpunción (CPPD) es, por tanto, consecuencia de la vasodilatación que se produce para que la presión del LCR permanezca constante. De esta manera al disminuir la presión del LCR se produce un aumento de irrigación, lo cual, presupone la dilatación de los vasos cerebrales 1, 2, 3.
2. Factores de riesgo
Los factores de riesgo para desarrollar CPPD pueden ser clasificados en dos grandes grupos (1, 2, 4, 5, 6):
No modificables:
1. Sexo: la CPPD es mas frecuente en mujeres que en hombres, particularmente durante su vida fértil. Esto se podría explicar porque los altos niveles de estrógenos producen distensión de los vasos cerebrales.
2. Edad: es mas frecuente en pacientes jóvenes de 20 a 40 años y su frecuencia disminuye a partir de los 50 años, siendo escasa a partir de los 60 años. Existen tres posibles factores por los cuales la incidencia disminuye a partir de los 40 años: la primera es el endurecimiento de la duramadre que hace que sea mas difícil que el LCR se filtre por el orifico de punción; la segunda, menor reacción de los vasos cerebrales a la hipotensión del LCR y finalmente, un espacio vertebral disminuido.
3. Antecedentes personales de cefalea, especialmente la cefalea tensional. Esta incidencia se incrementaba hasta el 70% si habían padecido cefalea la semana previa. Sin embargo, no se ha encontrado que la migraña incremente el riesgo de CPPD y la punción de la duramadre no predispone a ataques de migraña.
4. Bajo peso: un IMC<25Kg/m2 se ha demostrado que es un factor de riesgo de CPP. No hay estudios que demuestren que las mujeres obesas tengan un mayor riesgo.
5. Embarazo: sobretodo mayor tasa después del parto vaginal, ya que los pujos aumentan la pérdida de LCR. Además tras el parto, la diminución de la presión intraabdominal, disminuye la presión en el espacio epidural y con ello se aumenta la pérdida de LCR.
En conclusión, el mayor riesgo lo presenta una mujer joven embarazada a la que se le ha realizado una punción dural accidental con una aguja epidural de gran calibre.
Modificables (4):
- Tipo de la aguja: Las agujas espinales que se utilizan para realizar las punciones durales pueden ser traumáticas (Quincke, Tuchy, Levi) o atraumáticas (Greene, Whitacre o punta de lápiz, Sprotte, Polymedic, Gertie Marx, Atraucan). La diferencia entre ambas es fundamental. Las agujas espinales traumáticas tienen una punta biselada que realiza corte en las capas de la duramadre. Sin embargo, las agujas atraumaticas tienen una punta en forma en cono circular cerrado con un perfil redondeado, separando las fibras de la duramadre y ocasionando menos pérdida de LCR y por tanto menos incidencia de CPPD.
Se realizó un estudio que comparaba la incidencia de CPPD tras utilizar una aguja traumática (Quincke) y una atraumática (Whitacre). Se concluyó que la aguja Whitacre es menos traumática para los tejidos de la duramadre por su diseño no cortante en punta de lápiz.
2. Calibre de la aguja: El calibrede la aguja es directamente proporcional a la consecuencia de CPPD 1, 4. Cuanto mayor es el calibre de la aguja, mayor es la incidencia de CPPD:
- 70% si el tamaño de la aguja es entre 16-19 G
- 40% si el tamaño de la aguja es entre 20- 22 G
- 12% si el tamaño de la aguja es entre 24- 27 G
3. Número de intentos.
4. Experiencia del anestesista.
5. Orientación del bisel: un bisel en dirección perpendicular ocasiona el doble de incidencia de CPPD que orientar el bisel de forma paralela a las fibras de la duramadre.
6. Posición del paciente: no hace referencia a si el paciente se sitúa en decúbito lateral o en sedestación a la hora de efectuar la técnica, sino de que el paciente este en una buena posición anatómica y no haga movimientos mientras se esta realizando la punción.
3. Clínica
La cefalea post-punción lumbar se define como un dolor de cabeza tipo posicional que aparece dentro de los 5 primeros días tras una punción dural y empeora en sedestación y mejora con el decúbito supino, dicha característica apoya a su diagnóstico2.
Puede asociarse a lumbalgia, vértigo, tinnitus, cambios en la audición, parálisis de los nervios craneales, diplopía, ceguera, náuseas, fotofobia. 4
Es descrita como opresiva, profunda, situada en la región frontal u occipital aunque puede hacerse generalizada.
Características: 4
- Aparición: el 90% de los casos dentro de las primeras 72 horas después de la punción dural.
- Bilateral à áreas frontal y occipital, aunque se puede generalizar
- Opresiva, no pulsátil
- Irradiación: cuello y hombros
- Empeora con movimientos de la cabeza y maniobras que aumentan la presión intracraneal (toser, estornudar)
- Remite espontáneamente en 2 semanas o tras tratamiento
Otros síntomas asociados: 4
- Más de la mitad de los pacientes acusan síntomas asociados como mareo, nauseas y ocasionalmente vómito.
- Rigidez de cuello.
- Alteraciones visuales, por afectación de los pares craneales III, IV, y VI: Los síntomas visuales ocurren por la tracción de los nervios en su deslazamiento hacia abajo cuando ocurre la tracción del contenido craneal. De estos nervios, el motor ocular externo (VI par craneal) es el mas afectado por su angulación aguda dentro del cráneo, llegándose a producir parálisis de dicho nervio y dificultad en la abducción, con lo cual, el ojo se desvía hacia el interior 1. Los síntomas que provocan las alteraciones visuales pueden ser:
Visión borrosa o diplopía
Fotofobia o dificultad para enfocar
Alteraciones auditivas: los síntomas auditivos pueden estar causados por afectación del VIII par craneal o por una fístula de líquido perilinfático de la cóclea hacia el espacio subaracnoideo a través del acueducto coclear, el cual se encuentra abierto en el 50% de los adultos y genera un síndrome vestibular parecido al de Menière 6 . Los síntomas pueden ser:
- Vértigos, acúfenos, tinnitus
- Diminución de la audición
4. Diagnóstico
La presencia de cefalea postural con el antecedente de punción dural, accidental o intencionada, guían el diagnóstico. Pero en ocasiones es necesario realizar pruebas de imagen, siendo la primera prueba a realizar la resonancia magnética (RMN) en la que podemos encontrar un descenso de estructuras intracraneanas y un realce paquimeníngeo 6. No obstante, es necesario realizar un diagnostico diferencial con las siguientes patologías 3:
- Migraña: no cede con el decúbito.
- Eclampsia: se acompaña de hipertensión arterial.
- Meningitis: presenta rigidez de nuca y fiebre.
- Trombosis del seno cortical: la cefalea presenta síntomas neurológicos y no influye la postura.
- Hematoma subdural: se trata de una cefalea de inicio brusco junto con nauseas, vómitos, convulsiones y alteraciones focales motoras o sensitivas. Además no se relaciona con la postura.
- Angiopatía cerebral posparto: causada por un vasoespasmo cerebral ocasiona cefalea, convulsiones y déficit neurológico tras un parto normal.
- Neumoencéfalo: se produce al realizar una punción epidural con la técnica de aire. El tratamiento se basa en mantener una actitud expectante, administrando oxígeno al 100%, ya que acelera la reabsorción de aire intratecal.
5. Tratamiento
No existe un acuerdo universal para el tratamiento de la CPPD (3, 6, 7).
5.1 No invasivo o conservador:
- Deambulación precoz: antiguamente se optaba por reposo en cama, pero últimamente se ha demostrado que no existe evidencia de su beneficio.
- Medidas posturales: aunque a la mayoría de los pacientes les mejora la sintomatología en decúbito supino, no tiene gran evidencia de su beneficio. Sin embargo se sugiere cierto beneficio en el decúbito prono, pero es una postura complicada para el postparto.
- Hidratación: se recomienza mantener un balance hídrico normal, sin necesidad de sobrehidratar.
- Faja abdominal: aunque es complicada de tolerar, aumenta la presión en las venas epidurales, ocasionando mayor presión del LCR y disminuyendo la tracción de estructuras cerebrales, lo cual, mejora la cefalea. Es recomendable colocarla inmediatamente tras el parto y mantenerla hasta el alta hospitalaria.
- Analgésicos: paracetamol, AINES (antiinflamatorios no esteroideos) u opioides pueden ser administrados para mejorar el dolor.
- Cafeína: causa vasoconstricción cerebral y con ello se estimula la producción de LCR. Si transcurridas 24-48horas la cefalea no cede y es intensa o moderada se administran 300 mg vía oral cada 12-24 horas o 500 mg vía oral cada 24 horas. Está contraindicada en: preeclampsia, HTA crónica, trastornos epilépticos y taquiarritmias.
- Corticoides (hidrocortisona): se utilizan para frenar la respuesta inflamatoria tras la tracción meníngea. Se recomienda una dosis de carga de 200 mg intravenosos seguida de tres dosis de 100 mg cada 8 horas durante 2 días.No se recomiendan en: hipertensión, diabetes o úlcera gastrointestinal.
5.2 Invasivo
Parche hemático epidural (PHE): GOLD ESTÁNDAR (1, 3, 6)
Parche hemático epidural (PHE): GOLD ESTÁNDAR 1, 3, 6
La utilización de esta técnica surgió al observar que tras las punciones accidentales, los pacientes mejoraban rápidamente. Su eficacia y sus pocos efectos secundarios hacen que sea el gold estándar en el tratamiento de la CPPD.
Indicación: para la cefalea postpunción dural de intensidad moderada de mas de 24 horas de duración, que no mejora con la medicación habitual e impide una actividad normal. No está recomendado en cefaleas de menos 24 horas y su efectividad aumenta si se aplica a las 48-72 horas de la punción.
Técnica: Se trata de una técnica estéril que se puede efectuar tanto en decúbito lateral como en sedestación. Si es posible se debe realizar la punción epidural en el mismo espacio intervertebral que la punción previa.
Consiste en administrar 15-20 ml de sangra autóloga en el espacio epidural, con el objetivo de formar un coágulo que se adhiera a la duramadre y tape el orificio. Con ello, se consigue un incremento de la presión del LCR, reduciendo la tracción de las estructuras cerebrales.
Aunque lo mas frecuente es que alivie el dolor rápidamente, puede ser necesario repetirlo. El éxito terapéutico del parche hemático oscila entre el 95% tras la primera inyección y aumenta hasta un 98% si se repite el procedimiento.
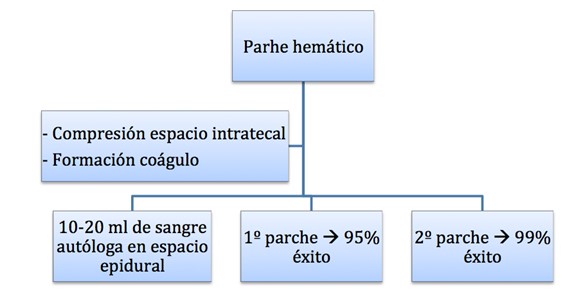
Beneficios: Con el parche hemático se consigue restaurar la circulación normal del líquido cefalorraquídeo, mejora las alteraciones visuales y auditivas, puede ayudar a prevenir el hematoma subdural y disminuye el porcentaje de cefalea crónica.
Complicaciones: Si aparece dolor de espalda, glúteos, miembros inferiores o empeoramiento de cefalea, es necesario parar la inyección.
Puede presentarse empeoramiento de los síntomas y dolores radiculares que normalmente ceden con analgésicos de primer escalón. La aplicación de dicho parche no altera la eficacia de las anestesias epidurales posteriores y en general esa técnica es un procedimiento seguro 6.
Tras el PHE se recomienda permanecer en decúbito supino 30-120 min y evitar esfuerzos físicos durante el menos 2-7 días.
Cuando la CPPD no responde al PHE, aparece fiebre o focalidad neurológica, es necesario una valoración mas exhaustiva para descartar meningitis, hemorragia intracraneal o trombosis.
Complicaciones 1: como toda prueba invasiva no esta exenta de complicaciones y algunas de ellas son:
- Dolor lumbar
- Dolor radicular a MMII
- Irritación meníngea
- Hematoma subdural
- Fiebre
- Neumoencéfalo
- Bradicardia transitoria
- Convulsiones
Contraindicaciones 6: no en todas las pacientes se puede realizar un parche hemático y algunas de las situaciones en las que no podemos administrarlo son las siguientes:
- Negativa del paciente
- Punción difícil
- Infección sitio de punción
- Coagulopatía o trompocitopenia
- Sepsis
- Pacientes oncológicos
- VIH
Entonces: ¿si el parche hemático es considerado el tratamiento gold estándar pero en nuestra paciente existe alguna contraindicación para realizarlo, que mas puedo hacer? Para contestar dicha pregunta se han propuesto algunas alterativas de tratamiento.
Alternativas al parque hemático
Al igual que el objetivo del PHE es aumentar la presión en espacio epidural y disminuir la salida de LCR a través del orifico dural, tenemos dos procedimientos que tendrían el mismo objetivo:
- Parche epidural salino: Se trata de una inyección de suero salino en el espacio epidural. Puede ser continua, 15-25 mL/h; o fraccionada, 30-60 mL cada 6 horas (en cualquier caso mantener 24 horas). En la actualidad, este tratamiento solo se administra si existe contraindicación para el PHE.
- Cirugía: como última alternativa, si persiste la fuga de líquido cefalorraquídeo y no hay respuesta a ningún tratamiento.
A pesar de estas alternativas existen otros tratamientos sin eficacia terapéutica demostrada y que están pendientes de estudios, como son el fentanilo intratecal, la morfina epidural y el parche epidural con pegamento biológico de fibrina, este último podría suponer una gran revolución y convertirse en la gran alterativa al PHE cuando existe alguna contraindicación, pero aún son necesarios mas estudios para su administración 3.
Conclusión
La cefalea post-punción lumbar es la complicación mas frecuente de la perforación accidental o deliberada de la duramadre y suele remitir durante la primera semana. Su fisiopatología aún no esta bien esclarecida y evitar algunos factores de riesgo como el tipo de aguja, el calibre de ésta y la orientación del bisel pueden disminuir su incidencia. Inicialmente se trata de manera conservadora con analgésicos de primer escalón, cafeína y corticoides pero cuando la cefalea es tan intensa que interfiere en la vida diaria o no mejora con el tratamiento conservador, se recurre al parche epidural de sangre autóloga, considerado un tratamiento seguro y superior al manejo conservador. En la actualidad se esta intentando buscar otra alterativas al parche hemático, aunque todavía no hay ninguna que haya igualado o aumentado su eficacia8.
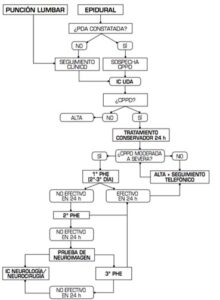
Para llevar a cabo un rápido manejo de la CPPD y disminuir la variabilidad en el tratamiento, la Sociedad Española del Dolor ha realizado este algoritmo (figura 4), resumiendo de forma breve y esquemática la actuación a lleva a cabo.
Bibliografía
1. Barash P, Cullen B, Stoelting R, Cahalan M, Stock C, Ortega R, et al. Fundamentos Anestesia Clínica. 1o. España: Wolters Kluwer; 2016.
2. Molina K. Factores de riesgo de cefalea post puncion dural durante anestesia raquídea. Colegio médico. 2017. (HTML)
3. Hernández A. Situaciones Clínicas en Anestesia y Cuidados Críticos. 5o. SEDAR, editor. Madrid: Editorial medica panamericana; 2020. 415–417 p
4. Rodríguez Márquez IA, Saab Ortega N. Actualización sobre factores de riesgo para cefalea pospunción dural. Rev Médicas UIS [Internet]. 2015 Sep 1;28(3):345–52. Available from: http://revistas.uis.edu.co/index.php/revistamedicasuis/article/view/5211/5520 (HTML)
5. Roewer N, Thiel H. Anestesia Texto y Atlas. 4o. Madrid: Editorial medica panamericana; 2011.
6. Francisco J, Zafra T, Clínica S. Cefalea post-punción lumbar Post-lumbar puncture headache. Acta Neurol Colomb [Internet]. 2008;24:112-117 (PDF)
7. Palleja de, Spinelli P, Boibo R, Larzabal N, Morales E. Cesárea con anestesia raquidea ¿problema actual o pasado?. Anest Analg Reanim 2017 Dic; 30 (2). (PDF)
8. Carrillo-Torres Jardín Núm O, Carrillo-Torres O, Camilo Dulce-Guerra J, Raquel Vázquez-Apodaca D, Fernando Sandoval-Magallanes F. Protocolo de tratamiento para la cefalea postpunción de duramadre. Rev Soc Esp Dolor [Internet]. 2016 [cited 2022 Apr 14];39(3):205–12. Available from: http://www.medigraphic.com/rmawww.medigraphic.org.mx (HTML)





¿Cual es su opinion de aplicar esteroides (metilprednisolona o hidrocortisona) aunado a lidocaina para parche hemático?
corrijo…en lugar de utilizar sangre homóloga