A. Gironés Muriel *, B. San Pedro Urquiza *, S. Domenech de Frutos **, S. Lage Piñeiro ***.
Cómo citar este artículo: Gironés Muriel, A., San Pedro, B., Domenech de Frutos, S., & Lage Piñeiro, S. (2011). Procesos de decisión en la antiagregación (IV): Síndrome Coronario Agudo. Revista Electrónica AnestesiaR, 3(7), 4. https://doi.org/10.30445/rear.v3i7.459
Tratamientos específicos antitrombóticos en el síndrome coronario agudo
El síndrome coronario agudo es la entidad patológica donde los tratamientos de antiagregación o anticoagulación se vuelven más elaborados. Las terapias múltiples, los nuevos antiagregantes y la gran producción científica que genera cambios en las recomendaciones, cambios apoyados por una potente industria farmacéutica, puede complicar la toma de decisiones preoperatorias.
En anteriores entradas hemos hablado sobre la profilaxis primaria de la isquemia cardíaca, y vemos como las recomendaciones sobre su tratamiento preventivo han ido evolucionado para ser cada vez más restrictivas. Los descubrimientos de nuevos factores individuales (tanto genéticos como ambientales) que desempeñen un papel fundamental en la incidencia del síndrome coronario son cada vez más estudiados y aclarados. Desde el descubrimiento de los isotipos del gen de la paraoxonasa-1, pasando por la implicación del perímetro abdominal, hasta llegar a la polución ambiental, se vislumbran con fuerza estos y otros nuevos factores individuales implicados en la aparición de un episodio isquémico coronario, lo que condicionará un cambio de recomendación en las guías futuras para prevenir dichos eventos.

Intentamos dar en esta entrada una versión simplificada de las recomendaciones antitrombóticas en el entorno del síndrome coronario agudo, diferenciando para su estudio varias entidades, y dejamos al lector que compruebe una vez más como las recomendaciones y estudios no son unánimes, aunque siguen unas pautas más o menos comunes.
– Pacientes con síndrome coronario agudo y elevación del ST (IAM).
– Pacientes con angina inestable o síndrome coronario agudo sin elevación del ST (SCASEST).
– Pacientes con by-pass coronario.
– Pacientes con stent coronario.
4.1.- Pacientes con IAM y elevación del ST
A partir del año 2.009 la American Heart Asociation (AHA) propuso una serie de recomendaciones sobre esta patología que difieren algo respecto a la de años precedentes. Hemos destacado algunas:
· Recomiendan iniciar tratamiento con los nuevos antagonistas de la glucoproteina IIb/IIIa (abciximab, tirofiban,eptifibatida) durante la angioplastia primaria solo en pacientes seleccionados (grado de evidencia IIa).
· Introduce el prasugrel como alternativa al clopidogrel, excepto en los pacientes de edad avanzada, con bajo peso o con riesgo de sangrado activo (grado de evidencia I).
· Recomienda mantener un año el clopidogrel o prasugrel en estos pacientes tratados con stent (grado de evidencia I).
· La anticoagulación con bivalirudina es valida como coadyuvante en la angioplastia primaria.
· Los stents farmacoactivos se pueden usar como alternativa a los convencionales en la angioplastia primaria.
Evidencias de la terapia antiagregante/anticoagulante
Existe una recomendación generalizada entre los diversos autores de administrar AAS asociado a fibrinolisis o a anticoagulación en toda fase aguda de un IAM, pues esta asociación mejora la tasa de eventos negativos tras el IAM frente a la terapeútica de usar solo fibrinolisis o anticoagulacion (Grado de evidencia I).
Hemos encontrado autores y guías de consenso que abogan por usar tan solo la aspirina por si misma, apoyados en estudios que reflejan una disminución de la tasa de eventos con el AAS por sí mismo (grado de evidencia I). También encontramos autores que han estudiado el efecto de otros antiagregantes, y remarcan que no han demostrado ser superiores a la aspirina , aunque sí frente a placebo (Grado de evidencia I ) .
En resumen, podemos hablar de un consenso unánime sobre la recomendación de administrar AAS a toda fase aguda de un IAM y su mantenimiento de manera indefinida, así como usar otros antiagregantes si no se puede usar AAS, especialmente clopidogrel, aunque esta última afirmación no es tan unánime.
Para demostrar las anteriores afirmaciones hemos buscado entre la abrumadora bibliografía al respecto, y nos encontramos con estudios muy referenciados. El ISIS-21 demostró una reducción de la mortalidad de un 42% cuando se asoció 160 mg. de AAS junto al tratamiento fibrinolítico en la fase aguda del IAM, frente a una reducción del 25% con el uso único de la aspirina y del 23% con la terapia fibrinolítica en solitario.
El estudio ATC, comentado en anteriores entradas, contaba como subgrupo a pacientes con IAM en los cuales la administración del AAS les redujo un 25% la tasa de eventos negativos cardiovasculares. Significativo también es un metaanálisis 2 que recoge el efecto de la aspirina en la reducción significativa de la tasa de reoclusión coronaria tras IAM , con seguimiento a los 4 años, constatado con arteriografía previa y posteriores.
Respecto a la asociación entre anticoagulantes y AAS, encontramos varios estudios 3 que reflejan una mejora significativa frente a mortalidad, reinfarto y ACVA tras un IAM , si bien es cierto que la tasa de hemorragias también se incrementó.
En definitiva, el tratamiento agudo y a corto plazo se enmarca dentro de tratamientos combinados, con variaciones año tras año debido al aporte de nuevos estudios que apoyan la administración de nuevos fármacos y combinaciones entre ellos.
4.2.- Pacientes con angina inestable o con síndrome coronario agudo sin elevación del ST (SCASEST)
Esta entidad patológica tiene una gran variabilidad clínica, así como múltiples tratamientos. Clásicamente, se han diferenciado 3 grupos de riesgo, dependiendo de la presencia o no de varios síntomas que condicionarán un mejor o peor pronóstico. Las guías NICE de 2.010 (National Institute for Health and Clinical Excellence) consideran prioritario implementar una serie de medidas terapéuticas en esta patología, que a nuestro parecer aportan un gran transfondo de coherencia y sentido común, aunque con discrepancia frente a otros autores en lo referente a la administración de los nuevos antiagregantes. Por todo ello, creemos conveniente mostrarlas:
· Tan pronto como se establezca el diagnóstico del SCASEST y se inicie el tratamiento con AAS y un agente antitrombótico, se debe evaluar formalmente el riesgo de futuros eventos cardiovasculares utilizando una escala de riesgo que prediga la mortalidad a los 6 meses.
· En pacientes con riesgo intermedio o alto (mortalidad a los 6 meses >3%) se debe considerar la administración de eptifibatida o tirofibán a los pacientes que van a someterse a una coronariografía en las primeras 96 h.
· Se debe ofrecer coronariografía (con o sin revascularización) en las primeras 96 h. a todo paciente con riesgo intermedio o elevado si no existe contraindicación (por sangrado activo o comorbilidad) y hacerla lo antes posible a todo paciente con alto riesgo de isquemia.
· Cuando las indicaciones de revascularización no estén claras, se deben discutir las opciones entre cardiologos intervencionistas, medico responsable y el propio paciente.
· En los pacientes tratados de forma conservadora, se debe realizar un test de isquemia antes del alta.
· Antes del alta se deben ofrecer consejos e información al paciente sobre el diagnóstico, seguimiento, rehabilitación cardíaca, manejo de los factores de riesgo y cambios de hábitos de vida.
Como en el anterior apartado, hemos buscado en la literatura las evidencias sobre los tratamientos recomendados, y estas son las conclusiones:
El AAS reduce la mortalidad global en todas las variedades de los síndromes coronarios agudos independientemente si se realiza o no una intervención coronaria percutánea (grado de evidencia I), puesto que disminuye la mortalidad en el síndrome coronario agudo entre un 43% y un 57% 4 , si bien constatamos que realmente no hay unanimidad en cual es la dosis adecuada .
Las tienopiridinas (ticlopidina y clopidogrel) también reducen la incidencia de infarto y de complicaciones vasculares. La olvidada ticlopidina está validada por estudios como Balsano F et al 5 afirmando que 250 mg. de ticlopidina cada 12 h. reduce la tasa de IAM un 46% con una p=0,009 a partir de las dos semanas de tratamiento. Aunque ya hemos visto que su uso se ha visto desplazado por el clopidogrel debido al mejor perfil de seguridad de este, con una abrumadora literatura que apoya su uso (estudios CURE 6, CREDO 7, CLASSICS 8, etc.).
La doble antiagregación, de la que hablaremos más en profundidad, está avalada por múltiples estudios, especialmente en el caso que se considere una angioplastia con la colocación de un stent (STARS 9,FANTASTIC 10, ISAR11, etc.). Existe, por tanto, un amplio consenso en la recomendación de administrar una doble antiagregación por su gran beneficio, calculado en una reducción del riesgo cardiovascular de hasta un 75% (1,6% frente a un 6,2%, con p=0,01).
El trifusal, sulfinpirazona, dipiridamol y trapidilo no han demostrado un beneficio consistente frente al uso del AAS. Por tanto, su recomendación no es ni mucho menos unánime, aunque existan estudios al respecto que lo apoyen, como el estudio STARC 12 con 254 pacientes, comparando tradipilo versus AAS y concluyendo que el trapidilo reduce la reestenosis comproblable por angiografía un 24,2% frente a 39,7% con AAS, con p< 0,01 .
Los inhibidores de la IIb/IIIa son también eficaces en el SCATEST de alto riesgo (grado de evidencia I) debido a su capacidad contrastada de reducir también infartos y mortalidad en los pacientes tratados, argumento demostrado en varios metaanálisis 12. Nos es llamativo la existencia de ciertas particularidades entre estos nuevos antiagregantes según la opción terapéutica a seguir. Particularidades basadas en los múltiples ensayos clínicos que precedieron y siguieron a su comercialización, y que pasamos a resumir (GUSTO IV-ACS RAPORT, IMPACT-II, PRISM entre otros 13).
· El abciximab es eficaz en pacientes que van a recibir una coronarioplastia percutánea.
· El tirofiban es eficaz en los que no van a recibir dicha intervención percutánea. A pesar se de esto se recomienda en las guías NICE previo a una angioplastia.
· La eptifibatida es eficaz a altas dosis , tiempo dependiente tanto si se realiza la coronarioplastia percutánea como si no.
· El lamifiban no demostró eficacia.
Nos parece también interesante destacar que hemos encontrado una recomendación negativa en el uso de los inhibidores de la IIb/IIIa por vía oral, pues aumentan las complicaciones hemorrágicas y aumentan la mortalidad un 1,66 frente a un 1,33 con una p=0,001 , no siendo recomendable su utilización en estos casos 14 (grado I de evidencia)
A modo de resumen, diremos que con unanimidad diversas entidades recomiendan con un grado de recomendación A el administrar AAS y clopidogrel en todos lo pacientes afectos de SCASEST salvo los que van a ser candidatos a by-pass coronario. El prasugrel y los nuevos IIb/IIIa siguen en proceso de debate, si bien las recomendaciones para su uso aumentan.
 4.3.- Cirugía cardiaca con by-pass
4.3.- Cirugía cardiaca con by-pass
Parece existir, un consenso generalizado en la recomendación de administrar AAS a todo paciente sometido a una cirugía de revascularización coronaria, pudiendo usarse en caso de intolerancia trifusal o indobufeno, pero no clopidogrel ni dipiridamol.
Estas recomendaciones se basan en una evidencia de grado I en la que el AAS mejora la permeabilidad del injerto coronario y aumenta la supervivencia, al igual que el indobufeno y el trifusal,tanto solos como asociados al AAS. En cambio, asociar clopidogrel al AAS parece aumentar las complicaciones 15 (grado de evidencia II). Y fármacos como la sufinpirazona ni el dipiridamol parece que no mejoran la tasa de reoclusión de estos injertos 16.
Son varios los estudios que avalan estas afirmaciones, como el de Goldman S y col 17 que midió efectos de la AAS asociado o no a dipiridamol, sulfinpirazona o placebo, encontrando una mejora en la permeabilidad del injerto con las pautas a base de AAS, mejorando 5 veces la supervivencia, no obteniendo en cambio mejores resultados con la adicción de otros antiplaquetarios. Así mismo, otro estudio con 5.065 pacientes 18 reflejo que 650 mg. de AAS de manera precóz cada 24 horas redujo la mortalidad (1,3% frente a 4%, con p< 0,001), redujo el IAM (2,8% frente a 5,4%, con p<0.001) y el ACVA (1,3% frente a 2,6%, con p=0,01) en este tipo de pacientes.
 4.4.- Paciente portador de Stent coronario
4.4.- Paciente portador de Stent coronario
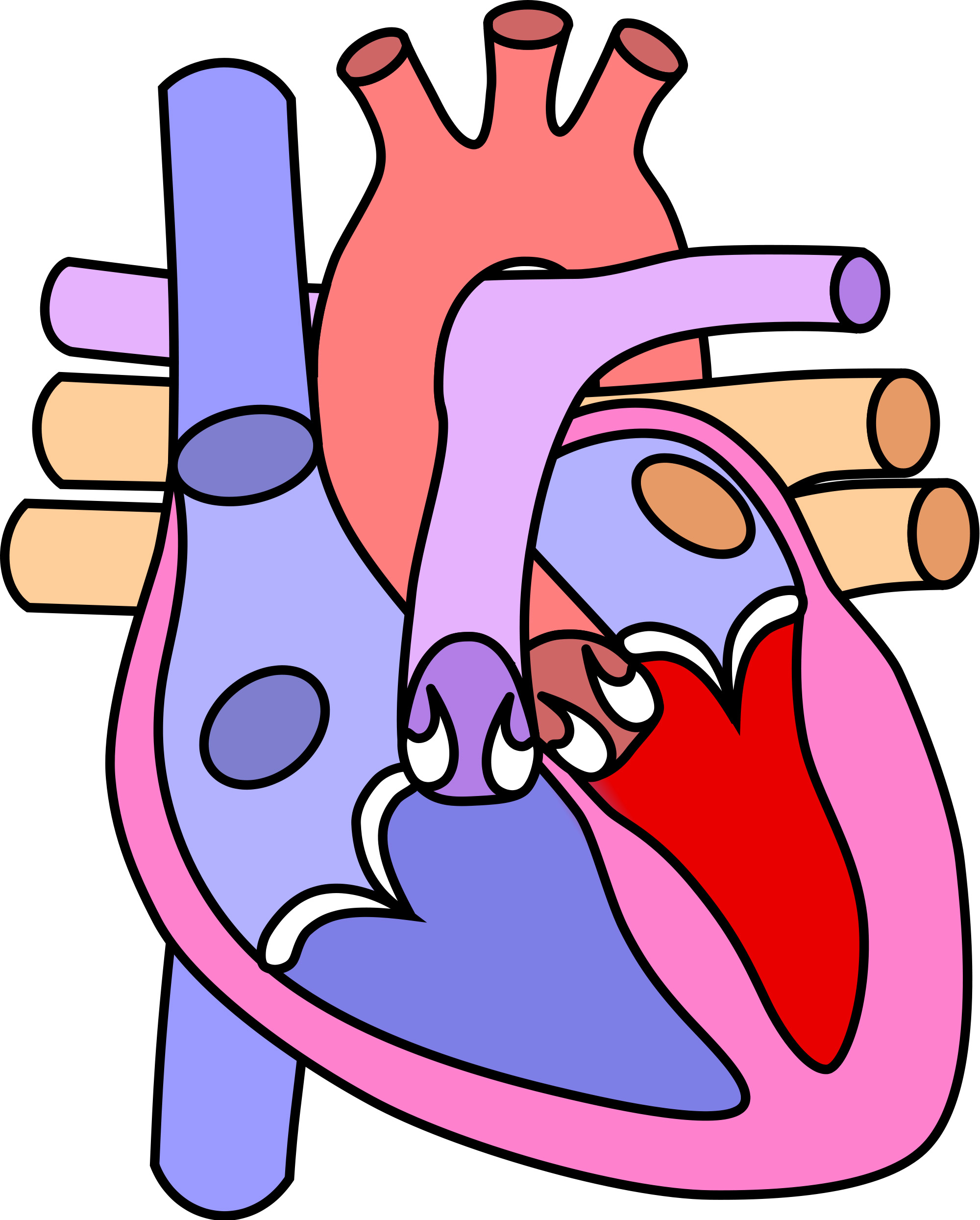
En el ámbito del síndrome coronario agudo, la incorporación al tratamiento de los stents coronarios ha supuesto un cambio en el pronóstico de esta patología. Su práctica va en aumento, como demuestran las 51.689 intervenciones de este tipo realizadas en España en el año 2.005, hasta llegar a cerca de las 57.000 en el 2.008. De todos ellos, se calcula que cerca del 60% son los relativamente nuevos stent farmacoactivos (SFA), que conllevan una complicación en el manejo preoperatorio de su antiagregación.
Stent coronarios
El uso del stent coronario como tratamiento revascularizante tras un episodio isquémico coronario agudo y su evolución hacia los stent farmacoactivos es fruto de su efectividad para mantener el flujo coronario mantenido en el tiempo tras un accidente isquémico.
Con la técnica clásica de dilatación coronaria con balón la tasa de reestenosis ronda un 30%, circunstancia que disminuye a un 15-20% cuando se usa un stent convencional. Sin embargo, esta cifra desciende a un escaso 5% cuando usamos los stents farmacoactivos. La causa de tal preocupación es que cuando aparece una reestenosis coronaria, un 22-90% presentan un IAM según series, y de ellos un 30-45% fallecen debido a que el nuevo fenómeno isquémico se presenta de manera brusca y sin un preacondicionamiento previo. Esa es una de las razones principales por la que los SFA son cada vez más utilizados.
Necesidad de doble antiagregación
Para entender la antiagregación necesaria en este tipo de pacientes hay que saber que la pared del stent mismo es un potente estimulo para la activación y agregación plaquetaria y, por tanto, de su trombosis y oclusión temprana . La presencia de dicho estimulo permanece hasta que el stent se recubre de un endotelio producido por el propio organismo (cicatrización del stent) cosa que se produce a las 4 u 8 semanas cuando usamos un stent convencional y hasta 18 meses cuando usamos un SFA.
Por otro lado , esta“ cicatrización“ normal y esperable del stent es también la causa de su estenosis, sobre todo en un periodo más tardío, y se origina cuando aparece una hiperplasia neointimal en ese proceso de epitelización. De hecho, Colombo et al 19 nos enseñaron que dicha normalización de la reología dentro del stent eran la principal causa de reestenosis tardía y no los problemas de coagulación a largo plazo, que son subsanados por la terapia antiagregante.
Por tal motivo aparecieron en el mercado una serie de stent con sustancias que impedían la proliferación del músculo liso y la hiperplasia de la intima a base de un recubrimiento de fármacos antiproliferativos. Nacieron entonces los stent farmacoactivos.
Entre dichos fármacos antiproliferativos contamos principalmente con los derivados de la familia ““limus (sirolumus, evorlimus…) y el paclitaxel o taxol adheridos de diferentes maneras a los stent. Esto podría condicionar una cinética distinta en su liberación y, por tanto, unas necesidades diferentes de prevención en la trombosis según el tiempo desde su colocación, cuestión que pocos autores recogen en sus recomendaciones.
En terminos generales, hay un alto nivel de evidencia sobre las ventajas de antiagregar cuando colocamos tales prótesis intracoronarias. Con un grado de evidencia I se afirma que hay una disminución de la tasa de reoclusión al administrar AAS. El estudio ATC, por ejemplo, nos indica una reducción global de reoclusión del 44%. También hay un alto nivel de evidencia para afirmar que existe un mayor grado de efectividad cuando se asocia al AAS una tienopiridina (generalmente clopidogrel), terapéutica recomendada por la mayoria de las guías clínicas 20. Esta doble antiagregación debe ser mantenida en el tiempo hasta la endotelización de la prótesis, cosa que sucede en periodos de tiempo diferentes según hemos visto, ya se trate de SC o SFA.
Como siempre, existen opiniones contrarias, y en este caso dos ensayos clínicos recientes (REAL-LATE y ZEST-LATE) aportan un punto de vista diferente. Tras aleatorizar a 2.701 pacientes portadores de SFA y seguirlos durante 19 meses encontraron una incidencia de muerte cardiovascular e infarto no mortal baja y similar tanto en los grupos tratados con AAS como en los tratados con el clásico AAS+ clopidogrel (1,2% vs 1,8%, p=0,18). Es más, parece que existió una mayor incidencia de eventos graves en el grupo tratado con la doble antiagregación que en los tratados tan solo con AAS ( 3,2% vs 1,8%, p=0,05).
Aunque los riesgos de trombosis en diferentes circunstancias se verán más adelante, diremos a modo de resumen que, a pesar de la doble antiagregación, un 0,5 a 2% de estos pacientes presentan fenómenos trombóticos 22 . Esto no quita razones para que la gran mayoría de autores estén de acuerdo con el alto grado de protección que origina la doble antiagregación. Contando con el apoyo estadístico en la tasa de trombosis del stent originados con la retirada prematura de la doble antiagregación, estimándose un incremento de dicho riesgo multiplicado por 30 cuando esta retirada se produce antes de tiempo.
De hecho, hay una amplia evidencia del riesgo hacia el paciente cuando suspendemos dicha terapeutica. Lo ilustramos con el trabajo de Kaluza et al en el año 2.000, donde observó retrospectivamente que en una pequeña serie de pacientes sometidos a cirugía tras la colocación reciente de un stent (con menos de 6 semanas de duración) la mortalidad postoperatoria rondó el 20% en los casos en los que fue suspendido el tratamiento antiagregante previo a dichas intervenciones. Posteriormente han aparecido más estudios donde se expresa que, de los pacientes que han sufrido trombosis del stent, entre el 33% y el 57% habían suspendido la doble antiagregación 23.
Bibliografía
[1] ISIS-2: (Second International Study of Infarct Survival) Collaborative Group. Randomized trial of intravenous streptokinase, oral aspirin, both, or neither among 17.187 cases of suspected acute myocardial infarction: ISIS-2. J Am Coll Cardiol 1988;12(6 Suppl A):3A-13A. [2] Roux S, Christeller S, Ludin E. Effects of aspirin on coronary reocclusion and recurrent ischemia after thrombolysis: a meta-analysis. J Am Coll Cardiol 1992;19:671-7 [3] Hurlen M, Abdelnoor M, Smith P, Erikssen J, Arnesen H.Warfarin, aspirin, or both after myocardial infarction. N Engl J Med 2002;347:969-74.Van Es RF, Jonker JJ,Verheugt FW, Deckers JW, Grobbee DE. Antithrombotics in the Secondary Prevention of Events in Coronary Thrombosis-2 (ASPECT-2) Research Group.Aspirin and coumadin after acute coronary syndromes (the ASPECT-2 study): a randomised controlled trial. Lancet 2002;360:109-13.
Hurlen M, Smith P, Arnesen H. Effects of warfarin, aspirin and the two combined, on mortality and thromboembolic morbidity after myocardial infarction. The WARIS-II (Warfarin-Aspirin Reinfarction Study) design. Scand Cardiovasc J 2000;34:168-71.
[4] Lewis HD, Davis JW, Archibald DG, Steinke WE, Smitherman TC, Doherty JE, et al. Protective effects of aspirin against acute myocardial infarction and death in men with unstable angina. Results of a Veterans Administration Cooperative Study.N Engl J Med 1983;309:396-403.Cairns JA, Gent M, Singer J, Finnie KJ, Froggatt GM, Holder DA, et al.Aspirin, sulfinpyrazone, or both in unstable angina. Results of a canadian multicenter trial. N Engl J Med 1985;313:1369-75.
Théroux P, Quimet H, McCans J, Latour JG, Joly P, Levy G, et al. Aspirin, heparin or both to treat acute unstable angina. N Engl J Med 1988; 319:1105-11.
The RISC group. Risk of myocardial infarction and death during treatment with low-dose aspirin and intravenous heparin in men with unstable coronary atery disease. Lancet 1990;226:827-30.
Malhotra S, Sharma YP, Grover A, Majumdar S, Hanif SM, Bhargava VK, et al. Effect of different aspirin doses on platelet aggregation in patients with stable coronary artery disease. Intern Med J 2003;33:350-4.
[5] Balsano F, Rizzon P,Violi F, Scrutinio D, Cimminiello C, Aguglia F, et al.Antiplatelet treatment with ticlopidine in unstable angina.A controlled multicenter clinical trial. The Studio della Ticlopidina nell“™Angina Instabile Group. Circulation 1990;82:17-26. [6] CURE:Peters RJ, Mehta SR, Fox KA, Zhao F, Lewis BS, Kopecky SL, et al. Clopidogrel in Unstable angina to prevent Recurrent Events (CURE) Trial Investigators. Effects of aspirin dose when used alone or in combination with clopidogrel in patients with acute coronary syndromes: observations from the Clopidogrel in Unstable angina to prevent Recurrent Events (CURE) study. Circulation 2003;108:1682-7. [7] CREDO: Steinhubl SR, Berger PB, Mann JT, Fry ET, DeLago A,Wilmer C, et al. Early and sustained dual oral antiplatelet therapy following percutaneous coronary intervention: a randomized controlled trial. JAMA 2002; 288: 2411-20. [8] CLASSICS : Bertrand ME, Rupprecht HJ, Urban P, Gershlick AH. Double-blind study of the safety of clopidogrel with and without a loading dose in combination with aspirin compared with ticlopidine in combination with aspirin after coronary stenting: the clopidogrel aspirin stent international cooperative study (CLASSICS). Circulation 2000;102:624-9. [9]STARS: Leon MB, Baim DS, Popma JJ, Gordon PC, Cutlip DE, Ho KK, et al.A clinical trial comparing three antithrombotic-drug regimens after coronary-artery stenting. Stent anticoagulation Restenosis Study Investigators. N Engl J Med 1998;339:1665-71. [10] FANTASTIC :Bertrand ME, Legrand V, Boland J, Fleck E, Bonnier J, mmanuelson H et al. Randomized Multicenter Comparison of Conventional Anticoagulation Versus Antiplatelet Therapy in Unplanned and Elective Coronary Stenting. The Full Anticoagulation Versus Aspirin and Ticlopidine (FANTASTIC)Study. Circulation 1998;98:1597-603. [11]ISAR:Schomig A, Neumann FJ, Kastrati A, Schuhlen H, Blasini R, Hadamitzky M, et al.A randomized comparison of antiplatelet and anticoagulant therapy after the placement of coronary-artery stents. N Engl J Med 1996; 334:1084-9. [12] STARC: Maresta A, Balducelli M, Cantini L, Casari A, Chioin R, Fabbri M, et al.Trapidil (triazolopyrimidine), a platelet-derived growth factor antagonist, reduces restenosis after percutaneous transluminal coronary angioplasty. Results of the randomized, double-blind STARC study. Studio Trapidil versus Aspirin nella Restenosi Coronarica. Circulation 1994; 90:2710-5 [13] The GUSTO IV-ACS Investigators: effect of glycoprotein IIb/IIIa receptor blocker abciximab on outcome in patients with acute coronary syndromes without early coronary revascularization: the GUSTO IV-ACS randomised trial. Lancet 2001;357:1915-24.Brener SJ, Barr LA, Burchenal JE, Katz S, George BS, Jones AA, et al. Randomized,placebo-controlled trial of platelet glycoprotein IIb/IIIa blockade with primary angioplasty for acute myocardial infarction. ReoPro and Primary PTCA Organization and Randomized Trial (RAPPORT) Investigators. Circulation 1998;98:734-41.
Trial of abciximab with and without low-dose reteplase for acute myocardial infarction. Strategies for Patency Enhancement in the Emergency Department (SPEED) Group. Circulation 2000;101:2788-94.
Lincoff AM, Califf RM, Anderson KM,Weisman HF, Aguirre FV, Kleiman NS, et al. Evidence for prevention of death and myocardial infarction with platelet membrane glycoprotein IIb/IIIa rceptor blockade by abciximab (c7E3 Fab) among patients with unstable angina undergoing percutaneous coronary revascularization. J Am Coll Cardiol 97;30:149-56.
The EPILOG Investigators: Platelet glycoprotein IIb/IIIa receptor blockade and low-dose heparin during percutaneous coronary revasularization. N Engl J Med 1997;336:1689-96.
The EPISTENT Study Group: randomised placebo-controlled and balloon- angioplasty-controlled trial to assess safety of coronary stenting with use of platelet glycoprotein IIb/IIIa blockade. Lancet 1998;352:87-92.
Hamm CW, Heeschen C, Goldmann B,Vahanian A,Adgey J, Miguel CM, et al. Benefit of abciximab in patients with refractory unstable angina in relation to serum troponin T levels. c7E3 Fab Antiplatelet Therapy in Unstable Refractory Angina (CAPTURE) Study Investigators. N Engl J Med 1999;340:1623-9.
Topol EJ, Moliterno DJ, Herrmann HC, Powers ER, Grines CL, Cohen DJ, et al. Do Tirofiban and ReoPro Give Similar Efficacy Trial. Comparison of two platelet glycoprotein IIb/IIIa inhibitors, tirofiban and abciximab, for the prevention of ischemic events with percutaneous coronary revascularization. N Engl J Med 2001;344:1888-94. PRISM Study Investigators. A comparison of aspirin plus tirofi-ban with aspirin plus heparin for unstable angina. N Engl J Med 1998; 338:1498-505.
PRISM-PLUS Study Investigators. Inhibition of the platelet gly-coprotein IIb-IIIa receptor with tirofiban in unstable angina and non-Q-wave myocardial infarction. Platelet receptor inhibition in ischemic syndrome management in patients limited by unstable signs and symptoms (PRISMPLUS) study investigators. N Engl J Med 1998;338:1488-97.
Zhao XQ, Theroux P, Snapinn SM, Sax FL. Intracoronary thrombus and platelet glycoprotein IIb/IIIa receptor blockade with tirofiban in unstable angina or non-Q-wave myocardial infarction. Angiographic results from the PRISM-PLUS trial (Platelet receptor inhibition for ischemic syndrome management in patients limited by unstable signs and symptoms).PRISM-PLUS Investigators. Circulation 1999;100:1609-15.
RESTORE Investigators: Effects of platelet glycoprotein IIb/IIIa blockade with tirofiban an adverse cardiac events in patientis with unstable angina or acute myocardial infarction undergoing coronary angioplasty. Circulation 997;96:1445-53.
Randomised placebo-controlled trial of effect of eptifibatide on complications of percutaneous coronary intervention: IMPACT-II. Integrilin to Minimise Platelet Aggregation and Coronary Thrombosis-II. Lancet 1997;349:1422-28.
The PURSUIT Trial Investigators. Inhibition of platelet glycoprotein IIb/IIIa with eptifibatide in patients with acute coronary syndromes. N Engl J Med 1998;339:436-43.
Theroux P, Kouz S, Roy L, Knudtson ML, Diodati JG, Marquis JF, et al. Platelet membrane receptor glycoprotein IIb/IIIa antagonism in unstable angina. The Canadian Lamifiban Study. Circulation 1996;94:899-905.
The PARAGON Trial Investigators. International randomized controlled trial of lamifiban (a platelet glycoprotein IIb/IIIa inhibitor, heparin or both in unstable angina. The PARAGON Investigators. Platelet IIb/IIIa antagonism for the reduction of acute coronary syndrome eventes in a global organization network. Circulation 1998; 97:2386-95.
[14]Chew DP. Et al. Increased Mortality With Oral Platelet Glycoprotein IIb/IIIa antagonists : A Metaanalisis of Phase III Multicenter Randomizaded Trials. Circulation2001: 103:201-6 [15] Hongo Rh, Ley J, Dick SE,Yee RR. The effect of clopidogrel in combination with aspirin when given before coronary artery bypass grafting. J Am Coll Cardiol 2002;40:231-7. [16] Baur HR,VanTassel RA, Pierach CA, Gobel FL. Effects of sulfinpyrazone on early graft closure after myocardial revascularization. Am J Cardiol 1982;49:420-4.Sanz G, Pajaron A, Alegría E, Coello I, Cardona M, Fournier JA, et al. Prevention of early aortocoronary bypass occlusion by low-dose aspirin and dipyridamole. Grupo Español para el Seguimiento del Injerto Coronario (GESIC). Circulation 1990;82:765-73.
Goldman S, Copeland J, Moritz T, Henderson W, Zadina K, Ovitt T, et al. Saphenous vein graft patency 1 year after coronary artery bypass surgery and effects of antiplatelet therapy. Results of a Veterans Administration Cooperative Study. Circulation 1989;80:1190-7.
[17] Goldman S, Copeland J, Moritz T, Henderson W, Zadina K, Ovitt T, et al. Improvement in early saphenous vein graft patency after coronary artery bypass surgery with antiplatelet therapy: results of a Veterans Administration Cooperative Study. Circulation 1988;77:1324-32. [18] Mangano DT, Multicenter Study of Perioperative Ischaemia Research Group. Aspirin and mortality from coronary bypass surgery. N Engl J Med 2002;347:1309-17. [19] Colombo A, Neumann FJ et al. Intracoronary stenting without anticoagulation accomplished with intravascular utrsaound guidance . Circulation 1995, 91 (6).1676-88 [20] Popma JJ et al. Antithrombotic therapy during percutaneus coronary intervention. The 7th AAC conference on antithrombotic an thrombotic therapy . Cheste 2004 . 126 3SupplSilver S et al . Guidelines for percutaneus Coronay intervention Eur Heart J 2005 : 26 (8)
[21] Iakovou I et al. Incidencia predictors and outcomes of thrombosis after successful implantation of drug-eluting stent . JAMA 2005 . 293 [22] Park DW. Et al . Frecuency of and risk factors for the stent thrombosis after drug-eluting stent implantantion during long term follow-up. Am J Cardiol. 2006 . 98 (3)Kuchulakanti PK. Et al . Correlates and long term outcomes of angiographically proven stent trombosis with sirolimus-and paclitaxel eluting stents. Circulation 2006. 113 (8)
[23] Watson H, Belcher G, Horrocks M.Adjuvant medical therapy in peripheral bypass surgery. Br J Surg 1999;86:981-91.Más bibliografía consultada
– PROTOCOLOS DE TRATAMIENTO ANTIAGREGANTES DE LA SEMI (Sociedad Española de Medicina interna), 2.004. Coordinador Demetrio Sánchez Fuentes. Autores José Manuel Barragán Casas, José Luis Hernández Hernández, José Antonio Riancho, Moral, Carmen Suárez Fernández. (pdf)
– HCSC Protocolo antiagregacion. Dra Durán Giménez- Rico. Dr F Duro Ventura. Dra A.M Muñoz de solano Palacios. Dr Borja San Pedro de Urquiza. Dr Siro Tato. Prof F. Lopez Timoneda. Servicio Anestesiologia Hospital Clínico San Carlos. Madrid. España.
– Valoración Preoperatorio del paciente Antiagregado, portador de Stents Coronario. Dra Angeles de Miguel Guijaro. Servicio Anestesiología H. Gregorio Marañón. Madrid. España. Guía Clínica consensuada.
– Manejo Preoperatorio de la Antiagregación en pacientes portadores de Stent Coronario. P. Sierra. P. Tormas et al. Rev esp anest. 2008. 55 8 (Supl 1). (pdf)
– James D; ACCP. The perioperative management of antithrombotic therapy. 8TH EDICITION CHEST 2008:133. (PubMed) (pdf) (html)
– Anticoagulación; Coordinado por Armando Gomez Ortiz MD. Sociedad Colombiana de Cardiología y Cirugía Cardiovascular 2005. (pdf)
– Hall R, Mazer CD. Antiplatelet Drugs: A Review of Their Pharmacology and Management in the Perioperative Period. Anesth Analg. 2011 Feb;112(2):292-318. Epub 2011 Jan 6. (PubMed)
*Adjunto al servicio de anestesiología del Hospital Sanitas la Moraleja. **Adjunto al servicio de urgencias del Hospital Sanitas la Moraleja *** DUE unidad quirúrgica Hospital Sanitas La Moraleja.


 4.3.- Cirugía cardiaca con by-pass
4.3.- Cirugía cardiaca con by-pass  4.4.- Paciente portador de Stent coronario
4.4.- Paciente portador de Stent coronario