Castellanos-González R (1), Jiménez García MJ (1), Pretus Rubio S (2), Díaz Campanero P (2)
(1) FEA Servicio Anestesiología y Reanimación del Hospital Universitario de Getafe
(2) MIR Servicio Anestesiología y Reanimación del Hospital Universitario de Getafe
Cómo citar este artículo: Castellanos González, R., Jiménez García, M. J., Rubio, S. P., & Campanero, P. D. (2021). ¿Utilizamos toda nuestra «artillería analgésica» en los pacientes quemados?. Revista Electrónica AnestesiaR, 13(3). https://doi.org/10.30445/rear.v13i3.905
Introducción y Objetivos
La Asociación Internacional para el Estudio del Dolor (IASP) define el dolor por trauma térmico como “un dolor agudo y grave, que se produce al sufrir una quemadura, continuo con exacerbaciones que declinan gradualmente”. Los pacientes quemados padecen una gran agresión física que genera un dolor intenso y se asocia a un importante sufrimiento físico y emocional acarreando un elevado grado de ansiedad y ocasionando un daño tanto familiar como social.
A pesar de los avances en el estudio de las terapias analgésicas, estos pacientes permanecen infratratados en un alto porcentaje (1), lo que puede influir negativamente en su evolución y asociar un mayor riesgo de aparición de dolor crónico y dolor neuropático.
¿Los estamos tratando adecuadamente? ¿Conocemos las opciones de las que disponemos? El objetivo de esta revisión narrativa es recordar los mecanismos básicos neurofisiopatológicos del dolor generado por quemaduras, así como revisar las herramientas terapeúticas existentes para mejorar el manejo analgésico de esta patología.
Resultados Revisión
El dolor ocasionado por quemaduras tiene distintos componentes:
- Componente nociceptivo: tras la quemadura se produce un aumento de la actividad de las fibras C (cuyos receptores pasan a ser unimodales y detectan cualquier estímulo como doloroso) y de las fibras A delta, y por lo tanto activando las vías nociceptivas corticales a través del asta dorsal medular.
- Componente neuropático: ocasionado por el daño de las terminaciones libres en las zonas lesionadas y por el déficit de reinervación durante la regeneración en las zonas cicatriciales, ocasionando dolor o parestesias.
- Alteración de la modulación: las quemaduras provocan un aumento de la modulación excitatoria provocando:
- Sensibilización periférica: reducción del umbral del dolor. Esto se debe a la liberación de multitud de mediadores inflamatorios (histamina, ATP, óxido nítrico, H+) en la zona de la quemadura. En los pacientes quemados la cantidad de respuesta inflamatoria que se desencadena provoca una alteración del sistema inmune del organismo, incluso desembocando en un síndrome de respuesta inflamatoria (SIRS) en los casos severos (2).
- Sensibilización central: aumento de la excitabilidad neuronal, debido a la activación repetida e intensa de los receptores postsinápticos NMDA del asta dorsal medular. Cuando el estímulo es mayor se produce liberación de glicina que remueve el magnesio del receptor del NMDA provocando su activación, lo que hace que se amplifique la intensidad y la frecuencia de la respuesta.
Estos mecanismos tienen como consecuencia:
- Hiperalgesia térmica: aumento de la intensidad de la respuesta ante estímulos dolorosos en la zona de la quemadura y una hiperalgesia secundaria provocando respuesta nociceptiva también ante estímulos en las zonas sanas que rodean la zona lesionada.
- Alodinia: respuesta dolorosa ante un estímulo que normalmente no es doloroso.
- Fenómeno de hiperexcitabilidad: provoca lo que se llama dolor persistente un tiempo después de que el estímulo doloroso desaparezca.
Hay que tener en cuenta que los pacientes que sufren quemaduras presentan distintas fases durante todo el proceso curativo: dolor basal o continuo (presente en reposo y no ocasionado por procedimientos específicos), dolor por procedimientos (curas, cambio de apósitos, intervenciones quirúrgicas con nuevas agresiones) (Imagen 1), y dolor interrecurrente (que es un episodio de dolor que aparece durante el curso de otro proceso doloroso). Por lo tanto debemos preguntarnos qué debemos pautar en cada momento: es necesario mantener una analgesia basal con rescates para manejar esos picos de dolor provocados en las distintas situaciones del proceso.
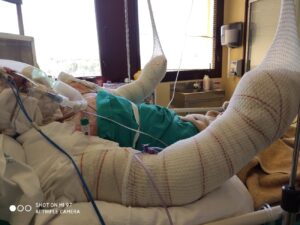
¿Qué opciones terapeúticas tenemos?
- Tratamiento quirúrgico: tratamiento de las escaras y cierre de las zonas cruentas, que provoca una disminución de la zona inflamada y por tanto disminuye el dolor.
- Tratamiento farmacológico:
Para abordar el manejo analgésico desde un punto de vista farmacológico, se utilizan distintos medicamentos con diferentes dianas y distinta potencia.
- Opioides:
Es uno de los fármacos disponible más eficaces para el dolor moderado-severo con componente nociceptivo, especialmente utilizados en la fase aguda de la quemadura (3).
Actúan tanto a nivel periférico como central sobre receptores µ, δ y κ inhibiendo la liberación de neurotransmisores excitatorios en el ganglio de la raíz dorsal y activando las vías descendientes inhibitorias. No previenen la sensibilización central y pueden provocar hiperalgesia secundaria, mecanismo que parece que puede estar relacionado con la tolerancia.
Los pacientes quemados requieren dosis mucho mayores que las dosis estándar para proporcionar analgesia (4). Esto parece explicarse por varios mecanismos. Una vez que los opioides se unen al receptor pueden actuar mediante distintas vías de señalización intracelular. Por un lado, la respuesta clásicamente conocida se realiza a través de la proteína G (efectos analgésicos). Pero también pueden producir su acción a través de β-arrestinas (causante de los efectos de hiperalgesia, tolerancia o depresión respiratoria) (5). Está demostrado que si se eliminan los receptores β-arrestina2 en ratones, mejora la respuesta analgésica de la morfina. Lo interesante es que esta vía actúa a través de la Akt (o protein-kinasa B), cuya fosforilación está disminuída en los daños por quemaduras, por lo que se inactiva y parece ser una de las causas responsables del menor efecto analgésico de los opioides en los pacientes quemados. También contribuye a explicar el desarrollo de tolerancia el hecho de que, tras una exposición repetida al opioide, el receptor se modifica, reclutando y uniéndose a la proteína β-arrestina.
Por otro lado, tras las quemaduras, la expresión y los niveles del receptor se encuentran alterados (disminuyen los receptores µ y las moléculas de señalización del asta dorsal del lado ipsilateral y se produce sobreexpresión de los receptores NMDA).
Es fundamental optimizar el tratamiento con estos fármacos para reducir los efectos secundarios y evitar la adicción. Por ello es importante la evaluación diaria y planificar una juiciosa escalada para adecuar la dosis óptima.
La administración mediante dispositivos de analgesia controlada por el paciente (PCA) ha demostrado ser más eficaz, permitiendo una administración flexible, facilitando el empoderamiento y aliviando la ansiedad.
El fentanilo es de elección en el dolor asociado a procedimiento ya que tiene un inicio de acción rápido por vía endovenosa (1 min) y una vida media relativamente corta (de 30 a 60 min) debido a su rápida distribución.
La morfina es poco soluble en lípidos, tiene un inicio de acción de 3-5 minutos, mayor duración que el fentanilo dejando un mayor efecto residual y permitiendo una titulación intermitente.
Se han estudiado recientemente protocolos de PCA de morfina. Parece que la pauta óptima consiste en indicar bolos de 1.5mg con tiempo de cierre de 7 minutos y una dosis máxima en 24h de 180mg, con dosis adicionales de 3mg/4h si se requieren (6).
Otro fármaco utilizado es el tramadol, opioide de potencia moderada, adecuado para el control del dolor basal moderado. También se ha descrito un efecto beneficioso en el manejo del dolor neuropático, cuya respuesta a los opioides es más controvertida (7).
- AINEs: han demostrado efectividad en dolor moderado en pacientes quemados (3), aunque hay que tener en cuenta que tienen efecto techo y efectos secundarios a nivel gastrointestinal o renal. Pueden disminuir los requerimientos de opioides hasta un 20-30%. Actúan tanto a nivel periférico inhibiendo la inflamación mediada por COX-2, así como a nivel central modulando la inflamación mediante la activación de la microglía.
- Paracetamol: ampliamente utilizado para el tratamiento del dolor de leve a moderado con efecto sinérgico en combinación con los opioides (previniendo la hiperalgesia de éstos). Presenta buen perfil de seguridad.
- Otras alternativas farmacológicas:
Una adecuada estrategia requiere un abordaje multimodal para reducir los efectos comentados debidos al uso de los opioides, con el objetivo de acceder a otras dianas terapeúticas.
- Ketamina: puede disminuir los requerimientos de opioides hasta un 30% (3). Actúan inhibiendo de forma competitiva los receptores NMDA, y disminuye la producción de factores inflamatorios. Es útil en el manejo del dolor neuropático y en la hiperalgesia producida por opioides.
- Gabapentinoides: gabapentina y pregabalina. Aumentan la liberación de neurotransmisores inhibitorios a nivel periférico y disminuyen la activación del receptor NMDA a nivel central. Han demostrado disminuir el dolor en el paciente quemado se recomienda la asociación precoz de pregabalina a dosis titulada de 37.5mg ante la aparición del dolor de dichas características (8).
- Agonistas α2-presinápticos: dexmedetomidina y clonidina. Han demostrado efectos ansiolíticos, analgésicos y son útiles para reducir el uso de opioides. Se pueden asociar a hipotensión por lo que requieren monitorización durante su uso, especialmente en fases agudas de la quemadura. Además son útiles para disminuir la ansiedad. Para el tratamiento durante los procedimientos intervencionistas, hay descritas pautas de dexmedetomidina asociada a ketamina y tramadol (9).
- Lidocaína: bloquea los canales de sodio voltaje-dependientes, produciendo una disminución de la transmisión de la nocicepción en las terminaciones aferentes. Tiene poder antiinflamatorio. Su uso ha sido descrito para tratar el dolor intercurrente pero todavía hay poca evidencia sobre su uso. En una revisión de Cochrane establecen que dado que se ha demostrado que la infusión de lidocaína iv es segura y mejora el dolor neuropático refractario puede ser beneficioso como tratamiento analgésico en quemados (10).
- Antidepresivos: reconocidos en el contexto de una analgesia multimodal. No están indicado para un dolor agudo ya que es necesaria la titulación minuciosa para evitar efectos secundarios. Su efecto se produce a nivel de la espina dorsal modulando la vía descendente inhibitoria. Tienen su papel en el dolor neuropático con elementos de sensibilidad central.
- Medidas no farmacológicas
Como se ha comentado, el dolor de los pacientes con quemaduras tiene componentes emocionales y psicológicos, que requieren un abordaje multidisciplinar. Por lo tanto, existen otras medidas no farmacológicas que pueden contribuir a una mejora en el tratamiento:
- Hipnosis: presenta resultados prometedores. Puede utilizarse previamente a la realización de una cura o desbridamiento.
- Realidad virtual, ha demostrado reducir la puntuación en la valoración del dolor en los pacientes con dolor severo.
- Estimulación eléctrica transcutánea. Consiste en un sistema que genera ondas eléctricas de bajo voltaje y poca intensidad, actuando sobre el sistema nervioso, modificando el umbral y por lo tanto disminuyendo la percepción del dolor. Incluso parece que puede mejorar la reepitelización de los tejidos y el edema.
- Apoyo psicológico en el marco de psicólogos y terapeutas dentro de un abordaje multidisciplinar.
Conclusión
El paciente quemado presenta un dolor intenso y cambiante a lo largo del proceso curativo que exige requerimientos analgésicos adaptados y un abordaje multimodal que exige un conocimiento profundo de su fisiopatología. Tenemos a nuestra disposición múltiples alternativas terapéuticas tanto farmacológicas como no farmacológicas y debemos tener una formación continua para realizar un manejo adecuado y eficaz.
Bibliografía
- Alencar de Castro RJ, Cunha Leal P, Kimiko Sakata R. Tratamiento del dolor en Quemados. Rev Bras Anestesiol. 2013;63:149-153. (HTML)
- Farina Jr. JA, Rosique MJ, Rosique RG. Curbing inflammation in burn patients. Int J Inflam 2013;2013:715645. (PubMed)
- Lipowska James D, Jowza M. Principles of Burn Pain Management. Clin Plastic Surg 2017;44:737-747. (PubMed)
- Tully A, Anderson L, Adams W, Mosier MJ. Opioid creep in burn center discharge regimens: doubled amounts and complexity of narcotic prescriptions over seven years. Burns 2019;45:328-334. (PubMed)
- Emery MA, Eitan S. Drug-specific differences in the ability of opioids to manage burn pain. Burns. 2020;46:503-513. (PubMed)
- Lang TC, Zhao R, Kim A, et al. A Critical Update of the Assessment and Acute Management of Patients with Severe Burns. Adv Wound Care (New Rochelle). 2019;8(12):607‐633. (PubMed)
- Duehmke RM, Derry S, Wiffen PJ, Bell RF, Aldington D, Moore RA. Tramadol for neuropathic pain in adults. Cochrane Database of Systematic Reviews 2017, Issue 6 (PubMed)
- Gray P. Pregabalin in severe burn injury pain: a double blind, randomized placebo-controlled trial. Pain 2011;152:1279-88. (HTML)
- Asmussen S, Maybauer DM, Fraser JF, et al. A metaanalysis of analgesic and sedative effects of dexmedetomidine in burn patients. Burns 2013;39:625-31. (PubMed)
- Wasiak J, Mahar PD, McGuinness SK, Spinks A, Danilla S, Clelnand H, et al. Intravenous lidocaine for the treatment of background or procedural burn pain. Cochrane Database of Sustematic Reviews 2014, Issue 10. (PubMed)

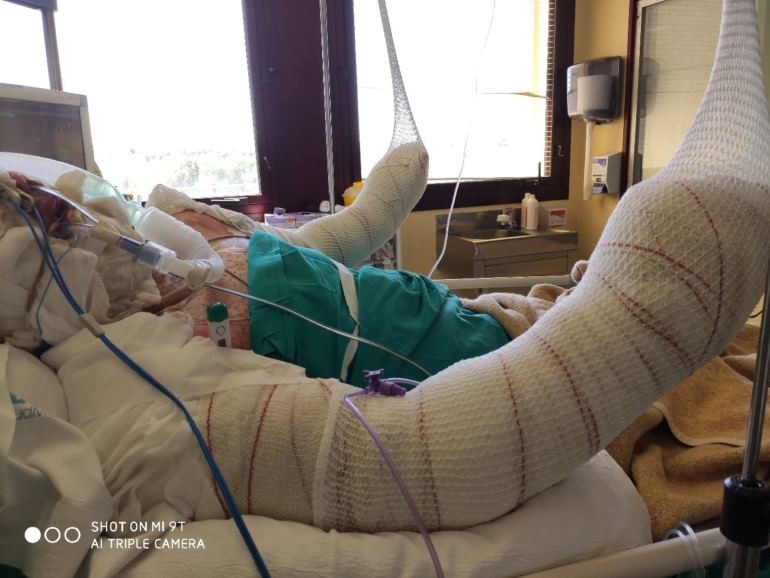




Yo necesito ayuda yo vivo en Seattle,Washington. Mi esposo tubo un accidente automovilístico y se quemo el 50% d su cuerpo de la cintura hacia arriba, le amputaron ya muchos d sus dedos d la manos y lleva ya casi dis meses en coma a sido muy difícil. Yo ocupa ayuda en todas las maneras para el no sé q pase cuando el despierte y no se como tratarlo y ayudarlo por favor ayúdeme.
Buenos días Esmeralda. Como está en coma ahora estará bajo los efectos de la sedación. Igualmente tendrá tratamiento para el dolor. Cuando despierte estará todavía un tiempo ingresado y sus médicos le seguirán poniendo analgesia como hasta ahora. Las unidades donde se tratan los grandes quemados cubren todos los aspectos que los pacientes necesitan. No te preocupes que requiere su tiempo para que puedas ir viendo cómo evoluciona y el tratamiento que irá siguiendo primero en planta y luego en casa. Sus médicos te irán explicando. Ánimo con el proceso. Un abrazo