Cifuentes García B (1), Íñiguez de Onzoño Pérez A (2), López-Torres López J (2), Flores García JA (1)
(1) Médico Interno Residente de Anestesiología y Cuidados Intensivos. Complejo Hospitalario Universitario de Albacete.
(2) Facultativo Especialista de Área de Anestesiología y Cuidados Intensivos. Complejo Hospitalario Universitario de Albacete.
Introducción
El trasplante renal es el tratamiento de elección en la enfermedad renal crónica terminal, presentando menor mortalidad en comparación con otras modalidades de tratamiento renal sustitutivo. Esto queda reflejado en el registro de 2018 de la Sociedad Española de Nefrología en el que la mortalidad de trasplante renal anual fue de 2.6% frente a 15.9% y 9.6%, en caso de hemodiálisis y diálisis peritoneal, respectivamente.
Como anestesiólogos tenemos un papel fundamental en la cirugía de trasplante renal. Empezando por la evaluación preoperatoria, debemos investigar las comorbilidades y complicaciones asociadas a la enfermedad renal crónica con el objetivo de estratificar el riesgo y optimizar el estado clínico del paciente previo al trasplante. En lo que refiere al periodo intraoperatorio, es imprescindible tener en cuenta qué fármacos debemos evitar y cuáles de ellos se asocian a mejores resultados, así como realizar un adecuado manejo hemodinámico.
Este trabajo ofrece una revisión actualizada de lo que un anestesiólogo debe conocer acerca del manejo preoperatorio e intraoperatorio del receptor en la cirugía de trasplante renal.
Evaluación preoperatoria
La insuficiencia renal se asocia con un aumento importante del riesgo de enfermedad cardiovascular y es un factor de riesgo independiente para eventos cardiovasculares en el postoperatorio (infarto de miocardio, ictus e insuficiencia cardiaca) (1). De hecho, la principal causa de muerte tras el trasplante renal son las complicaciones cardiacas (2), por lo que una evaluación cardiológica preoperatoria es de especial importancia en estos pacientes.
La guía de práctica clínica de la Sociedad Europea de Cardiología (ESC) y la European Society of Anesthesiology (ESA) en su actualización del 2014 sobre evaluación y manejo cardiovascular de cirugía no cardiaca incluye el trasplante renal en el grupo de riesgo intermedio (tasa estimada de evento de cardiaco del 1-5% a los 30 días), independientemente de las comorbilidades del paciente. Siguiendo las recomendaciones de esta guía, se recomienda la realización de ECG de 12 derivaciones de forma rutinaria dado que se trata de una intervención de riesgo intermedio con al menos un factor de riesgo para complicaciones cardiacas (disfunción renal), considerando repetirlo de forma anual mientras el paciente permanezca en lisa de espera. No se recomienda la realización de ecocardiografía sistemática a los pacientes programados para cirugía de riesgo intermedio ni la realización de pruebas de imagen con estrés si la capacidad funcional del paciente es normal.
No obstante, la American College of Cardiology y la American Heart Association (ACC/AHA)publicaron en 2012 un documento de consenso de evaluación y manejo cardiaco específico de trasplante renal en el que se considera razonable la realización de un ecocardiograma para valorar la función de ventrículo izquierdo a todos los pacientes candidatos a trasplante renal, así como la realización de pruebas no invasivas de esfuerzo en aquellos pacientes con múltiples factores de riesgo de enfermedad coronaria independientemente de su estado funcional. Los factores de riesgo relevantes incluyen: diabetes mellitus, enfermedad cardiovascular previa, más de un año de diálisis, hipertrofia de ventrículo izquierdo, hipertensión, tabaquismo y dislipemia (3).
Las comorbilidades más frecuentes entre los pacientes en espera de trasplante renal son la diabetes, la obesidad, la patología respiratoria, la enfermedad vascular periférica, la enfermedad cerebrovascular o los trastornos gastrointestinales (2). Estas deben ser valoradas con el objetivo de optimizar al máximo el estado clínico del paciente.
La evaluación preoperatoria debe incluir la posibilidad de que el paciente precise diálisis. La mayoría de los pacientes a los que se les realiza un trasplante renal han iniciado alguna modalidad de tratamiento renal sustitutivo. Sin embargo, en los últimos años está en auge la realización de trasplante renal de forma anticipada, es decir, antes de que se haya iniciado algún tipo de terapia de reemplazo renal. Esta nueva modalidad se asocia a una reducción de pérdida de injerto renal y una reducción de la mortalidad cuando se compara con pacientes en los que ya se ha iniciado algún tratamiento renal sustitutivo (4). De hecho, en el estudio de Meier-Kriesche et al. (5), se demostró de forma estadísticamente significativa que la mortalidad postrasplante aumenta cuanto mayor es el tiempo que ha pasado el paciente en hemodiálisis.
Respecto al periodo preoperatorio inmediato, debe individualizarse la necesidad de hemodiálisis pretrasplante teniendo en cuenta la hiperpotasemia y la sobrecarga de volumen que pueda presentar el paciente. Asimismo, se recomienda la corrección de la acidosis previa al acto quirúrgico ya que ayuda a reducir la elevación de potasio sérico y preserva la función del riñón trasplantado (6).
Manejo intraoperatorio
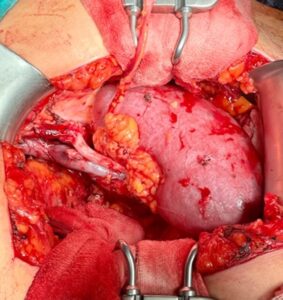
El trasplante renal habitualmente es realizado de forma heterotópica, colocando el injerto en la fosa ilíaca contralateral a la ubicación de origen (es decir, un riñón derecho se posicionaría preferentemente en fosa ilíaca izquierda). Se realiza anastomosis arteriovenosa a vasos ilíacos externos, suturando en primer lugar la vena y a continuación la arteria renal, procedimiento en el que se administra heparina intravascular para reducir el riesgo de trombosis. A continuación, se realiza un reimplante ureteral en la cúpula vesical en el que se inserta un catéter doble J (Imagen 1).
En la tabla 1 se muestran resumidas las recomendaciones de manejo intraoperatorio anestésico del receptor en la cirugía de trasplante renal.
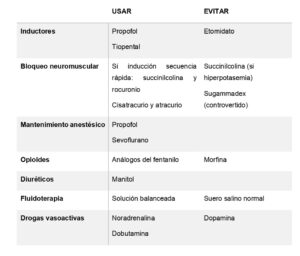
Consideraciones anestésicas
El trasplante renal habitualmente se realiza con anestesia general, no obstante, se han descrito casos con anestesia neuroaxial con resultados clínicos similares a largo plazo (7).
En la posición quirúrgica del paciente se debe prestar atención en evitar la compresión de la extremidad donde se ubica el acceso de diálisis.
En general se deben evitar los fármacos potencialmente nefrotóxicos:
Fármacos inductores
Para la inducción es seguro emplear propofol o tiopental, dado a que estos fármacos son metabolizados en el hígado. Debe evitarse el empleo de etomidato porque causa supresión corticosuprarrenal y aumenta la tasa de mortalidad entre los pacientes críticos (6).
Bloqueantes neuromusculares
Los pacientes con enfermedad renal avanzada y diabetes presentan mayor riesgo de gastroparesia, por tanto, en ellos se debe realizar una inducción de secuencia rápida. Respecto al bloqueante neuromuscular, la succinilcolina aumenta la concentración sérica de potasio, por lo que no se recomienda su empleo en aquellos pacientes que presenten una concentración sérica de potasio elevada previa a la inducción anestésica. Una alternativa es el empleo de rocuronio a dosis de 1.2 mg/kg. Sin embargo, el rocuronio es parcialmente eliminado en el riñón, pudiendo prolongarse su efecto en estos pacientes. Afortunadamente, en los últimos años se ha introducido el sugammadex, una gamma ciclodextrina que revierte el bloqueo neuromuscular inducido por rocuronio al formar un complejo con este en plasma y reduciendo así su cantidad disponible para unirse a los receptores nicotínicos en la unión neuromuscular. Sin embargo, actualmente, la Agencia Española de Medicamentos y Productos Sanitarios y la Food and Drug Administration (FDA) no recomiendan su uso en pacientes con insuficiencia renal grave. Esto se debe a que el complejo sugammadex-rocuronio es eliminado sin cambios por vía renal, existiendo la posibilidad de recurrencia de bloqueo neuromuscular si los dos fármacos se disocian. Varios estudios farmacocinéticos han observado que el aclaramiento de sugammadex y rocuronio es mucho menor en pacientes con insuficiencia renal grave que en los controles sanos. A pesar de ello, en estos trabajos ningún paciente mostró signos de recurarización (8–10).
Si no es necesaria una inducción de secuencia rápida, el cisatracurio o atracurio pueden ser los bloqueantes neuromusculares de elección dado que no dependen de la excreción renal para su eliminación.
Es importante mantener un adecuado bloqueo neuromuscular durante la intervención para proporcionar unas condiciones quirúrgicas óptimas, siendo recomendada la monitorización neuromuscular (6).
Mantenimiento anestésico
El sevoflurano es un fármaco seguro para el mantenimiento anestésico, así como el isoflurano y desflurano (6). A pesar de que hay evidencia de que el compuesto A (producto terminal resultado de la degradación del sevoflurano por los absorbentes de dióxido de carbono) es nefrotóxico en ratas (11), no se ha demostrado este efecto en humanos (12). Además, se ha observado en animales que el sevoflurano atenúa el daño renal por isquemia-reperfusión cuando se compara con ketamina o pentobarbital mediante la reducción de la respuesta inflamatoria (13).
Otra opción, es la realización de una anestesia intravenosa total con infusión continua de propofol. Un ensayo clínico aleatorizado reciente no encontró diferencias significativas en la función renal postrasplante en función a la técnica anestésica empleada (regional, general balanceada o total intravenosa) (7). Asimismo, el propofol ha demostrado presentar un efecto protector contra el daño renal por isquemia-reperfusión (14). Actualmente, está en fase de reclutamiento un estudio europeo multicéntrico aleatorizado que compara la incidencia de retraso en la función del injerto cuando se emplea anestesia basada en propofol versus anestesia basada en sevoflurano (ClinicalTrials.gov Identifier: NCT02727296).
Opioides
Debe emplearse la morfina con precaución, debido a que sus metabolitos activos son eliminados por vía renal. En cambio, el fentanilo, alfentanilo, sulfentanilo y remifentanilo pueden emplearse de forma segura (6).
Diuréticos
Hay evidencia que sostiene que el empleo de 200 a 250 ml de manitol 20% inmediatamente antes de la reperfusión del injerto previene de la insuficiencia renal postrasplante. El manitol actúa como agente osmótico reduciendo el edema celular que ocurre con la isquemia y reperfusión (15). Sin embargo, no debemos de pasar por alto que su empleo no está exento de efectos secundarios, como la deshidratación o alteraciones electrolíticas (hipernatremia o acidosis, entre otras).
Una práctica extendida es el empleo de furosemida perioperatoria para incrementar la diuresis tras la reperfusión, sin embargo, no hay evidencia sólida que justifique su uso, siendo necesarias más investigaciones (16).
Manejo hemodinámico
Es fundamental mantener una adecuada perfusión del injerto para reducir las secuelas de la isquemia-reperfusión. Los mecanismos de autorregulación que mantienen el flujo sanguíneo renal están ausentes en el riñón recién trasplantado, siendo el parénquima renal más sensible a los cambios de la presión arterial sistémica. Por tanto, es primordial asegurar un adecuado gasto cardiaco mediante la corrección de la hipovolemia antes de la reperfusión del injerto renal (2).
Monitorización
Respecto a la monitorización, en la revisión publicada por Schmid et al. en European Society of Anaesthesiology en 2012 se recomienda el uso de ECG, presión arterial no invasiva y saturación de oxígeno periférica en todos los pacientes, reservando la presión venosa central, la presión arterial invasiva y la monitorización avanzada para casos seleccionados (6).
Asimismo, la canalización un acceso venoso central puede resultar útil en caso de precisarse la administración de drogas vasoactivas o inmunosupresores, sin embargo, no es necesaria de forma rutinaria en todos los pacientes.
Fluidoterapia
Tradicionalmente, se ha empleado suero salino fisiológico en la cirugía de trasplante renal debido a la creencia de que así se evita la hiperpotasemia relacionada con las soluciones balanceadas. Paradójicamente, la infusión de cloruro de sodio al 0.9% produce más hiperpotasemia que la solución balanceada que contiene potasio. Esto se debe a que la infusión de suero salino fisiológico causa acidosis metabólica hiperclorémica lo que provoca la entrada del ión H+ al interior de las células desplazando el potasio fuera de las mismas, aumentando el potasio extracelular. Un ensayo clínico aleatorizado doble ciego publicado recientemente observó que los pacientes que recibieron cloruro de sodio al 0.9% en comparación con Plasma-Lyte 148® en cirugía de trasplante renal presentaron mayor incidencia de acidosis metabólica hiperclorémica e hiperpotasemia, sin asociarse a peores resultados clínicos (17). Además, también se ha observado que el empleo de soluciones balanceadas con acetato reduce la necesidad de drogas vasoactivas e hipotensión perioperatoria (18). En consecuencia, parece más adecuado el empleo de soluciones balanceadas en el trasplante renal.
Respecto a los coloides, no se recomienda su uso rutinario en la cirugía de trasplante renal, pudiendo ser ineficaces e incluso perjudiciales al asociarse a retraso en la función de injerto (2).
Drogas vasoactivas
Es fundamental evitar la hipotensión sobre todo tras la reperfusión del injerto. Se debe considerar el empleo de drogas vasoactivas si el paciente no tolera la sobrecarga de volumen, a pesar del riesgo de vasoconstricción renal (6).
El empleo de dopamina a dosis bajas en el receptor de trasplante renal ha sido ampliamente estudiado. Sin embargo, actualmente no se recomienda su uso pues no ha demostrado mejorar la función renal postrasplante y puede aumentar la mortalidad y la estancia en las Unidades de Cuidados Intensivos (19).
Conclusiones
- La evaluación preoperatoria cardiaca es fundamental, siendo las complicaciones cardiacas la principal causa de muerte postrasplante.
- En el preoperatorio inmediato no se recomienda la realización de diálisis de forma rutinaria, individualizándose su requerimiento.
- La estrategia anestésica deber ir enfocada a evitar los fármacos nefrotóxicos. La inducción es segura con propofol o tiopental. Si es necesaria una inducción de secuencia rápida se puede emplear succinilcolina (si los niveles de potasio sérico no están elevados) o rocuronio. El cisatracurio y atracurio son los bloqueantes neuromusculares más recomendables si ésta no se precisa.
- Tanto la anestesia balanceada como total intravenosa son modalidades válidas para el mantenimiento anestésico.
- Debe emplearse la morfina para analgesia postoperatoria con precaución.
- Es primordial mantener una adecuada perfusión del injerto mediante la corrección de la hipovolemia y el mantenimiento tensional adecuado.
- Las soluciones balanceadas son las más adecuadas para la fluidoterapia en el trasplante renal.
Bibliografía
1. 2014 ESC/ESA Guidelines on non-cardiac surgery: cardiovascular assessment and management: The Joint Task Force on non-cardiac surgery: cardiovascular assessment and management of the European Society of Cardiology (ESC) and the European Society of Anaesthesiology (ESA). Eur Heart J. 2014 Sep 14;35(35):2383–431. (HTML)
2. Mittel AM, Wagener G. Anesthesia for Kidney and Pancreas Transplantation. Anesthesiology Clinics. 2017 Sep;35(3):439–52. (HTML)
3. Lentine KL, Costa SP, Weir MR, Robb JF, Fleisher LA, Kasiske BL, et al. Cardiac Disease Evaluation and Management Among Kidney and Liver Transplantation Candidates. Journal of the American College of Cardiology. 2012 Jul;60(5):434–80. (PDF)
4. Kasiske BL, Snyder JJ, Matas AJ, Ellison MD, Gill JS, Kausz AT. Preemptive kidney transplantation: the advantage and the advantaged. J Am Soc Nephrol. 2002 May;13(5):1358–64. (HTML)
5. Meier-Kriesche HU, Port FK, Ojo AO, Rudich SM, Hanson JA, Cibrik DM, et al. Effect of waiting time on renal transplant outcome. Kidney Int. 2000 Sep;58(3):1311–7. (HTML)
6. Schmid S, Jungwirth B. Anaesthesia for renal transplant surgery: an update. European Journal of Anaesthesiology. 2012 Dec;29(12):552–8. (HTML)
7. Calixto-Flores A, Román-Sánchez M, Jiménez-Sánchez E, Cruz-Santiago J, Meza-Jiménez G, Bernáldez-Gómez G. Evaluation of Renal Function at 24, 48, and 72 Hours and 3 Months After Transplant: Comparison of 3 Anesthetic Techniques. Transplantation Proceedings. 2020 May;52(4):1094–101. (HTML)
8. Staals LM, Snoeck MMJ, Driessen JJ, van Hamersvelt HW, Flockton EA, van den Heuvel MW, et al. Reduced clearance of rocuronium and sugammadex in patients with severe to end-stage renal failure: a pharmacokinetic study†. British Journal of Anaesthesia. 2010 Jan 1;104(1):31–9. (HTML)
9. Panhuizen IF, Gold SJA, Buerkle C, Snoeck MMJ, Harper NJN, Kaspers MJGH, et al. Efficacy, safety and pharmacokinetics of sugammadex 4 mg kg-1 for reversal of deep neuromuscular blockade in patients with severe renal impairment. Br J Anaesth. 2015 May;114(5):777–84. (HTML)
10. Adams DR, Tollinche LE, Yeoh CB, Artman J, Mehta M, Phillips D, et al. Short-term safety and effectiveness of sugammadex for surgical patients with end-stage renal disease: a two-centre retrospective study. Anaesthesia. 2020;75(3):348–52. (HTML)
11. Gonsowski CT, Laster MJ, Eger EI, Ferrell LD, Kerschmann RL. Toxicity of compound A in rats. Effect of a 3-hour administration. Anesthesiology. 1994 Mar;80(3):556–65. (PubMed)
12. Ebert TJ, Arain SR. Renal responses to low-flow desflurane, sevoflurane, and propofol in patients. Anesthesiology. 2000 Dec;93(6):1401–6. (PubMed)
13. Lee HT, Ota-Setlik A, Fu Y, Nasr SH, Emala CW. Differential protective effects of volatile anesthetics against renal ischemia-reperfusion injury in vivo. Anesthesiology. 2004 Dec;101(6):1313–24. (PubMed)
14. Motayagheni N, Phan S, Eshraghi C, Nozari A, Atala A. A Review of Anesthetic Effects on Renal Function: Potential Organ Protection. Am J Nephrol. 2017;46(5):380–9. (PubMed)
15. Lugo-Baruqui JA, Ayyathurai R, Sriram A, Pragatheeshwar KD. Use of Mannitol for Ischemia Reperfusion Injury in Kidney Transplant and Partial Nephrectomies—Review of Literature. Curr Urol Rep. 2019 Jan;20(1):6. (PubMed)
16. Sandal S, Bansal P, Cantarovich M. The evidence and rationale for the perioperative use of loop diuretics during kidney transplantation: A comprehensive review. Transplantation Reviews. 2018 Apr 1;32(2):92–101. (HTML)
17. Weinberg L, Harris L, Bellomo R, Ierino FL, Story D, Eastwood G, et al. Effects of intraoperative and early postoperative normal saline or Plasma-Lyte 148® on hyperkalaemia in deceased donor renal transplantation: a double-blind randomized trial. Br J Anaesth. 2017 Oct 1;119(4):606–15. (PubMed)
18. Pfortmueller C, Funk G-C, Potura E, Reiterer C, Luf F, Kabon B, et al. Acetate-buffered crystalloid infusate versus infusion of 0.9% saline and hemodynamic stability in patients undergoing renal transplantation : Prospective, randomized, controlled trial. Wien Klin Wochenschr. 2017 Sep;129(17–18):598–604. (PubMed)
19. Ciapetti M, di Valvasone S, di Filippo A, Cecchi A, Bonizzoli M, Peris A. Low-Dose Dopamine in Kidney Transplantation. Transplantation Proceedings. 2009 Dec;41(10):4165–8. (HTML)




Excelente revisión .
Permite abordar aspectos relevantes que deben ser considerados en la anestesia del trasplante renal . Otros serían: condiciones óptimas para que los pacientes sean intervenidos Hb. Técnicas conductivas para reducir anestésicos y dolor postoperatorio . Transfusiones.Albúmina. Tipos de Diálisis .Riñón de Cadaver o de vivo relacionado .Manejo de insuficiencia cardíaca …
Gracias por publicar este artículo
Necesidad urgente de donantes de riñón A + ve y O + ve. Ofrecemos $ 500,000.00 USD por un solo riñón. Damos la mitad del monto ($ 250,000.00 USD) a los donantes antes de la cirugía, inmediatamente después de la documentación. Luego, se proporciona un equilibrio completo después de la cirugía.Número de WhatsApp: +917873223513
Comuníquese con el Dr. Antony Robert Charles del Hospital Bautista de Bangalore
Número de WhatsApp: +917873223513