Parreño Buedo D, Charco Roca LM.
Facultativo Especialista de Área de Anestesiología y Cuidados Intensivos. Complejo Hospitalario Universitario de Albacete.
Introducción
Como resultado del notable aumento de la industria química en los últimos años, la posibilidad de que ocurra una intoxicación aguda ya sea accidental o voluntaria, crece de forma vertiginosa en nuestros días.
Es frecuente recibir en los Servicios de Emergencias a pacientes en quienes se sospecha algún tipo de intoxicación y otros en quienes los antecedentes de intoxicación son obvios. Dependiendo de la clínica o las potenciales complicaciones estos pacientes pueden ser candidatos a ingreso en la Unidad de Cuidados Intensivos (UCI).
El manejo del paciente intoxicado agudo se basa en seis puntos (1) (Tabla 1). Aunque las maniobras de estabilización inicial son el pilar fundamental en el tratamiento del paciente intoxicado, las terapias extracorpóreas (TE) juegan un papel crucial, si no esencial, en un subconjunto de intoxicaciones para prevenir o revertir una toxicidad grave.
El grupo de trabajo EXTRIP desarrolló una metodología detallada de cómo actuar en este subconjunto de intoxicaciones formado, hasta la fecha, por 13 fármacos susceptibles para ser tratadas con dichas técnicas (2).
La presente revisión tiene como objetivo describir aspectos relacionados con el tratamiento de las intoxicaciones agudas, tratando inclusive aspectos farmacológicos y básicos que presentan este tipo de sustancias tóxicas. Se realizó una búsqueda bibliográfica en Pubmed y Medline con la siguiente estrategia: (Intoxication OR poisons OR overdose) AND (extracorporeal therapy OR extracorporeal treatment OR hemodialysis OR hemofiltration OR haemodialysis OR CRRT). Se completó la búsqueda de información revisando las publicaciones que el grupo de trabajo EXTRIP proporciona en http://www.extrip-workgroup.org/recommendations.
Tóxicos frecuentes en las intoxicaciones agudas y aproximación a su manejo
Las Tablas 2 y 3 resumen la potencial dializabilidad de los tóxicos basada en sus propiedades fisicoquímicas y farmacocinéticas.
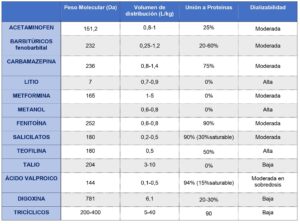
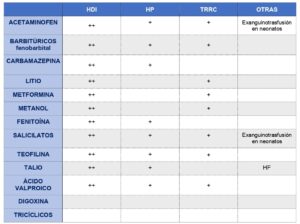
Abreviaturas: HDI; hemodiálisis intermitente, HP; hemoperfusión, TRRC; terapia de reemplazo renal contínua, HF; hemofiltración.
1. Acetaminofeno (Paracetamol).
El acetaminofeno es el analgésico más comúnmente utilizado a nivel mundial desde que se introdujo en el año 1955 y es la causa principal de insuficiencia hepática aguda fulminante inducida por fármacos.
El paracetamol es moderadamente dializable; presenta un peso molecular (PM) pequeño de 151Da, baja unión a proteínas 10-30% y un volumen de distribución 0,9-1,0 L/kg.
El pilar fundamental del tratamiento y el único necesario en la mayoría de las intoxicaciones es su antídoto altamente eficaz: La N-acetilcisteína (NAC). Sin embargo, en casos de intoxicación aguda grave con signos de disfunción mitocondrial (acidosis metabólica y alteración del estado mental) previos al inicio del fallo hepático, dicho antídoto no es suficiente a pesar de su ingesta precoz durante las primeras 8 horas (3).
El grupo de trabajo EXTRIP recomienda TE de manera adyuvante al tratamiento con NAC en casos como:
– Casos graves de intoxicación por Acetaminofén, con signos de insuficiencia mitocondrial temprana como coma, concentración elevada de lactato y acidosis metabólica.
– Concentraciones plasmáticas superiores a 1000mg/L (6620 μ mol / L) a pesar de inicio de NAC.
– Signos de insuficiencia mitocondrial, concentraciones superiores a 700 mg / L (4630 μ mol / L) y no se administra NAC (por falta de disponibilidad de dicho antídoto o alergia documentada del mismo).
– Signos de insuficiencia mitocondrial, concentraciones superiores a 900 mg/L (5969 μ mol / L) a pesar de inicio de NAC.
La hemodiálisis intermitente (HDI) es la modalidad de primera elección. Hemoperfusión (HP) intermitente o terapia de reemplazo renal continua (TRRC) son válidas como segunda opción. La exanguinotransfusión es una alternativa adecuada en neonatos.
El NAC es eliminado por técnicas extracorpóreas por lo que su dosis debe aumentarse durante la aplicación de las mismas.
La finalización de las TE se recomienda cuando existe una mejoría clínica sostenida evidente. El grupo EXTRIP prefirió criterios clínicos frente a guiarse por la concentración plasmática.
2. Barbitúricos (4).
Estos fármacos se dividen en dos grupos:
– De acción corta; se unen en un alto porcentaje a proteínas y son más solubles en lípidos, tienen un rápido inicio de acción con menor duración y son metabolizados casi exclusivamente en el hígado.
– De acción larga; se acumulan muy poco en tejidos (tienen un volumen de distribución pequeño), son menos solubles en lípidos y se excretan como fármacos activos por los riñones. En consecuencia, son más susceptibles de ser eliminados por TE.
El barbitúrico que con mayor frecuencia se asocia a casos de intoxicación aguda es el fenobarbital. Su rango terapéutico como anticonvulsivante es de 10-25 mg/L, concentraciones séricas de 50mg/L pueden inducir coma y superiores a 80mg/L pueden ser letales.
Para el tratamiento de la intoxicación por barbitúricos las medidas de apoyo son lo prioritario y además se deben proporcionar tratamientos que ayuden a acelerar la eliminación como (dosis múltiples de carbón activo) que deben usarse antes y durante las TE.
El grupo EXTRIP recomienda TE en casos de intoxicaciones por barbitúricos de acción prolongada cuando se presente uno o más de los siguientes:
– Coma.
– Shock refractario a fluidoterapia.
– Persistencia de toxicidad a pesar de tratamiento con carbón activo.
– Persistencia de concentración sérica elevada a pesar de tratamiento con carbón activo.
– Depresión respiratoria que precisa de ventilación mecánica.
La muerte por intoxicación por barbitúricos se limita principalmente a pacientes en coma con depresión respiratoria y/o shock asociados, siendo más probable en paciente con enfermedad pulmonar obstructiva crónica previa.
Por ello las TE deben iniciarse lo antes posible, durante las primeras 24 horas tras la exposición, para evitar un coma prolongado: La HDI es la modalidad indicada. HP y TRRC son alternativas aceptables en adultos en caso de no disponer de HDI.
La finalización de la técnica está indicada cuando la mejoría clínica es evidente y la terapia no debe ser interrumpida hasta observar dicha mejoría. Se deben monitorizar las concentraciones séricas para valorar la eficacia del tratamiento pero no para determinar el momento de la interrupción.
3. Carbamazepina (5).
Aunque ocurre en raras ocasiones, una intoxicación aguda puede causar efectos clínicos graves, sobre todo con dosis superiores de 40 mg/L (169 μmol / L). Dado que las concentraciones séricas de carbamazepina están disponibles en la mayoría de los centros en, tiempos relativamente rápidos, su monitorización es un factor relevante para guiar las decisiones del tratamiento.
El fármaco es moderadamente dializable: Es una molécula pequeña (PM de 236 Da), altamente unida a proteínas, tanto albúmina como glicoproteína alfa-1 en un 70-80%, porcentaje que no disminuye en sobredosis. Es altamente lipofílica distribuyéndose rápida y extensamente, con un gran volumen de distribución 0,8 a 1,4L/Kg.
La mayoría de intoxicaciones por cabamazepina se tratan con medidas de apoyo y dosis múltiples de carbón activo (DMCA). Sin embargo, aunque acelera la eliminación del fármaco el efecto suele ser incompleto y a menudo limitado por causas clínicas asociadas a esta intoxicación, como íleo paralítico.
Por ello el grupo de trabajo EXTRIP recomienda la aplicación TE en los siguientes casos:
– Convulsiones no controladas,
– Arritmias potencialmente mortales.
– Coma prolongado o depresión respiratoria.
– Persistencia de toxicidad significativa a pesar de medidas de apoyo y DMCA.
También se recomienda continuar con DMCA a la vez que se aplican TE ya que su efecto sobre la eliminación es aditivo, siempre y cuando las vías respiratorias estén protegidas.
La modalidad más empleada de TE en este contexto ha sido la HP intermitente. Sin embargo actualmente dada las mejoras tecnológicas, es la HDI la que se recomienda como primera opción. La finalización del tratamiento está indicada cuando exista una mejora clínica evidente y mantenida y, cuando la concentración plasmática se encuentre por debajo de 10 mg/L. Tras finalizar las TE, se deben continuar controlando las concentraciones séricas de carbamazepina por posible efecto rebote.
4. Litio (6).
El estrecho rango terapéutico del litio lo convierte en un fármaco de difícil manejo, con abundantes efectos adversos y alta frecuencia de intoxicaciones.
La dosis terapéutica es 0,6-1,2 mEq/L, se cataloga como toxicidad leve 1,5-2,5 mEq/L, moderada 2,5-3,5 mEq/L y severa 3,5-5 mEq/L.
El litio es altamente dializable: Presenta un bajo PM, baja depuración endógena, baja unión a proteínas y un bajo volumen de distribución 0,5 L/kg inicialmente, aumentando con el tiempo a 0,7-0,9 L/kg. La distribución a los tejidos lo hace siguiendo un modelo multicompartimental con retraso en la difusión del compartimento extracelular al intracelular.
Como medidas de apoyo deben iniciarse la fluidoterapia, lavado gástrico e irrigación de todo el intestino con polietilenglicol (el carbón activo no absorbe el litio). Pero dadas sus propiedades farmacocinéticas, el tratamiento más eficiente ante una intoxicación grave por litio es la HDI ya que, lo reduce a un ritmo superior al aclaramiento endógeno eliminándolo rápidamente del sistema nervioso central. La HDI debe mantenerse un mínimo de 6 horas si no se dispone de la medición de concentración de litio.
Las TRRC también son una alternativa en caso de no disponer de HDI o en casos de efecto rebote, como terapia prolongada adicional una vez finalizado el primer tratamiento con HDI.
Se recomiendan TE cuando:
– Función renal alterada y concentración de Litio es de 4 mEq/L.
– Bajo nivel de conciencia, convulsiones o arritmias potencialmente mortales.
– Si se desea reducir la concentración de litio a 1 mEq/L en menos de 36 horas.
Se recomienda el cese de TE cuando la concentración de Litio es 1 mEq/L o la mejoría clínica es evidente.
Tras la finalización de TE, se debe observar al paciente durante un mínimo de 12 horas, por el frecuente efecto rebote que puede ocurrir tanto por redistribución como por absorción desde tracto gastrointestinal.
5. Metformina.
La intoxicación aguda por metformina presenta una mortalidad de hasta el 30% debido, en la mayoría de las ocasiones, por cuadros de acidosis láctica asociada a metformina (MALA); definida como concentraciones de lactato superiores a 5mmolL y pH arterial menor a 7,35 con exposición previa a metformina.
Son varios los tratamiento aplicados en caso de intoxicación aguda, en particular terapias extracorpóreas como hemodiálisis y hemofiltración. De hecho, una reciente revisión señala que la intoxicación por metformina, fue la causa toxicológica más común donde se aplicaron TE (7).
Es un tóxico moderadamente dializable: Tiene un bajo PM (165 Da) y no se une a proteínas. El factor limitante para su eliminación mediante TE es su gran VD de 1 a 5 L/kg con amplia distribución intracelular incluidos los eritrocitos; sin embargo, se ha comprobado que en casos de insuficiencia renal o intoxicación este VD disminuye.
La concentración plasmática letal es mayor 50mg/mL y la dosis tóxica se considera cuando se administran más de 5 gramos.
Se recomienda el uso de TE debito a la alta mortalidad asociada a MALA ya que las opciones de tratamiento se limitan a medidas de apoyo y perfusión de bicarbonato. Se debe iniciar TE cuando los niveles de lactato sean superiores a 2 mmol/L, pH ≤ 7 y las medidas de apoyo fracasen. También se sugieren en casos de inestabilidad hemodinámica, insuficiencia renal, insuficiencia hepática y disminución del nivel de conciencia.
La técnica inicial que se recomienda es la HDI. Las TRRC también están indicadas en caso de no disponer de HDI, pero aplicando dosis superiores a las utilizadas en cuadros de insuficiencia renal aguda.
Dado que la metformina no se une a proteínas plasmáticas, la HP, dispositivos de asistencia hepática o intercambio de plasma no ofrecen ninguna ventaja y no están indicados.
La finalización de las TE está indicada cuando la concentración sérica de lactado es inferior a 3mmol/L y pH superior a 7,35. Debido a la naturaleza impredecible del rebote, se debe monitorizar de cerca el estado ácido-base, especialmente para determinar si se inicia de nuevo la terapia o no.
6. Metanol (8).
La intoxicación por metanol puede producir alteraciones visuales, trastornos motores y cognitivos, con una mortalidad de hasta el 40% si no se aplican las medidas adecuadas.
Se metaboliza por la enzima alcohol deshidrogenasa hepática (ADH) a formaldehído y luego a ácido fórmico, considerado el principal compuesto tóxico. Antídotos, como el etanol y fomepizol, son inhibidores competitivos de la ADH y previenen la biotransformación tóxica y progresión de la toxicidad.
Es un tóxico altamente dializable. Tiene un bajo VD de 0,77 L/kg, y tanto el metanol como el ácido fórmico se eliminan fácilmente mediante TE. Los beneficios clínicos de dichas terapias incluyen la prevención de la toxicidad (mejoran las alteraciones bioquímicas, eliminan metanol) y facilitan reversión de la neurotoxicidad.
Se debe comenzar de manera precoz con TE en casos de intoxicación grave por metanol, que está determinada por:
– Coma, convulsiones, déficits visuales.
– Acidosis metabólica con pH ≤ 7,15
– Acidosis metabólica persistente a pesar de antídotos y medidas de apoyo.
– Anión gap (AG) >24 mmol/L. Un AG de 20 mmol/L es aproximadamente igual a una concentración de ácido fórmico sérico de 5 mmol/L (200 mg/L), que se ha sugerido que es la concentración tóxica mínima (19).
– Concentración sérica de metanol superior a 700mg/L (en terapia con fomepizol); más de 600mg/L en terapia con etanol; superior a 500mg/L en ausencia de bloqueador de ADH.
– En el contexto de la función renal alterada.
La HDI es la modalidad de elección. Las TRRC son alterativas aceptables en caso de no disponer de HDI. Debe evitarse la anticoagulación sistémica porque es posible que la administración de anticoagulantes pueda aumentar el desarrollo o la gravedad de hemorragia intracraneal.
Se debe continuar el tratamiento con antídoto durante las TE, teniendo en cuenta que dicho antídoto es eliminado por las TE por lo que las dosis de mantenimiento deben ser al menos duplicadas. El tratamiento puede finalizar cuando la concentración de metanol es <200 mg/L o 6.2 mmol/L y presenta mejoría clínica.
7. Fenitoína (9).
La intoxicación aguda por fenitoína se caracteriza por efectos cerebelosos y vestibulares; en casos de intoxicación grave puede resultar en coma y depresión respiratoria.
Es moderadamente dializable. Presenta un bajo PM (252 Da), VD pequeño (0.6 a 0.8 L/kg), pero se une ampliamente a proteínas (90%, porcentaje que permanece sin cambios en casos de sobredosis pero que disminuye levemente en casos de insuficiencia renal, hipoalbuminemia y desnutrición).
En caso de intoxicación aguda, los síntomas potencialmente mortales son poco frecuentes y generalmente se resuelven por completo con el tratamiento de apoyo adecuado. No existen antídotos para revertir los efectos tóxicos de la fenitoína y el uso de carbón activado en dosis múltiples sigue siendo controvertido.
Dada su elevada unión a proteínas, la HP y el recambio plasmático han sido las TE más indicadas en las últimas décadas. Actualmente, debido a las mejoras tecnológicas, es la HDI la terapia recomendada como primera opción, dejando a la anteriores como alternativas.
Las indicaciones para aplicar TE se basan únicamente en los síntomas clínicos:
– Coma prolongado.
– Ataxia incapacitante prolongada.
– No se recomiendan TE ante una sospecha de fenitoína ingerida.
– No se recomienda TE basándose únicamente en la concentración sérica de fenitoína.
La finalización de las técnicas está indicada cuando la mejoría clínica es evidente. Se debe monitorizar tanto el estado clínico como las concentraciones séricas de fenitoína durante al menos 24 horas, por el riesgo de efecto rebote y la posible necesidad de continuar con TE.
8. Salicilatos (10).
El término «salicilatos» se refiere a todas las formas, la mayoría ácido acetilsalicílico (aspirina) y salicilato de metilo. Actualmente las intoxicaciones agudas por salicilatos siguen siendo una causa importante de muerte en todo el mundo.
Son sustancias moderadamente dializables: PM de 180 Da, se unen ampliamente a la albúmina (90%) pero es un proceso saturable y puede disminuir al 30% tras una sobredosis y tienen un bajo VD (0,2 L / kg).
Los pilares del tratamiento en caso de intoxicación son los cuidados de apoyo, descontaminación gastrointestinal, reposición de volumen intravascular y administración de bicarbonato.
Queda reservado el tratamiento con TE para:
– Casos graves de alteración del estado mental: las TE son los únicos procedimientos que reducen rápidamente la carga de salicilato circulante de manera eficiente, corrigiendo la acidemia y por tanto, disminuyendo la entrada del fármaco al sistema nervioso central. Las TE reducen la carga de fármaco previniendo el desarrollo de edema cerebral.
– Concentración superior a 7,2 mmol/L (100mg/dL), 6,5 mmol/L (90 mg/dL) en pacientes con insuficiencia renal crónica, incluso 5,8 mmol/L (80 mg / dL) en casos de insuficiencia renal aguda; en ausencia de síntomas clínicos.
– Si el pH sanguíneo ≤ 7,20: incluso la acidosis leve es causa de intoxicación grave, independientemente de si es metabólica o respiratoria.
– Hipoxemia que precisa de oxigenoterapia: El síndrome de distrés respiratorio agudo (SDRA) es una manifestación clínica característica de la intoxicación aguda grave por salicilatos. El grupo de trabajo EXTRIP lo considera indicación independiente para tratamiento con terapias extracorpóreas.
– Si el tratamiento de apoyo fracasa (bicarbonato, fluidoterapia, etc.).
La modalidad indicada es HDI. La HP y las TRRC son alternativas aceptables en caso de no disponer de HDI. La exanguinotrasfusión queda reservada para neonatos.
La finalización de TE está indicada cuando persiste una mejoría clínica evidente, las concentraciones séricas son inferiores a 1,4 mmol/L (19 mg/dL) o la TE ha sido aplicada durante al menos de 4 a 6 horas (en caso de que las concentraciones séricas no estén disponibles). La posibilidad de efecto rebote, ya sea por absorción o redistribución, se debe tener presente.
Se recomienda continuar con bicarbonato intravenoso entre las sesiones de TE, ello promueve la alcalosis (minimiza la entrada de salicilato en el sistema nervioso central) y alcalinización urinaria (reduce la reabsorción tubular renal y aumenta la excreción del fármaco con pH urinario de 7,5-8).
9. Teofilina (11).
La teofilina (1,3-dimetilxantina) es un compuesto de metilxantina, similar a la cafeína (1,3,7-trimetilxantina). Utilizada para el tratamiento del broncoespasmo, apnea neonatal, letargo y pérdida de peso.
Es un fármaco fácilmente dializable; Molécula pequeña (180 Da), con modesta unión a proteínas 40-60% (aún menor en lactantes y cirróticos), bajo volumen de distribución 0,5 L/kg y un bajo aclaramiento endógeno 40 a 60 ml/min.
Ya que no existe un antídoto específico, las terapias de apoyo son el pilar fundamental del tratamiento, entre ellas el DMCA.
Las TE se recomiendan en:
– Casos de intoxicación grave: convulsiones, arritmias mortales, inestabilidad hemodinámica, rabdomiólisis y alteraciones severas electrolíticas.
– Concentraciones superiores a 100mg/L (555 mmol/L). En menores de 6 meses o más de 60 años y exposición crónica, el límite es 50mg/L (278 mmol / L).
La HDI es la modalidad recomendada actualmente, dejando en segundo lugar a la HP y las TRRC. La exanguinotransfusión es una alternativa adecuada para neonatos.
Se debe continuar con tratamiento con DMCA a la vez que se aplican TE ya que mejora la eliminación del fármaco y previene la absorción de la fórmula de liberación continua.
La finalización de la TE se recomienda cuando las concentraciones plasmáticas son menores a 15 mg/L (83 mmol / L). Puede haber un efecto rebote en cuyo caso estaría indicado un nuevo ciclo de TE.
10. Talio (12).
Las sales de talio se usaban antiguamente como agentes medicinales (para la tiña) y raticidas. Actualmente, el talio se utiliza en la fabricación de lentes ópticas, termómetros de frío extremo e iluminación eléctrica.
Las investigaciones epidemiológicas estiman que la dosis oral potencialmente mortal es de 0,6 a 8 mg/kg. Las pequeñas cantidades utilizadas para el contraste radiactivo (10 mg) no representan una amenaza para la salud humana.
El talio es ligeramente dializable; pese a que no presenta unión a proteínas y tiene un bajo PM el factor limitante para ser eliminado mediante TE es su gran VD y una difusión intercompartimental lenta, con frecuente efecto rebote tras su depuración.
Aplicadas de manera precoz, tras la ingesta del fármaco, las TE parecen más eficaces que las vías endógenas para eliminar el talio pero, una vez completada la distribución a los tejidos, es poco probable que dichas técnicas sean efectivas.
Dado que el Talio es altamente tóxico y puede causar morbilidad grave y mortalidad con ingesta bajas (6mg/kg) y al no existir alternativas terapéuticas eficaces, sí se recomienda el uso de TE de manera precoz, antes de que se desarrolle un daño irreversible, cuando se sospeche mínima exposición al Talio o, suponiendo que las concentraciones de Talio estén disponibles; si es >1mg/L.
El grupo EXTRIP recomienda que durante la aplicación de TE también se deben aplicar medidas capaces de mejorar la eliminación del fármaco, como la administración de azul de prusia o DMCA.
Se recomienda de manera inicial HDI, la HP intermitente o hemofiltración (HF) son alternativas. Tras la sesión inicial, se aconseja técnicas continuas de mantenimiento para evitar efecto rebote.
En cuanto a la duración del tratamiento, se propuso un límite empírico de 72 horas pero, debido al efecto rebote y gran volumen de distribución del talio, algunos miembros del grupo de trabajo propusieron que se individualizara en función de historia clínica, síntomas, concentración de Talio (si está disponible en laboratorio) y complicaciones de la TE.
11. Ácido valproico (13).
La sobredosis por ácido valproico es un trastorno toxicológico común. La mayoría de los pacientes tienen un curso clínico benigno y una buena evolución.
Concentraciones séricas entre 50 y 100 mg / L (350 – 700 μ mol / L) se consideran terapéuticas. Con intoxicaciones leves, alrededor de 200mg/kg, se produce depresión del SNC pero ingestas superiores a 400mg/kg se asocia coma, depresión respiratoria, edema cerebral e inestabilidad hemodinámica.
Es moderamente dializable en caso de sobredosis: bajo PM (144 Da), pequeño VD (0,1-0,5 L/kg) y bajo aclaramiento endógeno. Pero tiene una alta unión a proteínas a dosis terapéuticas, hasta un 94%. Esta unión es saturable en casos de uremia y sobredosis, disminuyendo a un 15% y aumentando la fracción libre de fármaco.
La mayoría de los episodios de intoxicación aguda por ácido valproico se resuelven con medidas de apoyo y lavado gástrico con dosis única de carbón activo (dosis múltiples no se recomiendan).
Se propone la L-carnitina como antídoto, recomendándose en casos de intoxicación grave y encefalopatía hiperamonémica, aunque presenta poca evidencia clínica y su aplicación es limitada.
El grupo EXTRIP recomienda TE, especialmente HDI por su gran capacidad para corregir la acidosis y eliminar el amonio. La HP y TRRC serían alternativas válidas en caso de no disponer de HDI.
Las TE estarían indicadas cuando:
– Concentración sérica de ácido valproico 1300 m /L (9000 μmol/L).
– Edema cerebral o inestabilidad hemodinámica.
– Coma o depresión respiratoria que requiere ventilación.
– Hiperamonemia.
– pH ≤ 7,10.
Las TE deben continuarse hasta que la mejoría clínica sea evidente o hasta que la concentración sérica de ácido valproico se encuentre entre 50 y 100 mg/L (350 – 700 μmol/L).
12. Digoxina y Antidepresivos tricíclicos (ATC).
Para estos fármacos, los efectos adversos de la TE superan cualquier beneficio y, por lo tanto, las recomendaciones del grupo EXTRIP son no aplicar dichas terapias.
Sin embargo estudios recientes indican que el empleo de TE en intoxicaciones por fármacos ligeramente dializables, en los que no estarían indicadas como digoxina, ATC, metadona; son cada vez más utilizadas, no ya con la finalidad de eliminación de toxinas si no como soporte ante una insuficiencia orgánica.
La digoxina es ligeramente dializable (14). El factor limitante para aplicar TE es su gran VD (6.2 ± 2.6 L / kg), encontrándose grandes concentraciones de este fármaco en el corazón y riñón, siendo el músculo esquelético la mayor reserva corporal. El masivo efecto rebote que acontece tras TE es otro factor limitante. Dada la eficacia del tratamiento con fragmentos de anticuerpos antidigoxina (Fab), los cuales revierten los efectos tóxicos de los glucósidos cardiacos en menos de 4h en el 75% de los pacientes, las recomendaciones actuales son la no aplicación TE.
El tratamiento de los pacientes intoxicados con ATC incluye las medidas de soporte y tratar las convulsiones con benzodiazepinas. El bicarbonato de sodio combina el efecto de la carga de sodio y la alcalosis y sigue siendo la terapia de elección, especialmente para pacientes que presentan convulsiones, hipotensión que no responde a los líquidos o hallazgos típicos del ECG (arritmia ventricular, QRS> 100 ms, ondas R prominentes en aVR). Su dializabilidad es pobre: A pesar de tener un peso molecular pequeño (200-400 Da), su gran VD es un factor limitante a la hora de aplicar TE ya que, cualquier disminución de concentración plasmática tendrá un efecto insignificante en las reservar corporales totales, con el consiguiente efecto rebote (15).
Conclusiones
A pesar de que son numerosas las dificultades para realizar estudios con evidencia en el campo de las terapias extracorpóreas en intoxicaciones agudas; grupos de trabajo como EXTRIP continúan ampliando y desarrollando la literatura relevante al respecto y es probable que en los próximos años aumente el uso de estas técnicas, tanto para la eliminación de toxinas como para terapias de apoyo tras una intoxicación aguda.
Bibliografía
1. Ford, Delaney. Initial Approach to the Poisoned Patient. En: Ford´s ClinicaL Toxicology. Filadelfia, Saunders; 2001. p. 5-11. (HTML)
2. Jha VK, Padmaprakash KV. Extracorporeal Treatment in the Management of Acute Poisoning: What an Intensivist Should Know?. Indian J Crit Care Med. 2018 Dec;22(12):862-869. (PDF)
3. Gosselin S, Juurlink DN, Kielstein JT, Ghannoum M, Lavergne V, Nolin TD; EXTRIP workgroup. Extracorporeal treatment for acetaminophen poisoning: Recommendations from the EXTRIP workgroup. Clinical toxicology. 2014; 52(8):856-67. (PubMed)
4. Mactier R, Laliberte M, Mardini J, Ghannoum M, Lavergne V, Gosselin S, et al; EXTRIP Workgroup. Extracorporeal treatment for barbiturate poisoning: recommendations from the EXTRIP Workgroup .Am J Kidney Dis 2014; 64(3): 347-358. (HTML)
5. Ghannoum M,Yates C, Galvao TF, Sowinski KM, Vo TH, Coogan A, et al. EXTRIP workgroup. Extracorporeal treatment for carbamazepine poisoning: systematic review and recommendations from the EXTRIP workgroup. Clin Toxicol (Phila) 2014; 52(10): 993-1004. (PubMed)
6. Decker B, Goldfarb DS, Dargan PI, Friesen M, Gosselin S, Hoffman RS, et al; EXTRIP Workgroup. Extracorporeal Treatment for Lithium Poisoning: Systematic Review and Recommendations from the EXTRIP Workgroup. Clin J Am Soc Nephro 2015; 10(5):875-87. (PubMed)
7. Calello D, Liu KD, Wiegand TJ. Roberts DM, Lavergne V, Gosselin S, et al; EXTRIP Workgroup. Extracorporeal Treatment for Metformin Poisoning: Systematic Review and Recommendations From the Extracorporeal Treatments in Poisoning Workgroup. Crit Care Med. 2015; 43(8):1716-30. (HTML)
8. Roberts DM, Yates C, Megarbane B, Winchester JF, Maclaren R, Gosselin S, et al; EXTRIP workgroup. Recommendations for the Role of Extracorporeal Treatments in the Management of Acute Methanol Poisoning: A Systematic Review and Consensus Statement. Critical Care Medicine 2015; 43(2): 461-472. (HTML)
9. Anseeuw K, Mowry JB, Burdmann EA, Ghannoum M, Hoffman RS, Gosselin S, et al; EXTRIP Workgroup. Extracorporeal Treatment in Phenytoin Poisoning: Systematic Review and Recommendations from the EXTRIP (Extracorporeal Treatments in Poisoning) Workgroup. Am J Kidney Dis. 2016; 67(2):187-97. (PubMed)
10. Juurlink DN, Gosselin S, Kielstein JT, Ghannoum M, Lavergne V, Nolin TD, et al. EXTRIP Workgroup. Extracorporeal Treatment for Salicylate Poisoning: Systematic Review and Recommendations From the EXTRIP Workgroup. Ann Emerg Med. 2015; 266(2):165-81. (PubMed)
11. Ghannoum M, Wiegand TJ, Liu KD, Calello DP, Godin M, Lavergne V, et al; EXTRIP workgroup. Extracorporeal treatment for theophylline poisoning: Systematic review and recommendations from the EXTRIP workgroup. Clin Toxicol (Phila) 2015; 53(4): 215-229. (PubMed)
12. Ghannoum M, Nolin TD, Goldfarb DS, Roberts DM, Mactier R, Mowry JB, et al; EXTRIP Workgroup. Extracorporeal treatment for thallium poisoning: recommendations from the EXTRIP Workgroup. Clin J Am Soc Nephrol 2012; 7(10):1682-1690. (HTML)
13. Ghannoum M, Laliberté M, Nolin TD, MacTier R, Lavergne V, Hoffman RS, et al. EXTRIP Workgroup. Extracorporeal treatment for valproic acid poisoning: Systematic review and recommendations from the EXTRIP workgroup.Clin Toxicol (Phila) 2015; 53(5): 454-465. (HTML)
14. Mowry JB, Burmann EA, Anseeuw K, Ayoub P, Ghannoum M, Hoffman RS, et al; EXTRIP Workgroup. Extracorporeal treatment for digoxin poisoning: systematic review and recommendations from the EXTRIP Workgroup. Clin Toxicol (Phila) 2016; 54(2):103-14. (HTML)
15. Yates C, Galvao T, Sowinski KM, Mardini K, Botnaru T, Gosselin S, et al. EXTRIP workgroup. Extracorporeal treatment for tricyclic antidepressant poisoning: recommendations from the EXTRIP Workgroup.Seminars in dialysis. 2014; 27(4):381-9. (HTML)