Canales Lara PM (1), Vizuete Jiménez JM (2) Charco Roca LM (3), Villar Martínez C (3)
(1) Facultativo Especialista de Área de Anestesiología y Cuidados Intensivos. Hospital Universitario i Politécnico La Fe, Valencia.
(2) Jefe de Sección de Cuidados Críticos de Anestesiología. Complejo Hospitalario Universitario de Albacete.
(3) Facultativo Especialista de Área de Anestesiología y Cuidados Intensivos. Complejo Hospitalario Universitario de Albacete.
Cómo citar este artículo: Canales Lara, P. M., Jiménez Vizuete, J. M., Charco Roca, L. M., & Martínez Villar, C. (2022). Utilidad de los cartuchos de hemoperfusión en el shock séptico. Revista Electrónica AnestesiaR, 14(9). https://doi.org/10.30445/rear.v14i9.1041
Resumen
Introducción: El shock séptico es una de las entidades más frecuentes observadas en las Unidades de Cuidados Intensivos y está asociada a una elevada morbimortalidad. La sepsis se caracteriza por una desregulación del sistema inmune. En ella, se produce un desequilibrio entre sustancias proinflamatorias y sustancias antiinflamatorias. Los pacientes sépticos suelen tener una elevación en los niveles de endotoxinas y citoquinas. Niveles elevados de citoquinas en estos pacientes se han asociado a mayor mortalidad. La hemoperfusión o hemoadsorción es una técnica de depuración de la sangre cuyo objetivo es disminuir los niveles de citoquinas en plasma. Esta técnica se basa en poner en contacto la sangre del paciente con una membrana adsorbente mediante un circuito extracorpóreo (habitualmente asociado a una técnica continua de depuración extrarrenal aunque no es estrictamente necesario). Existen tres dispositivos en el mercado: el Cytosorb® (Palex), la polimixina B y el cartucho Oxiris® (Baxter).
Discusión: Con respecto al Cytosorb®, no hay evidencia que nos haga aconsejar su utilización de manera rutinaria en pacientes con shock séptico ya que no ha demostrado una reducción en la mortalidad. Respecto a la polimixina B, no existe suficiente evidencia disponible en la literatura para aconsejar el uso de estos cartuchos en pacientes con shock séptico de manera rutinaria. Por último, con el cartucho Oxiris® no hay estudios cuyo objetivo primario sea el análisis de mortalidad, por lo que no se puede aconsejar su uso de manera rutinaria.
Conclusiones: No existen evidencias concluyentes en las que basarse para aconsejar el uso de las terapias de hemoadsorción en pacientes en shock séptico. Únicamente hay una subpoblación de pacientes con shock séptico grave y con alta mortalidad (basado en las escalas de gravedad) en los que puede que este tipo de terapias muestren ciertos beneficios en cuestiones de reducción de parámetros inflamatorios, días libres de vasopresores y disminución de la mortalidad.
Introducción
El shock séptico es una de las entidades más frecuentes en las Unidades de Cuidados Intensivos (UCIs). La mortalidad de los pacientes con shock séptico es elevada y los pilares del tratamiento incluyen administración temprana de antibióticos, control del foco, resucitación hemodinámica con fluidoterapia intravenosa y vasopresores, y tratamiento de las disfunciones orgánicas asociadas. Las guías de la Surviving Sepsis Campaign realizan una recomendación débil a favor del uso del tratamiento renal sustitutivo, recomendando las terapias continuas de depuración extrarrenal (TCDER). Sin embargo, no realizan ninguna recomendación respecto al uso de técnicas de purificación de la sangre (1,2).
El fracaso renal agudo (FRA) puede ocurrir entre un 22 y 69% en pacientes sépticos y está asociado con resultados adversos a corto y largo plazo, y a un aumento de la mortalidad. Un 15-20% de estos pacientes pueden requerir TCDER (3).
Las TCDER están diseñadas para imitar la función depurativa del riñón de una manera lenta y continua. En el contexto de la sepsis o shock séptico están indicadas para eliminar sustancias tóxicas como la urea y para el manejo de balances hídricos cuando hay FRA asociado.
La sepsis se caracteriza por una desregulación de la respuesta inmune a las infecciones que resulta en una disfunción multiorgánica potencialmente mortal. La exagerada respuesta inmune que se produce en el sitio de la infección es multifactorial. Componentes celulares de la pared bacteriana (endotoxinas o lipopolisacáridos), conocidos como patrones moleculares asociados a patógenos (PAMPs por sus siglas en inglés) y patrones moleculares asociados al daño (DAMPs por sus siglas en inglés) son liberados por las células del huésped y juegan un papel importante en la respuesta inmune pro-inflamatoria y anti-inflamatoria de las citoquinas. Los lipopolisacáridos son por sí mismos una causa dosis dependiente de la elevación de citoquinas (4). Los pacientes con sepsis suelen tener elevados niveles de endotoxinas y citoquinas, como la interleucina 6 (IL-6), IL-8, IL-10 y el factor de necrosis tumoral alfa (TNFa) que se ha asociado a mayor mortalidad. Sabiendo que niveles elevados de estas citoquinas se asocian a mayor mortalidad, se han intentado diversos tratamientos para la reducción de las mismas en el torrente sanguíneo.
La hemofiltración de alto volumen (HFAV) desciende los niveles de citoquinas por un mecanismo no muy bien conocido. Se han postulado 4 hipótesis acerca de cómo desciende estos niveles. (5).
- La hipótesis del umbral de inmunomodulación que habla de que la HFAV disminuye los niveles plasmáticos de mediadores anti y proinflamatorios y que ello provoca una disminución de los niveles en el intersticio y en los tejidos hasta alcanzar un umbral que interrumpe el flujo de mediadores inflamatorios.
- La hipótesis de la entrega de mediadores, en la que se postula que la HFAV incrementa el flujo linfático, lo que provoca un paso de los mediadores del intersticio a la sangre que facilita su eliminación.
- La hipótesis de la reducción de la apoptosis, en la que la HFAV disminuye los niveles de caspasa III y caspasa VIII disminuyendo la apoptosis de monocitos, macrófagos y neutrófilos.
- La hipótesis del nivel celular-modelo citoquinético, que postula que la HFAV actúa restaurando la función inmune a través de la regulación de monocitos, neutrófilos y linfocitos.
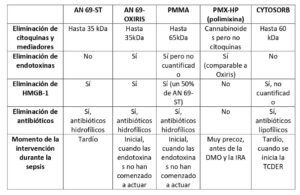
La hemoperfusión (o hemoadsorción) se basa en un concepto similar al previamente explicado. Implica el contacto de la sangre del paciente con una membrana adsorbente a través de un circuito extracorpóreo para reducir la cantidad de citoquinas presentes en el torrente sanguíneo. Estas membranas adsorbentes están formadas por materiales sintéticos en la actualidad y según las composiciones de estos materiales pueden adsorber sustancias de mayor o menor peso molecular, incluyendo endotoxinas y citoquinas (3,6). Los polímeros que forman estas membranas presentan poros de diferentes tamaños y cadenas laterales con las que se generan columnas adsorbentes capaces de extraer partículas de un determinado peso molecular de la circulación (Tabla 1) (2).
El objetivo de esta revisión bibliográfica es encontrar la evidencia publicada sobre el uso de las diferentes membranas adsorbentes, y si estas producen cambios en el pronóstico de los pacientes. Para ello, se ha realizado una búsqueda bibliográfica no sistemática en PubMed. Para ello, se han utilizado los términos «Continuous Renal Replacement Therapy/instrumentation«[Mesh] y “Continuous Renal Replacement Therapy AND «Shock, Septic«[Mesh]”.
Desarrollo
- Cytosorb®
El Cytosorb® es un dispositivo de hemoperfusión que utiliza la purificación extracorpórea para reducir los niveles séricos de citoquinas inflamatorias. Los cartuchos pueden ser utilizados de manera aislada o junto a TCDER, máquinas de bypass cardiopulmonar o membranas de oxigenación extracorpóreas (8).
Un metanálisis publicado en abril de 2019 por Ankawi et al. (9) revisa varios estudios con el objetivo principal de analizar la mortalidad o el descenso de las dosis de drogas vasoactivas asociado al uso de Cytosorb®.
Dado que se puede aplicar con cualquier técnica de circulación extracorpórea se analiza por una parte al paciente con shock séptico y TCDER, y por otra al paciente en bypass cardiopulmonar. Dos ensayos clínicos aleatorizados con objetivo principal el análisis de mortalidad, no demostraron disminución de la misma a 28 y 60 días. De hecho, observaron que los pacientes tratados con ytosorb® presentaban mayor mortalidad que los pacientes en el grupo control (siendo la diferencia de mortalidad a 60 días significativamente mayor). Sin embargo, hay que comentar que los pacientes tratados con ytosorb® tenían mayores puntuaciones en las escalas de gravedad y las poblaciones no eran totalmente comparables por ese motivo.
En otras dos series, con objetivo principal el análisis de la reducción de drogas vasoactivas, sí se observó una reducción en las dosis respecto al basal.
En los estudios en los que se analizaron los niveles de IL-6, sí que se observaron un descenso de los mismos (mayor en los pacientes tratados con Cytosorb que en grupo control).
Otro estudio analizó de manera retrospectiva pacientes con shock séptico tratados con ytosorb® y TCDER frente a los que sólo habían precisado TCDER. Se observó una mortalidad similar en ambos grupos de manera inicial, pero posteriormente se observó que el grupo tratado con Cytosorb® tenía un peor pronóstico inicial al presentar parámetros de mayor gravedad. Tras el análisis, concluyeron que, si ambas poblaciones hubieran sido comparables en cuestión de pronóstico, la población tratada con Cytosorb® hubiera tenido menor mortalidad (10).
El ensayo de Hawchar et al. analizó a 20 pacientes tratados con Cytosorb® de forma aislada sin TCDER, y demostró un descenso significativo de procalcitonina y endotelina-1 junto con una disminución de los requerimientos de vasopresores respecto al grupo control (11).
Con los resultados obtenidos, no hay evidencia que nos haga aconsejar la utilización de Cytosorb® de manera rutinaria en pacientes con shock séptico, al no haberse demostrado una disminución de la mortalidad, aunque sí parece demostrado el descenso de parámetros infecciosos y de dosis de drogas vasoactivas.
2. Polimixina B
La hemoperfusión directa mediante la polimixina B (una columna adsorbente de endotoxina) fue desarrollada en Japón para el tratamiento del shock séptico por gram-negativos. Ha sido comercializado como Toraymyxin®. Aunque la polimixina B se considera nefrotóxica, la Toraymyxin® se considera segura (8).
Respecto a la polimixina B hay dos metaanálisis publicados en 2017 y 2018. Analizando el metaanálisis de 2017 realizado por Tzu Chang en Taiwan (12) donde analiza 17 estudios (5 ensayos clínicos aleatorizados y 12 en los que hacen comparaciones con grupo control), se observa una reducción significativa de la mortalidad, pero sólo en aquellos pacientes más graves. En los pacientes con un mejor pronóstico (mortalidad prevista más baja), esta tendencia se invertía y presentaban mayor mortalidad con el uso de la polimixina B. La mayoría de estos estudios planteaban la mortalidad a 28 días como objetivo principal.
En el metaanálisis publicado por Tomoko Fuji et al. en 2018 (13) se analizan 6 ensayos clínicos aleatorizados con un total de 868 pacientes y uno de ellos, el ensayo EUPHRATES (14), con 450 pacientes. Los resultados del metaanálisis son concordantes a los observados de manera individual en el ensayo EUPHRATES. Se seleccionaron ensayos clínicos que presentaban dos ramas todos ellos, uno en las que los pacientes eran tratados con TCDER con Cytosorb® frente a sólo TCDER. En este metaanálisis se analizó la mortalidad a los 28 días, la aparición de efectos adversos fatales y la reducción de la puntuación en escalas de gravedad de shock séptico (SOFA o MODS). En cuestión de mortalidad, se observó un RR de 1,03 con un intervalo de confianza (0,78 – 1,36) con el uso de polimixina B. En cuestión de aparición de efectos adversos fatales el RR fue de 1,83 (0,63-5,32). Por último, en la reducción de la escala de gravedad, el RR fue de -0.26 (-0.64-0.12), apoyando el uso de polimixina B pero con un resultado no significativo.
Otros estudios posteriores han analizado el estudio EUPHRATES (15,16) con la población con mayor riesgo de mortalidad (mortalidad mayor al 60%). En ese subgrupo de población, el uso de polimixina B ha demostrado una reducción significativa de la mortalidad, una disminución en días de ventilación mecánica y una menor dosis de drogas vasoactivas.
Con los resultados obtenidos, no existe suficiente evidencia disponible en la literatura para aconsejar el uso de cartuchos de polimixina B en pacientes con shock séptico. Existiría la posibilidad de su uso en pacientes con una alta mortalidad en los que la evidencia actual indica que podría mejorar su pronóstico de mortalidad.
3. Oxiris®
Hay gran cantidad de cartuchos de perfusión investigándose en la actualidad, basados en membranas de polimetil-metacrilato (PMMA), membranas AN69 tratadas superficialmente (AN69-ST) y membrana AN69 modificadas (Oxiris®). Las membranas PMMA son membranas poliméricas, sintéticas e hidrofóbicas con una estructura con microporos y son las utilizadas en hemodiálisis en pacientes con insuficiencia renal crónica. Hay modificaciones de estas membranas PMMA que se están utilizando en la hemodiafiltración continua.
Las membranas AN69- ST están desarrolladas a partir de las AN69 (primera membrana polimérica desarrollada en 1969). Esta membrana está cargada negativamente para captar las moléculas positivas y es tratada posteriormente con una molécula cargada positivamente para captar las endotoxinas cargadas negativamente. Además, está cubierta por heparina para reducir eventos trombóticos y alargar la vida del filtro.
Pese a que estas sustancias llevan varios años en los mercados, su uso no está generalizado y hay pocas guías que establezcan recomendaciones al respecto.
Con respecto al cartucho Oxiris® aún no existen metaanálisis publicados.
Una serie corta de casos (4 pacientes) utilizó Oxiris® tanto en hemodiálisis como en hemodiafiltración veno-venosa continua de manera ininterrumpida entre 12 y 36 horas y objetivó una reducción de las cifras de lactato sérico, dosis de noradrenalina y descenso en la puntuación SOFA (17).
Otro estudio publicado en 2019 analiza 31 pacientes en dos hospitales de Francia (18). Se observa una supervivencia mayor de la esperada (aunque no significativa) respecto a lo inicialmente estimado por la escala SAPS II, una disminución significativa de las dosis de noradrenalina y niveles de lactato sérico, pero no la puntuación SOFA.
El grupo de trabajo de Turani et al. tenía como objetivo analizar el descenso de parámetros infecciosos y mejoría en parámetros hemodinámicos (19). Se incluyeron 60 pacientes que presentaron un descenso significativo de las dosis de noradrenalina y un aumento de la relación presión arterial de oxígeno (PaO2) respecto a fracción inspirada de oxígeno (FiO2). Además, observaron descensos significativos de urea, creatinina, lactato, puntuación en la escala SOFA y descenso en los niveles de diversas citoquinas (IL-6 o IL-10 entre otras).
El único ensayo clínico publicado hasta este momento ha sido realizado en 16 pacientes en Suecia (20). Se establecieron dos ramas en los que unos pacientes recibían inicialmente TCDER con el cartucho Oxiris® y otros no y posteriormente se les daba otro ciclo de TCDER con las terapias cambiadas. Los resultados muestran que en los pacientes que se trató en primer lugar con Oxiris®, los niveles de endotoxinas descendían de manera significativa respecto a los que se les aplicaba TCDER con un cartucho convencional. Además, se observó que los niveles de lactato y las dosis de noradrenalina descienden con el uso de esta membrana. Una grave limitación que presenta este trabajo es que no es un ensayo clínico aleatorizado y los pacientes con niveles más elevados de endotoxinas era a los que se les aplicaba en primer lugar la terapia con Oxiris®. Un resultado negativo con respecto a este es que los pacientes que posteriormente eran tratados con Oxiris® (primer periodo con TCDER convencional), no presentaban una reducción en los niveles de endotoxinas o una disminución en dosis de lactato o noradrenalina.
El cartucho de hemofiltración Oxiris® ha demostrado una reducción de endotoxinas y mejoría de los niveles de lactato y disminución de dosis de noradrenalina en pacientes en shock séptico, pero no hay estudios que hablen de mortalidad por lo que no se puede aconsejar su uso de manera rutinaria.
Conclusiones
No existen evidencias concluyentes para aconsejar el uso de las terapias de adsorción en pacientes en shock séptico.
Hay resultados discordantes en cuanto a mortalidad y no hay una evidencia a favor de su uso.
Únicamente hay una subpoblación de pacientes con shock séptico grave y con alta mortalidad (basado en las escalas de gravedad) en los que puede que este tipo de terapias muestren ciertos beneficios en cuestiones de reducción de parámetros inflamatorios, días libres de vasopresores y disminución de la mortalidad.
Bibliografía
1 Rhodes A, Evans LE, Alhazzani W, Levy MM, Antonelli M, Ferrer R, et al. Surviving Sepsis Campaign: International Guidelines for Management of Sepsis and Septic Shock: 2016. Crit Care Med. 2017 Mar;45(3):486-552. doi: 10.1097/CCM.0000000000002255. PubMed PMID: 28098591. (PubMed)
2 Karkar A, Ronco C. Prescription of CRRT: a pathway to optimize therapy. Ann Intensive Care. 2020 Mar 6;10(1):32. doi: 10.1186/s13613-020-0648-y. Review. PubMed PMID: 32144519; PubMed Central PMCID: PMC7060300. (PMC)
3 Honoré PM, De Bels D, Spapen HD. An update on membranes and cartridges for extracorporeal blood purification in sepsis and septic shock. Curr Opin Crit Care. 2018 Dec;24(6):463-468. doi: 10.1097/MCC.0000000000000542. Review. PubMed PMID: 30247215. (PMC)
4. Hawchar F, László I, Öveges N, Trásy D, Ondrik Z, Molnar Z. Extracorporeal cytokine adsorption in septic shock: A proof of concept randomized, controlled pilot study. J Crit Care. 2019 Feb;49:172-178. doi: 10.1016/j.jcrc.2018.11.003. Epub 2018 Nov 10. PubMed PMID: 30448517. (PubMed)
5. Jiménez Vizuete JM, Romero Mingo S, Girón Lacasa M. (2017). Terapias de reemplazo renal en la sepsis. ¿Algo más que sustitución renal?. Cuéllar Obispo E, Neira Reina F, Ortega García JL, Echevarría Moreno M. Actualizaciones en Anestesiología, Reanimación y Tratamiento del Dolor 2017. (pp. 175-196). Sevilla: Liberlibro.com.
6. Putzu A, Schorer R, Lopez-Delgado JC, Cassina T, Landoni G. Blood Purification and Mortality in Sepsis and Septic Shock: A Systematic Review and Meta-analysis of Randomized Trials. Anesthesiology. 2019 Sep;131(3):580-593. doi: 10.1097/ALN.0000000000002820. PubMed PMID: 31246600. (PubMed)
7. Clark WR, Gao D, Lorenzin A, Ronco C. Membranes and Sorbents. Contrib Nephrol. 2018;194:70-79. doi: 10.1159/000485603. Epub 2018 Mar 29. Review. PubMed PMID: 29597218. (HTML)
8. Bonavia A, Groff A, Karamchandani K, Singbartl K. Clinical Utility of Extracorporeal Cytokine Hemoadsorption Therapy: A Literature Review. Blood Purif. 2018;46(4):337-349. doi: 10.1159/000492379. Epub 2018 Sep 3. Review. PubMed PMID: 30176653. (HTML)
9. Ankawi G, Xie Y, Yang B, Xie Y, Xie P, Ronco C. What Have We Learned about the Use of Cytosorb Adsorption Columns?. Blood Purif. 2019;48(3):196-202. doi: 10.1159/000500013. Epub 2019 Apr 30. Review. PubMed PMID: 31039564. (PMC)
10. Brouwer WP, Duran S, Kuijper M, Ince C. Hemoadsorption with CytoSorb shows a decreased observed versus expected 28-day all-cause mortality in ICU patients with septic shock: a propensity-score-weighted retrospective study. Crit Care. 2019 Sep 18;23(1):317. doi: 10.1186/s13054-019-2588-1. PubMed PMID: 31533846; PubMed Central PMCID: PMC6749645. (PubMed)
11. Hawchar F, László I, Öveges N, Trásy D, Ondrik Z, Molnar Z. Extracorporeal cytokine adsorption in septic shock: A proof of concept randomized, controlled pilot study. J Crit Care. 2019 Feb;49:172-178. doi: 10.1016/j.jcrc.2018.11.003. Epub 2018 Nov 10. PubMed PMID: 30448517. (PubMed)
12 Chang T, Tu YK, Lee CT, Chao A, Huang CH, Wang MJ, et al. Effects of Polymyxin B Hemoperfusion on Mortality in Patients With Severe Sepsis and Septic Shock: A Systemic Review, Meta-Analysis Update, and Disease Severity Subgroup Meta-Analysis. Crit Care Med. 2017 Aug;45(8):e858-e864. doi: 10.1097/CCM.0000000000002362. PubMed PMID: 28445237; PubMed Central PMCID: PMC5515642.
13 Fujii T, Ganeko R, Kataoka Y, Furukawa TA, Featherstone R, Doi K, et al. Polymyxin B-immobilized hemoperfusion and mortality in critically ill adult patients with sepsis/septic shock: a systematic review with meta-analysis and trial sequential analysis. Intensive Care Med. 2018 Feb;44(2):167-178. doi: 10.1007/s00134-017-5004-9. Epub 2017 Dec 4. PubMed PMID: 29204670. (PubMed)
14 Dellinger RP, Bagshaw SM, Antonelli M, Foster DM, Klein DJ, Marshall JC, et al. Effect of Targeted Polymyxin B Hemoperfusion on 28-Day Mortality in Patients With Septic Shock and Elevated Endotoxin Level: The EUPHRATES Randomized Clinical Trial. JAMA. 2018 Oct 9;320(14):1455-1463. doi: 10.1001/jama.2018.14618. PubMed PMID: 30304428; PubMed Central PMCID: PMC6233793.
15 Rachoin JS, Foster D, Giese R, Weisberg LS, Klein DJ. Importance of Endotoxin Clearance in Endotoxemic Septic Shock: An Analysis From the Evaluating Use of PolymyxinB Hemoperfusion in a Randomized Controlled Trial of Adults Treated for Endotoxemic Septic Shock (EUPHRATES) Trial. Crit Care Explor. 2020 Feb;2(2):e0083. doi: 10.1097/CCE.0000000000000083. eCollection 2020 Feb. PubMed PMID: 32211615; PubMed Central PMCID: PMC7069594. Klein DJ, Foster D,
16 Klein DJ, Foster D, Walker PM, Bagshaw SM, Mekonnen H, Antonelli M. Polymyxin B hemoperfusion in endotoxemic septic shock patients without extreme endotoxemia: a post hoc analysis of the EUPHRATES trial. Intensive Care Med. 2018 Dec;44(12):2205-2212. doi: 10.1007/s00134-018-5463-7. Epub 2018 Nov 23. PubMed PMID: 30470853; PubMed Central PMCID: PMC6280819.
17. Zhang L, Yan Tang GK, Liu S, Cai J, Chan WM, Yang Y, et al. Hemofilter with Adsorptive Capacities: Case Report Series. Blood Purif. 2019;47 Suppl 3:1-6. doi: 10.1159/000499357. Epub 2019 Apr 12. PubMed PMID: 30982026.
18 Schwindenhammer V, Girardot T, Chaulier K, Grégoire A, Monard C, Huriaux L, et al. oXiris® Use in Septic Shock: Experience of Two French Centres. Blood Purif. 2019;47 Suppl 3:1-7. doi: 10.1159/000499510. Epub 2019 Apr 12. PubMed PMID: 30982028. (HTML)
19 Turani F, Barchetta R, Falco M, Busatti S, Weltert L. Continuous Renal Replacement Therapy with the Adsorbing Filter oXiris in Septic Patients: A Case Series. Blood Purif. 2019;47 Suppl 3:1-5. doi: 10.1159/000499589. Epub 2019 Apr 12. Review. PubMed PMID: 30982024. (PubMed)
20 Broman ME, Hansson F, Vincent JL, Bodelsson M. Endotoxin and cytokine reducing properties of the oXiris membrane in patients with septic shock: A randomized crossover double-blind study. PLoS One. 2019;14(8):e0220444. doi: 10.1371/journal.pone.0220444. eCollection 2019. PubMed PMID: 31369593; PubMed Central PMCID: PMC6675097. (PubMed)