Campos Rosas C (1), Martínez Lorenzo M (1), Ruiz Portillo L (1), Bernal Basurto R (2)
(1) Médico Interno Residente Servicio Anestesiología y Reanimación. Hospital Universitario Torrecárdenas, Almería.
(2) Facultativo Especialista de Área. Servicio Anestesiología y Reanimación. Hospital Universitario Torrecárdenas, Almería.
1. Aspectos generales de la esclerosis múltiple
1.1. Epidemiología
La esclerosis múltiple (EM) es una enfermedad inmunomediada del sistema nervioso central (SNC) que se caracteriza por una inflamación crónica que lleva a la aparición de placas de desmielinización y gliosis en el cerebro y en la médula espinal (1).
La prevalencia es de 2 a 150 casos por cada 10.000 habitantes (2), con una gran variabilidad entre países. La mayor incidencia la encontramos en el norte de Europa, sur de Canadá, norte de EEUU, este de Australia y Nueva Zelanda, siendo rara entre las personas de origen asiático y africano (3).
El número de personas afectadas en todo el mundo se estima en aproximadamente 2´8 millones (2), afectando en España a unas 50.000-55.000 según datos de la Sociedad Española de Neurología(4). La enfermedad es al menos el doble de frecuente en mujeres que en hombres (69% vs 31%) (2). Aunque puede debutar en cualquier momento de la vida, la edad promedio del diagnóstico en todo el mundo está en torno a los 32 años, lo que la convierte en la causa neurológica no traumática más común de discapacidad en los adultos jóvenes (4).
1.2. Etiología
Varias líneas de investigación apoyan la hipótesis de que la EM es una enfermedad autoinmune que ocurre en personas genéticamente susceptibles después de una exposición ambiental, posiblemente viral (5).
- Factores genéticos (1,2,6): la tasa de concordancia en gemelos monocigóticos es del 25-30% y del 2-3% en dicigóticos, lo que sugiere que existe predisposición genética. Entre los posibles genes implicados encontramos:
- Complejo mayor de histocompatibilidad (MHC): son los más estudiados, existiendo asociación con HLA-DR2 y HLA-DQ.
- Otros genes no MHC: se han identificado más de 100 loci de genes no MHC probablemente relacionados con la EM.
- Factores ambientales (2,3):
- Virus: estudios recientes han implicado al virus de Epstein-Barr en la etiología de la EM.
- Latitud: existe una mayor incidencia de la enfermedad cuanto más lejos del ecuador nos encontremos, probablemente relacionado con la baja exposición solar y el déficit de vitamina D.
1.3. Patogenia
La hipótesis etiológica más aceptada es que la EM es una enfermedad autoinmune mediada por linfocitos T reactivos frente a la proteína básica de la mielina o la proteína proteolipídica, lo que da lugar a la aparición de placas de desmielinización y pérdida axonal (1,7).
Estas células T autorreactivas activadas son capaces de atravesar la barrera hemato-encefálica, induciendo un proceso inflamatorio que produce daño en la estructura de la mielina y altera los canales de sodio y con ello una conducción nerviosa anormal. Además, en los últimos años se ha descrito la presencia en líquido cefalorraquídeo de estos pacientes de oligopéptidos endógenos con actividad bloqueadora de los canales de sodio, capaces de enlentecer aún más la conducción axonal (5,6).
La aparición de un bloqueo parcial en áreas desmielinizadas es responsable de los síntomas negativos de la enfermedad como la debilidad y la hipoestesia. Por el contrario, impulsos ectópicos generados en estas áreas originan los síntomas positivos de la EM como convulsiones, disestesias o espasticidad (5,6).
1.4. Historia natural
La EM se caracteriza por la aparición de síntomas neurológicos variables e impredecibles, con episodios de recaídas y remisiones a lo largo de su evolución (7).
Hablamos de brote ante el hallazgo de una disfunción neurológica que dura más de 24 horas y evoluciona en días o semanas con recuperación completa, parcial o nula. Para ser considerados dos brotes diferentes las manifestaciones deben aparecer al menos con 1 mes de separación (criterio de diseminación temporal) y afectar a dos partes distintas del SNC (criterio de diseminación espacial) (1,8).
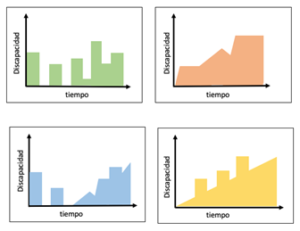
Según su historia natural podremos diferenciar cuatro patrones clínicos diferentes (1,7,8) (Fig 1):
- EM recurrente-remitente (RR): es la forma más común, incluyendo casi el 90% de los pacientes afectados. Consiste en la aparición de brotes recidivantes, separados por intervalos de tiempo durante los cuales puede haber una recuperación total o quedar algunos déficits residuales. Característicamente no existe progresión clínica entre episodios. (Fig A: Curso evolutivo de la forma RR).
- EM progresiva secundaria (SP): al principio suele debutar como una forma recurrente-remitente pero luego la incapacidad progresa. (Fig B: Curso evolutivo de la forma SP).
- EM progresiva primaria (PP): la enfermedad progresa gradualmente desde su debut. Afecta al 15% de pacientes, siendo más frecuente en los de inicio tardío. Tiene mal pronóstico. (Fig C: Curso evolutivo de la forma PP).
EM progresiva-recurrente (RP): desde el principio es progresiva, apareciendo además recaídas en forma de brotes. Fig. D: Curso evolutivo de la forma RP.
1.5. Clínica
Según las fibras nerviosas afectadas podremos encontrar (1,2,3,7,8):
- Alteraciones sensitivas: a nivel de las extremidades pueden aparecer hipoestesias, parestesias o prurito. Además es posible encontrar alteraciones de la sensibilidad facial o neuralgia del trigémino.
- Dolor: es un síntoma muy común. Son frecuentes el dolor ardiente continuo en las extremidades, la migraña, el dolor de espalda y los espasmos tónicos dolorosos. El signo de Lhermitte (sensación dolorosa transitoria de descarga eléctrica que se extiende por la columna vertebral y las extremidades provocada al flexionar el cuello) puede aparecer en el 40% de los pacientes y es característico de la EM.
- Fatiga: se ve a menudo durante un ataque agudo y característicamente puede preceder y persistir más allá del brote.
- Alteraciones motoras: paraparesia, paraplejia, hemiparesia y menos frecuentemente debilidad de extremidades superiores. También pueden presentarse espasticidad de los miembros, aumento de los reflejos tendinosos profundos y amiotrofia por desuso.
- Disfunción del tronco cerebral: disartria, diplopia, disfagia, hipoacusia o vértigo. En la exploración es típica la presencia de nistagmo horizontal, vertical y rotatorio y oftalmoplejía internuclear.
- Alteraciones visuales: típicas entre las manifestaciones clínicas iniciales. Suelen ser unilaterales e incluyen pérdida de visión parcial o total (escotoma central), visión borrosa o doble y/o dolor con los movimientos oculares. La mayoría de ellas son manifestaciones de una neuritis óptica. Durante el episodio agudo, el fondo de ojo puede ser normal (neuritis retrobulbar) o presentar edema de papila (papilitis). Además se puede apreciar una disminución del reflejo pupilar o bien el signo de Marcus-Gunn.
- Alteraciones cerebelosas: disartria, incoordinación motora, inestabilidad de la marcha, temblor intencional, dismetría o nistagmo.
- Alteraciones autonómicas: disfunción intestinal o vesical, alteraciones del control de esfínteres y/o disfunción sexual.
- Alteraciones cognitivas: afectación de la memoria reciente, atención y fluencia verbal. Aumento de la incidencia de epilepsia (afecta al 2-3% de los pacientes con EM).
- Trastornos afectivos: depresión (presente en el 19-54%), trastorno bipolar u otros síntomas psiquiátricos.
1.6. Diagnóstico
El diagnóstico de la EM es complejo, ya que no existe ninguna prueba patognomónica.
Actualmente se lleva a cabo a través de los Criterios de McDonald (2,6), revisados en 2017. Estos incluyen aspectos clínicos, pruebas de laboratorio y pruebas de imagen (siendo la más importante la RMN) y requieren demostrar que se han producido daños en el sistema nervioso central diseminados en espacio y tiempo.
2. Esclerosis múltiple y anestesia
En ocasiones las personas con EM tienen que someterse a una cirugía o algún tipo de procedimiento que requiere la administración de anestesia. En esos casos son muchas las dudas que pueden surgir a los pacientes y a los anestesiólogos en torno a su seguridad.
En general, podemos afirmar que tanto la anestesia como la cirugía no conlleva más riesgos en los pacientes con EM que los que tiene el resto de la población (2,9). Sin embargo, existen ciertos aspectos que deberemos tener en cuenta.
El manejo anestésico óptimo implica (3):
- Evaluación preoperatoria exhaustiva, prestando especial atención a la exploración neurológica del paciente y a su tratamiento farmacológico.
- Vigilancia intraoperatoria de las condiciones que pueden precipitar un brote.
- Atención postoperatoria a los riesgos respiratorios y de otro tipo.
2.1. Preoperatorio
La evaluación preoperatoria de los pacientes con EM debe incluir una revisión exhaustiva de la historia clínica del paciente y un examen clínico detallado.
- Consideraciones neurológicas:
Se debe realizar una evaluación completa del tipo de EM que presente nuestro paciente, así como reflejar en la preanestesia todas los déficits neurológicos que presente junto con su gravedad, especialmente en caso de preveer una anestesia locorregional (3).
- Consideraciones del tratamiento:
A día de hoy, la EM no tiene cura. Los medicamentos utilizados de forma paliativa y/o sintomática producen numerosas reacciones adversas, algunas de las cuales pueden complicar la práctica anestésica por lo que deben revisarse y tenerse en cuenta a la hora de planear nuestra actuación. Entre las más importantes destacamos (2,7,10):
- Aumento del riesgo de infecciones: se deben al uso de fármacos inmunomoduladores, siendo las más frecuentes las respiratorias. Además, se debe tener precaución con la aparición de fiebre alta en este contexto ya que puede provocar un empeoramiento agudo de los síntomas de la EM.
- Alteración de la eritropoyesis: en ocasiones podemos encontrar anemia en rango transfusional y/o trombocitopenia, lo que puede condicionar la técnica anestésica.
- Aumento del riesgo de insuficiencia hepática grave: se debería solicitar un perfil hepático para descartarla. En caso de que aparezca, deberemos priorizar el uso de fármacos con farmacocinética independiente de órganos como el cisatracurio o el remifentanilo ya que la capacidad de metabolización por parte del hígado estará disminuida,
- Hipotensión y bradicardia.
Actualmente no existe evidencia de que la suspensión del tratamiento de la EM previo a una cirugía reduzca el número de las complicaciones asociadas. Sin embargo, varios estudios e informes de casos sí que describen la recurrencia de la enfermedad días o meses después de suspender el tratamiento de la EM, especialmente en aquellos que presentaban una enfermedad activa en ese momento. Por este motivo, las intervenciones quirúrgicas electivas deberían realizarse durante una fase de remisión de la enfermedad y en caso de decidir interrumpir la medicación, esta debería reiniciarse lo antes posible.
- Consideraciones respiratorias:
En etapas avanzadas de la EM pueden existir alteraciones respiratorias debido a la aparición de lesiones a nivel de los centros superiores (2,7). Por este motivo, debe llevarse a cabo un examen respiratorio preoperatorio, que será más o menos exhaustivo en función de la gravedad de la enfermedad, la evaluación clínica inicial y el tipo de procedimiento quirúrgico que se prevea realizar.
- Historia clínica (2):
- Síndrome de apnea obstructiva del sueño (SAOS).
- Apnea central del sueño.
- Síndrome de Ondina.
- Otros: insomnio, trastornos del movimiento nocturno o la narcolepsia.
- Exploración física (7):
- Signos que indican debilidad de los músculos respiratorios: disminución de la capacidad para toser, para eliminar secreciones y para exhalar profundamente. Es la herramienta inicial más importante como predictor de debilidad de los músculos respiratorios y puede ser incluso superior a la espirometría.
- Predictores de vía aérea difícil.
- Signos y síntomas de aspiración crónica: especialmente si los músculos faríngeos y laríngeos están gravemente dañados.
- Pruebas de función pulmonar (2,3):
- Disminución de la capacidad inspiratoria y espiratoria máxima. El volumen pulmonar total y la capacidad vital pueden ser normales.
- Ligera caída de la capacidad vital forzada (CVF) y del volumen espiratorio forzado en el primer segundo (FEV1), con un índice de Tiffenau normal. Esto hace muy importante llevar a cabo una buena preoxigenación antes de la inducción anestésica.
- Disminución de la capacidad de difusión del monóxido de carbono (DLCO).
- Parálisis diafragmática: en casos de afectación de la médula cervical.
- Respuesta al aumento de la PaCO2 alterada: por alteración del centro de control de la ventilación.
- Otras recomendaciones (2):
- Se debe considerar el uso de presión positiva continua en las vías respiratorias (CPAP) o presión positiva binivel perioperatoriamente de forma preventiva para reducir los eventos hipóxicos.
- Algunos autores recomiendan determinar gases en sangre arterial antes de la intervención.
- Deberán evitarse las benzodiazepinas como ansiolíticos en estadíos avanzados de la enfermedad.
- Consideraciones cardiovasculares: (2,7)
- Inestabilidad hemodinámica: puede deberse a la existencia de disfunción autonómica (en caso de lesiones en la médula espinal torácica alta) y/o a efectos secundarios de algunos tratamientos de la EM.
- La hipotensión pronunciada puede ser difícil de tratar con la administración de volumen o vasopresores y puede ocurrir particularmente durante la inducción o la administración de la anestesia regional cerca de la médula espinal.
- Es característica la aparición de bradicardia en pacientes con Fingolimod, sobre todo al comienzo del tratamiento. Esta puede exacerbarse perioperatoriamente por el uso de otros fármacos bradicardizantes como los opioides.
- Si los pacientes con EM se quejan antes de la operación de síntomas como impotencia, síncope, arritmias cardiacas, disfunción urinaria o intestinal, esto debe tomarse como una señal de advertencia de la aparición de problemas hemodinámicos perioperatorios.
- Comorbilidad cardiovascular: la cardiopatía coronaria, la insuficiencia cardíaca crónica, el accidente cerebrovascular isquémico y la enfermedad arterial periférica son significativamente más frecuentes en la EM que en la población general debido a las mayores tasas de tabaquismo y obesidad.
2.2. Intraoperatorio
La EM no es una razón para evitar someterse a un procedimiento con anestesia. Sin embargo, debemos prestar atención a aquellos factores que pueden provocar una exacerbación de la enfermedad tras la intervención.
Generalmente se acepta que el estrés (2,7) puede causar una recaída en pacientes con EM. Situaciones como enfermedades subyacentes graves, infecciones, partos o la angustia emocional puede desencadenar un brote de la enfermedad. Por su parte, no hay evidencia de que la anestesia y/o la cirugía per se provoquen un deterioro agudo de la EM de forma independiente. Por este motivo, en los pacientes con EM (que no presenten compromiso respiratorio) está especialmente indicada la ansiolisis con midazolam.
Además, deberemos prestar especial atención a los aumentos de la temperatura corporal. La sensibilidad al calor, conocida como fenómeno de Uhthoff (2,11), es una característica de la EM y otros trastornos desmielinizantes y se define como un empeoramiento de los síntomas, estereotipado y reversible, secundario a la hipertermia. Entre los posibles factores desencadenantes podemos encontrar infecciones, inflamación, baños calientes, exposiciones ambientales, ejercicio fisico o menstruación. Esto provoca una disminución de la velocidad de conducción en los axones desmielinizados, capaz de exacerbar la clínica previa, que volverá a la normalidad una vez reestablecida su basal.
Para evitarlo se deben tomar una serie de medidas durante el perioperatorio:
- Monitorización continua de la temperatura corporal, incluso en procedimientos cortos.
- Tratamiento precoz en caso de hipertermia con antipiréticos o antibióticos (si se sospechan causas infecciosas).
- Modificación de la temperatura ambiente, uso de dispositivos de enfriamiento y administración de líquidos fríos.
- Precaución con el uso de almohadillas térmicas u otros dispositivos de calefacción.
Por último, debemos recordar que el postparto (5,10) supone también un factor de riesgo de recaída en la EM. Los estudios disponibles sugieren que ni modalidad de parto ni el tipo de anestesia obstétrica tienen ningún impacto en el curso de la EM en los 6 meses posteriores al mismo. Sólo la presencia de enfermedad activa durante el año previo al embarazo se ha presentado como factor de riesgo independiente asociado a la recaída postparto.
Anestesia general:
- Hipnóticos y analgésicos (2,3,7):
No existe evidencia de complicaciones con el uso de los siguientes fármacos.
- Anestésicos inhalados: sevofluorano, desfluorano y óxido nitroso.
- Propofol.
- Opioides: remifentanilo y fentanilo. Precaución en pacientes con sospecha de compromiso respiratorio.
- Midazolam: su efecto mínimo sobre el control de la termorregulación es una propiedad muy importante al usarlo como inductor anestésico en pacientes con EM.
- Dexmedetomidina.
- Relajantes musculares (2,7):
Los pacientes con EM suelen mostrar un aumento del número de receptores nicotínicos de acetilcolina en el músculo esquelético junto con un aumento del tiempo de apertura de sus canales. De forma general, estos cambios hacen necesario incrementar las dosis de bloqueante neuromuscular, aunque no se conoce exactamente cuánto.
- No despolarizantes: de elección. El rocuronio tiene ventajas sobre otros relajantes debido a la existencia del sugammadex como reversor.
- Succinilcolina: debe evitarse su uso por un aumento del riesgo de hiperpotasemia grave debido a los cambios en los receptores antes comentados. Esta puede producirse incluso en pacientes con valores de potasio previamente normales y el peligro aumenta en pacientes con brotes activos y conforme avanza la enfermedad.
Debido a esta respuesta impredecible, la monitorización del bloqueo neuromuscular mediante el test de tren de cuatro (TOF) se hace imprescindible en los casos en los que estos pacientes vayan a ser intervenidos con necesidad de relajación muscular. Preferentemente el TOF se colocará en una extremidad no afectada o en la menos afectada. De esta forma podremos titular cuidadosamente la cantidad de fármaco administrada con el objetivo de usar la menor dosis necesaria.
- Anestésicos locales IV (5):
Según algunos estudios, los anestésicos locales (AL) administrados sistémicamente pueden desenmascarar placas desmielinizadas silenciosas.
Esto se debe a que, como hemos mencionado previamente, los pacientes con EM presentan una disminución de la conducción nerviosa en segmentos desmielinizados. Al administrar los AL de forma intravenosa, estos actúan aumentando el grado de bloqueo ya existente previamente, por lo que se pueden agravar transitoriamente síntomas negativos de la enfermedad o incluso hacer aparecer déficits nuevos.
Anestesia neuroaxial:
El uso seguro de los AL cerca de la médula espinal en la EM ha sido objeto de debate Estos fármacos comparten propiedades fisiológicas con los oligopéptidos endógenos bloqueadores de los canales de sodio presentes en los pacientes con EM. Así, existía la preocupación teórica de que los AL pudieran desencadenar o aumentar los síntomas negativos de la EM al usarse para llevar a cabo bloqueos centrales o subaracnoideos igual que ocurre cuando se administran por vía intravenosa (5,7,14).
- Anestesia epidural:
La mayoría de los datos sobre anestesia epidural en la EM provienen de población obstétrica (10,14). Dado que estas pacientes tienen un mayor riesgo recaída en los primeros tres meses postparto, se podría pensar que los procedimientos anestésicos obstétricos podrían ser los responsables. Sin embargo, se ha demostrado que el embarazo debe considerarse un factor desencadenante independiente de las exacerbaciones y el uso de la anestesia epidural es seguro (8,12).
Para mayor seguridad, los AL deben usarse a la concentración más baja posible y si es posible sin añadir epinefrina (2).
- Anestesia subaracnoidea:
El acceso directo al SNC existente con esta técnica anestésica podría sugerir que esos riesgos teóricos descritos previamente podrían ser mayores. Sin embargo, numerosos estudios realizados en pacientes sometidos a intervenciones urológicas (13), plásticas (5) y cesáreas (8,12,14) no han mostraron problemas con su utilización y, a día de hoy, la anestesia raquídea se considera también un procedimiento seguro en los pacientes con EM.
Anestesia locorregional:
Al comienzo de este tema, hemos descrito a la EM como una enfermedad del SNC, por lo que, en principio, la administración de AL en los nervios periféricos no debería influir en su curso clínico. Sin embargo, en estudios postmortem se ha evidenciado la existencia de afectación nerviosa periférica sensitiva y motora, mostrando cambios en la excitabilidad axonal causada por una regulación positiva de los canales de potasio (2).
Debido a ello, existe preocupación por la posible existencia de un aumento de la neurotoxicidad de los AL sobre las neuronas desmielinizadas (3), aunque esto no ha podido ser demostrado.
Así, aunque es cierto que existen pocos datos, actualmente el uso de los bloqueos periféricos en los pacientes con EM se considera un procedimiento seguro (2). Se recomienda la realización de bloqueos ecoguaidos, con objetivo de reducir la cantidad de AL administrada y con ello la potencial toxicidad neuronal (13). Del mismo modo, si es posible, se debe evitar el uso de vasoconstrictores para no reducir la perfusión de los nervios (2).
Entre las ventajas de su uso encontramos la disminución del dolor postoperatorio, reduciendo así el estrés y así el riesgo de recaída (2).
2.3. Postoperatorio
Los pacientes con EM deben ser cuidadosamente monitorizados durante el postoperatorio inmediato prestando atención a (2,9,15)
- Temperatura corporal: vigilancia de la hipertermia y tratamiento precoz.
- Tensión arterial.
- Ventilación: los pacientes con afectación bulbar y respiratoria presentan mayor riesgo de compromiso de la vía aérea, hipoventilación y atelectasias. Además, el bloqueo neuromuscular residual puede afectar a estos pacientes, de forma más severa que a los pacientes con una función neurológica normal.
- Control neurológico: las recaídas pueden aparecer durante el período postoperatorio de forma precoz. Debe hacerse un examen neurológico frecuente para detectar la presencia de un nuevo brote y evaluar la necesidad de intervención.
3. Conclusiones
La EM es una enfermedad desmielinizante crónica del SNC que afecta principalmente a las mujeres en la tercera y cuarta décadas de la vida. Característicamente presenta un curso clínico variable, con recaídas y remisiones. Numerosos sistemas pueden verse afectados, lo que junto a sus tratamientos pueden afectar al manejo anestésico.
A pesar de las creencias de que la anestesia puede desencadenar un brote o empeorar el estado clínico de los pacientes con EM, una revisión exhaustiva de la literatura concluye que estos pacientes pueden ser intervenidos de manera segura.
Entre los aspectos más importantes destacamos la necesidad de llevar a cabo una evaluación preoperatoria minuciosa. Además, se deben conocer los mecanismos fisiopatológicos que puedan complicar el manejo perioperatorio de nuestros pacientes.
En cuanto a la anestesia general, los fármacos preferidos son el sevofluorano, desfluorano, óxido nitroso, propofol, remifentanilo, fentanilo y rocuronio. No se recomienda la succinilcolina como relajante muscular por el riesgo de hiperpotasemia. Además, se debe controlar el grado de relajación muscular mediante el TOF.
El uso de anestesia epidural y raquídea es seguro, recomendando la utilización de dosis bajas de AL sin vasoconstrictor.
Los bloqueos de nervios periféricos deben realizarse bajo control ecográfico.
Aunque los datos disponibles son limitados, estos sugieren que la tasa de recaída de la enfermedad en los periodos postoperatorio o postparto no se ve influenciada por la técnica anestésica empleada. Así, la elección debe basarse en un balance de los riesgos y beneficios específicos para cada paciente.
4. Bibliografía
1. Gómez-Porro P, Gómez-Mayordomo V, Ezcurra G, Aledo-Serrano A. Enfermedades desmielinizantes. En Manual AMIR Neurología y neurocirugía. 12ª Ed. Madrid; 2019. p. 74-78.
2. Drust A, Bartels C, Hachenberg T. Anesthesia and Multiple Sclerosis: What needs to be considered?. Anesthesiol Intensivmed Emergency Med Pain Therapy. 2016; 51:458-467. (PubMed)
3. Dorottaa IR, Schubertb A. Multiple sclerosis and anesthetic implications. Curr Opin Anesthesiol. 2002; 15:365-370. (PubMed)
4. Llaneza, MA. Situación de la esclerosis múltiple en España. Redacción médica [Internet]. 21 jul 2021 [Consultado 18 abr 2022]. Recuperado a partir de: https://www.redaccionmedica.com/secciones/neurologia/espana-diagnostica-cada-ano-2-000-nuevos-casos-de-esclerosis-multiple-1309
5. Perlas A, Chan VW. Neuraxial anesthesia and multiple sclerosis. Can J Anesth. 2005; 52(5):454–458. (PubMed)
6. Kasper DL, Fauci AS, Hauser SL, Longo DL, Jameson J, Loscalzo J. Esclerosis múltiple. En Harrison Manual de Medicina. 19ª Ed. McGraw Hill. LUIV4; 2017. p.
7. Makris A, Piperopoulos A, Karmaniolou I. Multiple sclerosis: basic knowledge and new insights in perioperative management. J Anesth. 2014; 28(2):267-78. (PubMed)
8. Harazim H, Štourač P, Janků P, Zelinková H, Frank K, Dufek M, et al. Obstetric anesthesia/analgesia does not affect disease course in multiple sclerosis: 10-year retrospective cohort study. Brain Behav. 2018;8(9):e01082 (PubMed)
9. De Lott LB, Zerafa S, Shedden K, Dunietz GL, Earley M, Segal BM, et al. Multiple sclerosis relapse risk in the postoperative period: Effects of invasive surgery and anesthesia. Mult Scler. 2020; 26(11):1437-1440. (PMC)
10. Varytė G, Zakarevičienė J, Ramašauskaitė D, Laužikienė D, Arlauskienė A. Pregnancy and Multiple Sclerosis: An Update on the Disease Modifying Treatment Strategy and a Review of Pregnancy’s Impact on Disease Activity. Medicina (Kaunas). 2020 Jan 21;56(2):49. (PubMed)
11. Gallego M, Anillo VE, Gómez V, García FJ. Fenómeno de Uhthoff en paciente con esclerosis multiple durante perioperatorio de cirugía de cadera. Reporte de un caso. Rev Colom Anestesiol. 2018;46(4):345-348.
12. Bouvet L, Fontana M, Bouthors AS, Bonnin M, Storme B, Bayoumeu F, et al. Post-partum relapse in women with multiple sclerosis after neuraxial labour analgesia or neuraxial anaesthesia: A multicentre retrospective cohort study. Anaesth Crit Care Pain Med. 2021;40(5):100834. (PubMed)
13. Martucci G. Should we feel free to use loco-regional anesthesia in multiple sclerosis?. Saudi J Anaesth. 2014;8(3):313-314. (PubMed)
14. Quispe Ricci AC. Manejo anestésico en cesárea de una gestante con esclerosis múltiple: reporte de un caso y revisión de la literatura. Rev Colomb Anestesiol. 2015;43(1):104–106. (HTML)
15. Del Castillo S, Jirón J, Sardi N, Cragwell M. Anestesia general con máscara laríngea en un paciente con esclerosis múltiple. Rev Esp Anestesiol Reanim. 2009; 56(3):198-199. (Medes)