Eugenio Martínez Hurtado 1
Sara Hervilla Ezquerra 2
Cómo citar este artículo: Hervilla Ezquerra, S., & Martínez Hurtado, E. (2011). Soporte Vital Básico en el paciente Pediátrico: Recomendaciones ILCOR 2010. Revista Electrónica AnestesiaR, 3(12), 2. https://doi.org/10.30445/rear.v3i12.486
A diferencia de los adultos, en los niños la parada cardíaca suele ser el resultado final de un fallo respiratorio progresivo o de un shock, por lo que se le denomina también fallo asfíctico 1.
Otro mecanismo de parada cardíaca lo constituyen, hasta en el 5““15% de los casos intra y extrahospitalarios, la Fibrilación Ventricular (FV) o la Taquicardia Ventricular rápida sin pulso (TV), llegando al 27% de los casos intrahospitalarios. La incidencia disminuye con la edad 2.
La evidencia sugiere que las muertes súbitas en los niños podrían asociarse a anomalías genéticas en los canales iónicos de las células musculares.
La supervivencia a una parada cardíaca infantil intrahospitalario en la década de los 80 era del 9%, en el año 2.000 estaba en torno al 17%, y en el 2.006 al 27% 15. Sin embargo, la supervivencia extrahospitalaria no se ha modificado sustancialmente, manteniéndose en torno al 6% (3% para lactantes y 9% para niños) 3.
El Soporte Vital Avanzado Pediátrico (SVAP) suele desarrollarse en un ambiente donde hay varios reanimadores que se activan rápidamente y desarrollan sus acciones simultáneamente y, donde lo más importante, es lograr que trabajen como un equipo eficaz.
Por tanto, una reanimación exitosa incluirá:
““ Un reanimador debe comenzar las compresiones torácicas inmediatamente, mientras otro comienza con la ventilación con Mascarilla Facial con reservorio (Clase I, LOE 3).
““ Las compresiones serán adecuadas en ritmo (al menos 100 compresiones por minutos) y profundidad (4 cm. en lactantes y 5 cm. en niños, aprox.), permitiendo la reexpansión completa del pecho, minimizando las interrupciones, evitando la ventilación excesiva y, si es posible, realizándola sobre una superficie dura.
““ Mientras un reanimador realiza las compresiones y otro ventila, el resto debe monitorizar al paciente y/o desfibrilar, lograr un acceso vascular y preparar la medicación que vaya a necesitarse. El acceso vascular puede ser una vía intravenosa periférica o central (IV) o Intraósea (IO).
Tras revisar el documento internacional de consenso 4 y las guías publicadas tanto por el European Resuscitation Council (ERC) 5 como por la American Heart Association (AHA) 6, continuamos revisando aquellos cambios más importantes o los“ toques de atención“ que el comité de expertos ha emitido respecto a las recomendaciones para la resucitación pediátrica y, tras ver el SVBP, abordamos el SVAP.
Las recomendaciones se clasifican en I, IIA, IIB, III e Indeterminada y el nivel de evidencia científica que las respalda desde LOE 1-5.
Manejo de la Vía Aérea
Tanto la AHA 2.010 como al ERC 2.010 recomiendan:
““ Mantener la vía aérea permeable es fundamental, y se acepta tanto el abordaje por vía orofaríngea como nasofaríngea. Se debe emplear la vía orofaríngea en niños inconscientes, en los que no haya reflejo nauseoso.
““ En cuanto a la ventilación, cuando no sea posible con Mascarilla Facial con reservorio y no se pueda llevar a cabo una intubación endotraqueal, se acepta emplear una Mascarilla Laríngea (ML) cuando el reanimador tenga experiencia en su uso (Clase IIa, LOE 3), teniendo en cuenta que su uso está asociado a una mayor incidencia de complicaciones en niños que en adultos.
““ Ya que no hay datos suficientes sobre la concentración de oxígeno inspirado óptimo, se recomienda ventilar con oxígeno al 100% durante la reanimación (Clase IIa, LOE 3). Una vez se haya restaurado la circulación, se debe monitorizar la saturación de oxihemoglobina arterial (SaO2) para regular la concentración de oxígeno, de tal manera que se mantenga igual o superior al 94% (Clase IIb, LOE 3). Hay que tener en consideración aquellas situaciones en las que el pulsioxímetro puede ser poco fiable, como pobre perfusión periférica, envenenamiento por monóxido de carbono, metahemoglobinemia, etc.
Debemos tener en cuenta además:
Empleo de tubos traqueales (TET) con balón versus tubos sin balón
Ambos tipos de TET pueden ser utilizados con seguridad en lactantes y niños pequeños (Clase IIa, LOE 3), y se debe comprobar y evitar presiones excesivas de inflado (se recomiendan presiones menores de 20 mmH2O).
En algunas circunstancias, como pobre complianza pulmonar, alta resistencia de la vía aérea o fuga a nivel dela glotis, tanto la AHA como el ERC recomiendan un TET con balón (Clase IIa, LOE 2).
En cuanto al tamaño del TET, debería ser seleccionado mediante la aplicación de una fórmula validada (aunque el ERC recuerda que puede hacerse en función de la longitud del cuerpo del niño 7).
Tanto para la AHA 2.010 como para el ERC 2.010 si usamos un TET sin balón en niños < 1 año puede usarse un tubo de 3,5 mm DI y de 4 mm DI entre 1 y 2 años. Por encima de los 2 años el tamaño del TET se estimará con la fórmula (años/4)+4.
Por otro lado, si usamos un TET con balón en niños < 1 año puede usarse un tubo de 3,0 mm DI. En niños de 1 a 2 años puede usarse un tubo de 3,5 mm DI (Clase IIa, LOE 2). Por encima de los 2 años puede calcularse el TET con balón mediante la fórmula (años/4)+3,5 (Clase IIa, LOE 2).
Tabla 1. Elección del tamaño del TET.
Presión cricoidea durante la intubación traqueal
No hay suficiente evidencia para recomendar el uso de la presión cricoidea como método para prevenir la aspiración durante la intubación traqueal en niños. Por tanto, la aplicación de presión sobre el cricoides se debe modificar o suspender si interfiere con la ventilación o si complica la intubación (Clase III, LOE 3).
Por otro lado, la AHA 2.010 recomienda aplicar la presión cricoidea en aquellas victimas que no respondan para reducir la entrada de aire al estómago durante la reanimación (Clase IIa, LOE 2). Esto podría requerir la presencia de un tercer reanimador si la presión cricoidea no la puede aplicar el mismo que está aplicando la mascarilla a la cara. En caso de aplicarla, hay que evitar que la presión sea excesiva y obstruya la tráquea (Clase III, LOE 2).
Secuencia de intubación rápida (SIR)
La AHA 2.010 recomienda que sólo aquellos reanimadores con entrenamiento, experiencia en el uso de medicación y competencia en el manejo de la vía aérea infantil, y a fin de facilitar la intubación de urgencia y reducir la incidencia de complicaciones, pueden usar sedantes, bloqueantes neuromusculares y otras medicaciones para realizar una SIR en el paciente pediátrico 8. En caso de que se use la SIR debe tenerse preparado un plan secundario para manejar la vía aérea en caso de no poder llevar a cabo la intubación.
La ERC 2.010, por otro lado, dice que en los niños en parada cardíaca o coma no se necesita sedación o analgesia para intubar. En los demás casos la intubación debe ir precedida de oxigenación, sedación rápida, analgesia y el empleo de bloqueantes neuromusculares para minimizar las complicaciones y/o fallos, y el reanimador que intube debe poseer la experiencia y estar familiarizado con las drogas empleadas en la SIR 9.
Monitorización de dióxido de carbono espirado (CO2), idealmente por capnografía
La monitorización de dióxido de carbono espirado (CO2), idealmente por capnografía, es útil para confirmar la posición correcta del tubo traqueal y recomendable durante la RCP para ayudar a evaluar y optimizar su calidad en cualquier situación (Clase I, LOE 3).
Limitación del oxígeno a los niveles normales tras la reanimación
Para la AHA 2.010, una vez restablecida la circulación, se debe monitorizar la SaO2. Cuando se disponga del equipo apropiado, puede ser razonable ajustar la administración de oxígeno para mantener la SaO2 a un valor igual o superior al 94%, con el fin de evitar la hiperoxia y garantizar una administración adecuada de oxígeno. Dado que una SaO2 del 100% puede equivaler a una PaO2 de entre 80 y 500 mm Hg aprox., por lo general es apropiado disminuir la FiO2 si la SaO2 llega al 100%, siempre que se pueda mantener la saturación a un valor igual o superior al 94% (Clase IIb, LOE 3).
El ERC 2.010 por su parte recomienda aplicar oxígeno a alta concentración (FiO2 del 100%) durante la fase inicial de la reanimación y, una vez restaurada la circulación, disminuir la FiO2 para mantener una SaO2 entre el 94““98%.
Ventilación y Oxigenación a través de Cateteres Transtraqueales
Se debe considerar esta posibilidad en pacientes con una obstrucción severa de la vía aérea por encima del cartílago cricoides si los métodos tradicionales no han tenido éxito y el reanimador tiene experiencia en su uso y el material adecuado. Dado que la ventilación transtraqueal resulta insuficiente para lavar eficazmente el CO2, debe considerarse como una técnica temporal mientras se asegura correctamente la vía aérea (Clase IIb, LOE 3).
Manejo Cardiocirculatorio
Debe monitorizarse inmediatamente al niño. El EKG diferenciará entre ritmos normales y anómalos, además de servir de ayuda para comprobar la respuesta a la medicación y los cambios clínicos.
El ecocardiograma no ha demostrado suficiente evidencia para ser empleado de forma rutinaria en la parada cardíaca infantil, pero en manos de personal entrenado puede ser de ayuda para identificar pacientes con causas de parada potencialmente tratable, en especial el taponamiento cardíaco o el llenado ventricular insuficiente (Clase IIb, LOE 3).
La monitorización de dióxido de carbono espirado (ETCO2) mediante capnografía continua o capnometría, si están disponibles, pueden ser de ayuda durante la reanimación, sobre todo para confirmar la efectividad de las compresiones torácicas (Clase IIa, LOE 3), como comentamos en el SVBP.
Fluídos, drogas y accesos vasculares
Tanto la AHA 2.010 como el ERC 2.010 coinciden en la importancia de obtener un acceso vascular para administrar medicación y tomar muestras de sangre. Dado que en niños el acceso venoso periférico (IV) puede ser dificultoso durante una urgencia,al cabo de 3 intentos o tras 1 minuto, se intentará el acceso intraóseo (IO), que suele lograrse con rapidez y mínimas complicaciones 9.
Acceso IO
El acceso IO es rápido, seguro y efectivo, y puede usarse como acceso vascular inicial en la parada cardíaca (Clase I, LOE 3). Pueden emplearse todas las medicaciones intravenosas sin peligro con la misma eficacia que un acceso venoso central, además de poder usarse para obtener muestras analíticas. Sin embargo, las gasometrías no serán fiables tras la administración de bicarbonato sódico 10.
Tras la administración de la medicación debe administrarse un bolo de Suero Salino 0,9% (SSF 0,9%) para lograr una distribución de la medicación a la circulación central más rápida.
Acceso Venoso
Como ya se ha comentado, los accesos venosos periféricos (IVP) son útiles pero complicados en niños, por lo que no se debe realizar más de 3 intentos.
Los accesos venosos centrales (IVC) son más seguros a largo plazo, pero requieren entrenamiento y experiencia, por lo que no se recomiendan como acceso inicial.
En caso de disponer de accesos periféricos y centrales, usaremos preferentemente el acceso central.
Medicación Intratraqueal
Si el acceso vascular no es posible, los medicamentos liposolubes (como la Lidocaína, Epinefrina, Atropina y Naloxona [LEAN]) pueden usarse por vía Intratraqueal a través del TET. Para ello se deben cesar las compresiones, se administrará la medicación diluida en 5 ml de SSF 0,9% y realizaran 5 ventilaciones.
Sin embargo, los efectos no serán iguales a los obtenidos por vía intravenosa. Además, las dosis óptimas intratraqueales son desconocidas a causa de la gran variabilidad de la absorción alveolar. Los expertos de la AHA recomiendan doblar o triplicar la dosis de lidocaína, atropina o naloxona cuando se administran a través del TET. La epinefrina se administrará a dosis 10 veces superiores a las intravenosas (0,1 mg/kg, o 0,1 ml/kg a una concentración de 1:1.000). (Tabla 2)
El ERC 2.010 recomienda:
““ Adrenalina: 100 mcg/kg.
““ Lidocaína: 2““3mg/kg.
““ Atropina: 30 mcg/kg.
““ No se conoce la dosis óptima de Naloxona.
No debe emplearse esta vía para administrar medicación no liposolube (p.ej. glucosa, bicarbonato sódico, calcio, etc.), puesto que pueden dañar la mucosa de la vía aérea.
Tabla 2.- Medicación usada en el SVAP (AHA 2.010 – ERC 2.010)
Calcio
Para la AHA 2010 no se recomienda administrar calcio de forma rutinaria para el paro cardiorrespiratorio pediátrico en ausencia de hipocalcemia, sobredosis de calcioantagonistas, hipermagnesemia o hiperkalemia documentadas.
Vasopresina ““ Terlipresina
Para la AHA 2.010 – ERC 2.010 no hay suficiente evidencia para recomendar de forma rutinaria su uso en la parada cardíaca.
Etomidato
Se ha visto que el Etomidato facilita la intubación endotraqueal en lactantes y niños con un efecto hemodinámico mínimo, pero no se recomienda su uso de forma rutinaria en pacientes pediátricos con evidencia de shock séptico puesto que se ha demostrado que aumenta las tasas de mortalidad en estos pacientes (Clase III, LOE 2). Además, provoca una supresión suprarrenal, y la respuesta esteroidea endógena puede ser de suma importancia en pacientes con un shock séptico.
Fluídos
Si la perfusión sistémica no es adecuada, y aunque la presión arterial sea normal, puede darse un bolo de 20 ml/kg de una solución isotónica cristaloide.
No hay suficientes datos para recomendar el uso del salino hipertónico en el shock asociado a heridas en la cabeza o por hipovolemia. Evitar soluciones con dextrosa a menos que haya hipoglucemia, que si se produce debe ser rápidamente solucionada.
Dosis de energía de desfibrilación
Ya se habló de los desfibriladores en el SVBP.
Actuación ante una parada cardíaca infantil
Comenzar y continuar con el SVBP.
Mientras se realiza la RCP, y sin detenerla, se comprobará el ritmo cardíaco mediante un EKG o, si se está usando un DEA, comprobar si el aparato nos indica que es un ritmo“ desfibrilable“ (p.ej. FV o TV rápida sin pulso) o “no desfibrilable“ (p.ej. Asistolia o actividad eléctrica sin pulso [DEM]).
A grandes rasgos AHA 2.010 y ERC 2.010 coinciden en sus algoritmos.
Si el ritmo es“ no desfibrilable“ mientras un reanimador continua las compresiones otro debe establecer un acceso vascular y administrar 0,01 mg/kg de epinefrina (0,1 ml/kg de una solución al 1:10.000), un máx. de 1 mg (10 ml) sin detener las compresiones. Se puede repetir la misma dosis de epinefrina cada 3 a 5 minutos (Clase I, LOE 2). No se ha demostrado que dosis superiores sean beneficiosas, y pueden resultar peligrosas, sobre todo en los cuadros asfícticos (Clase III, LOE 2).
ERC 2.010 ““ SVAP algoritmo ““ Ritmo no desfibrilable
Puede administrarse mayores dosis de epinefrina en casos particulares, como la sobredosis por B““bloqueantes.
Se continuará con la RCP y la administración de epinefrina hasta la recuperación del niño o el cese de los esfuerzos (ERC 2010 – Ritmo No desfibrilable).
AHA 2.010 – SVAP Algoritmo Parada Sin Pulso
Si en algún momento hay un ritmo «desfibrilable«, se realizará cardioversión inmediata y se continuarán las compresiones durante 2 minutos antes de comprobar de nuevo el ritmo (AHA 2010, Box 7).
A partir de la segunda cardioversión, y mientras se continua la RCP, se administrará Amiodarona (Clase IIb, LOE 3) o Lidocaína si no disponemos de Amiodarona (AHA 2010, Box 8).
ERC 2.010 – algoritmo SVAP
El ERC 2010 recomienda también cardioversión inmediata (4 J/kg) si el ritmo es desfibrilable y revisión a los 2 minutos. Si continúa el ritmo desfibrilable, realizar una segunda cardioversión (4 J/kg).
ERC 2.010 – SVAP algoritmo – Ritmo desfibrilable
Si transcurridos otros 2 minutos continúa el ritmo desfibrilable, realizar una tercera cardioversión (4 J/kg) y administrar Adrenalina 10 mcg/kg y Amiodarona 5 mg/kg en cuanto se reinicie la RCP.
Se continuará administrando Adrenalina cada 3““5 minutos si es preciso, y se administrará una segunda dosis de Amiodarona 5 mg/kg si tras 2 minutos de la tercera cardioversión persiste el ritmo desfibrilable.
Hay que identificar y tratar las causas reversibles (4 H y 4 T), teniendo presente que las 2 primeras H (Hipoxia e Hipovolemia) son las que mayor prevalencia tienen en los niños gravemente enfermos. Son: Hipoxia, Hipovolemia, Hiper/hipokalemia, Hipotermia, neumotórax a Tensión, Tóxicos, Taponamiento (coronario o pulmonar) y Trombosis (coronaria o pulmonar).
Torsade de Pointes
El AHA 2010 comenta que esta TV polimórfica asociada a QT alargado puede ser bien congénita o el resultado de la intoxicación por antiarrítmicos del tipo IA (p.ej. Procainamida, Quinidina, etc.) o del tipo III (p.ej. Sotalol y Amiodarona), por Antidepresivos Tricíclicos (ATC), digital o interacciones medicamentosas.
Dado que con frecuencia degenera en FV o TV sin pulso, se debe iniciar la RCP y desfibrilar cuando se produzca la parada cardíaca.
Dependiendo de la causa, se administrará en infusion rápida (minutos) de Sulfato Magnésico (25 a 50 mg/kg.; dosis máx. única de 2 g).
Actuación ante una Arritmia Inestable
Ante una arritmia en un niño el ERC 2.010 nos dice que lo primero es comprobar si hay signos vitales y pulso central. Si están ausentes se tratará como si fuera una parada cardíorrespiratoria. Si hay signos vitales y pulso central, se comprobará el estado hemodinámico. Si hay compromiso, los pasos a seguir serán:
““ Apertura de la vía aérea.
““ Oxigenar y, si es necesario, Ventilar.
““ Monitorizar con EKG o con un DEA y valorar el ritmo cardíaco (lento/rápido, regular/irregular y tamaño del QRS).
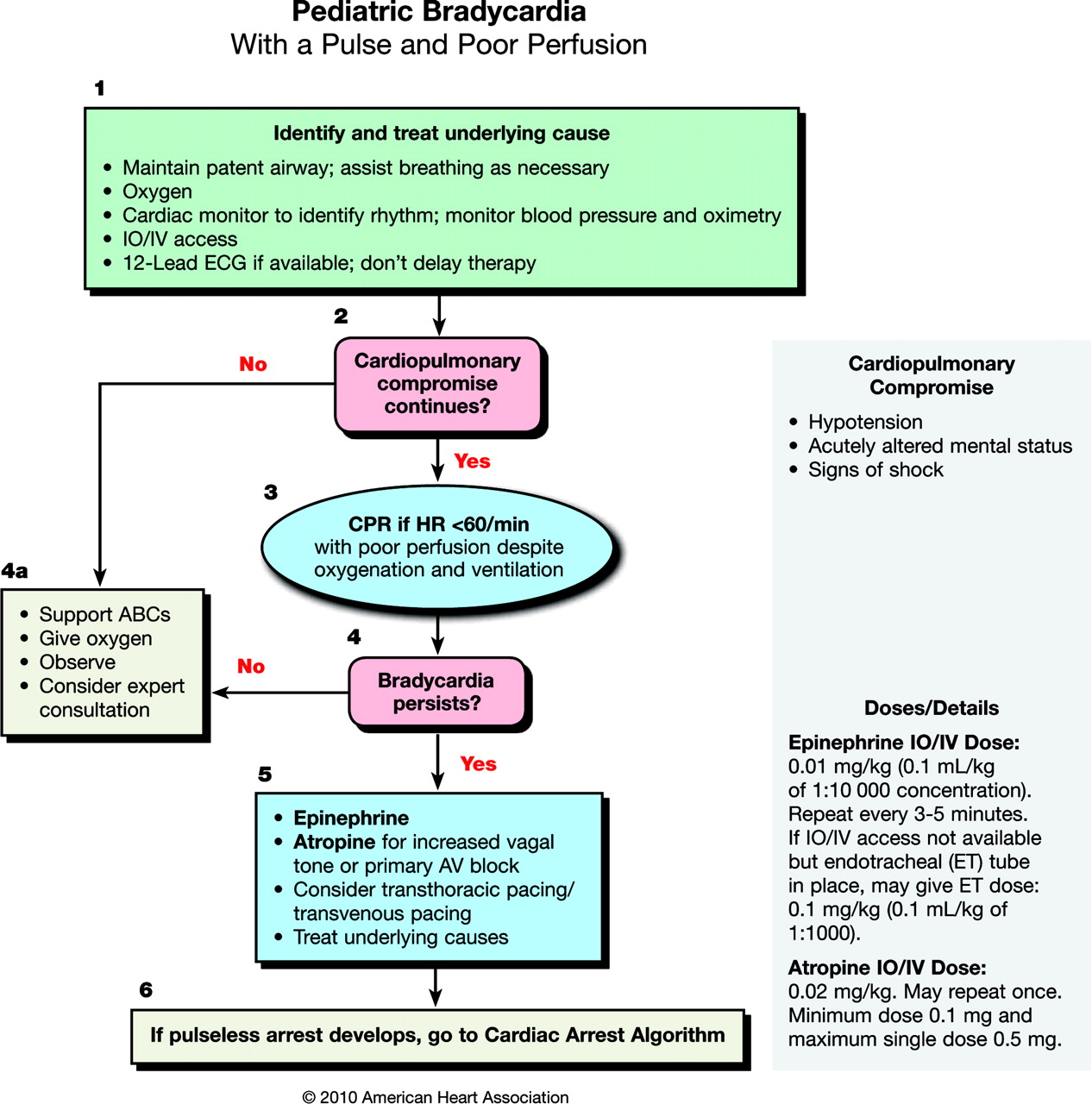
Bradicardia
En niños suele ser secundaria a hipoxia, acidosis y/o hipotensión severa, y puede acabar en parada cardiorrespiratoria. Por lo que si el niño no responde a la oxigenación/ventilación con presión positiva, se comenzará a aplicar compresiones torácicas y se administrará Adrenalina (Clase I, LOE 2). Si la causa de la bradicardia es vagal puede emplearse Atropina (Clase I, LOE 3) (ERC 2.010).
El algoritmo del AHA 2.010 es aplicable a niños con bradicardia y compromiso cardiorrespiratorio, pero con pulso palpable. En caso de que se pierda el pulso se establecerá una RCP de la parada cardíaca (AHA 2.010 ““ SVAP Algoritmo Parada Sin Pulso).
AHA 2.010 – SVAP Algoritmo Bradicardia
Taquicardia
Taquicardia de Complejo Estrecho (ERC <0,08 sg.; AHA <0,09 sg.)
El ERC 2010 recomienda que, en caso de que se trate de una Taquicardia Supraventricular (TSV) y el niño esté hemodinámicamente estable, pueden intentarse maniobras vagales (p.ej. valsalva) (Clase IIa, LOE 3). Si el niño está hemodinámicamente inestable con depresión del nivel de consciencia se realizará una cardioversión eléctrica sincronizada (podrían usarse las maniobras vagales, siempre que no retarden la cardioversión o la administración Adenosina).
La Adenosina suele ser efectiva en la reversión de la TSV a ritmo sinusal (0,1 mg/kg), pero debe inyectarse IV/IO rápida y seguida de un bolo de 5 ml de SSF 0,9% (Clase I, LOE 3).
La cardioversión también está indicada de entrada si no hay acceso vascular o si ya se ha empleado Adenosina sin éxito. La energía inicial para la cardioversión de la TSV es 0,5 a 1 J/kg; si se precisa una segunda cardioversión, se aplicará a 2 J/kg (Clase IIb, LOE 3). Si no revierte, y antes de aplicar una tercera cardioversión, puede administrarse Amiodarona (5 mg/kg IV/IO) o Procainamida (15 mg/kg) lentamente (Clase IIb, LOE 3).
El Verapamilo IV/IO puede ser una alternativa en niños mayores (0,1 a 0,3 mg/kg), pero no debe emplearse de forma habitual en niños pequeños por el riesgo de depresión miocárdica, hipotensión y parada cardíaca (Clase III, LOE 3).
AHA 2.010 – SVAP Algoritmo Taquicardia
Los algoritmos de la AHA 2.010 pueden emplearse en niños con Taquicardia pero con pulso palpable. En caso de no encontrar pulso lo trataremos como una parada cardiorrespiratoria.
Taquicardia de Complejo Estrecho (ERC >0,08 sg.; AHA >0,09 sg.)
En los niños este tipo de taquicardia es rara, y si aparece suele ser de origen supraventricular (TSV) antes que ventricular (TV). De todos modos, en un niño hemodinámicamente inestable, y mientras no se demuestre lo contrario, debe considerarse TV.
La TV ocurre normalmente en niños con enfermedades cardiacas subyacentes.El tratamiento de elección de la TV inestable con pulso es la cardioversión sincronizada (energía inicial de 0,5 a 1 J/kg; si falla, aumentar a 2 J/kg) (Clase IIb, LOE 3). En caso de que sea precisa una segunda cardioversión y resulte ineficaz, o exista recurrencia de la TV, podemos usar como antiarrítmico la Amiodarona.
En niños hemodinámicamente estables es recomendable consultar con un cardiólogo antes de iniciar cualquier tratamiento por el riesgo que conllevan todas las posibilidades terapéuticas.
Shock Séptico (AHA 2.010)
No se han encontrado diferencias significativas en la supervivencia tras tratamiento con coloides versus cristaloides. Por tanto, se recomienda comenzar el tratamiento de los niños en Shock Séptico con critaloides (Clase IIa, LOE 3).
La monitorización de la Saturación Central de Oxígeno Venosa en la vena cava superior (ScvO2), buscando un ScvO2 del 70%, parece haber demostrado aumentar la supervivencia en niños en shock séptico grave (Clase IIb, LOE 2). Para ello se recomienda la ventilación mecánica temprana (Clase IIb, LOE 3).
Shock Hipovolemico (AHA 2.010)
Se recomienda usar una solución cristaloide como fluidoterapia inicial (Ringer Lactato o SSF 0,9%) (Clase I, LOE 1), sin que se hayan demostrado beneficios en el uso de coloides en las fases iniciales de la reanimación.
Los signos de shock deben tratarse con un bolo de 20 ml/kg de SSF 0,9% independientemente de las cifras de presión arterial (Clase IIb, LOE 3).
Los cristaloides parecen tener un efecto beneficioso durante las cirugías traumatológicas, de lesiones cerebrales y en quemados.
No hay suficiente evidencia científica para recomendar un volumen o ritmo de infusión en lactantes y niños en shock hemorrágico secundario a un traumatismo ni para recomendar o rechazar el uso de una solución salina hipertónica en el shock asociado a lesión craneal o hipovolemia.
Circunstancias Especiales
Trauma
No hay que hiperventilar al niño, incluso en casos de traumatismos craneales (Clase III, LOE 3). Las técnicas de hiperventilación pueden emplearse como forma de rescate temporal en caso de que encontremos signos de herniación encefálica inminente (p.ej. aumento súbito de la presión Intracraneal [PIC], midriasis uni o bilateral, con pupila arreactiva a la luz, bradicardia, hipertensión, etc.).
Si existe un trauma maxilofacial y se sospecha una fractura de la base del cráneo son preferibles las sondas orotraqueales antes que las nasogástricas (Clase IIa, LOE 4).
En caso de parada cardiorrespiratoria en un niño con una traumatismo penetrante puede considerarse la realización de una toracotomía para realizar la RCP (Clase IIb, LOE 3).
Ventrículo único post primera fase de reparación
La supervivencia a una parada cardiaca en niños con ventrículo único tras una primera fase de reparación es del 20% aprox., subiendo hasta el 33% al alta, sin que haya evidencias de que esta supervivencia mejore cambiando los protocolos de RCP 11.
El diagnóstico de parada cardíaca es difícil en estos niños, pero puede mejorar con la monitorización de la extracción de oxígeno (mediante SCvO2 o NIRS 12)
Circulación post-Fontan
Durante la parada cardiaca en niños en los que falle la circulación post-Fontan puede emplearse la oxigenación a través de membrana extracorpórea (ECMO) (Clase IIa, LOE 3), aunque no se pueden hacer recomendaciones a favor ni en contra en aquellos niños con fisiología hemi““Fontan 13.
Hipertensión Pulmonar (HTPu)
Se llevarán a cabo los protocolos habituales de SVBP/SVAP, incluyendo oxigenación y ventilación en aquellos niños con HTP en parada cardiorrespiratoria, prestando especial atención a corregir la hipercarbia y mantener la precarga mediante bolos de SSF 0,9%.
Debe reinstaurarse la medicación HTP tan pronto como se pueda (Clase IIa, LOE 3). Valorar la administración de protóxido inhalado (NO) o prostaciclina o análogos en aerosol para disminuir la resistencia vascular pulmonar (Clase IIa, LOE 3); en caso de no poder, valorar la administración intravenosa de bolos de prostaciclina (Clase IIa, LOE 3). La ECMO puede resultar beneficiosa si se instaura precozmente (Clase IIa, LOE 3).
Bibliografía
1.- Young KD, Seidel JS. Pediatric cardiopulmonary resuscitation: a collective review. Ann Emerg Med. 1999;33:195““205. (PubMed)
2.- Appleton GO, Cummins RO, Larson MP, Graves JR. CPR and the single rescuer: at what age should you“ call first“ rather than“ call fast“? Ann Emerg Med. 1995 Apr;25(4):492-4. (PubMed)
3.- Atkins DL, Everson-Stewart S, Sears GK, Daya M, Osmond MH, Warden CR, Berg RA. Epidemiology and outcomes from out-of-hospital cardiac arrest in children: the Resuscitation Outcomes Consortium Epistry-Cardiac Arrest. Circulation. 2009 Mar 24;119(11):1484-91. Epub 2009 Mar 9. (PubMed) (pdf) (pdf)
4.- Nolan JP et al. 2010 International Consensus on Cardiopulmonary Resuscitation and Emergency Cardiovascular Care Science With Treatment Recommendations. Resuscitation 2010;81S:e1-e25. (PubMed)
5.- Biarent D, Bingham R, Eich C, López-Herce J, Maconochie I, Rodríguez-Núñez A, Rajka T, Zideman D. European Resuscitation Council Guidelines for Resuscitation 2010 Section 6. Paediatric life support. Resuscitation. 2010 Oct;81(10):1364-88. (PubMed) (pdf completo) (pdf Section 6).
6.- Kleinman ME, Chameides L, Schexnayder SM, Samson RA, Hazinski MF, Atkins DL, Berg MD, de Caen AR, Fink EL, Freid EB, Hickey RW, Marino BS, Nadkarni VM, Proctor LT, Qureshi FA, Sartorelli K, Topjian A, van der Jagt EW, Zaritsky AL. Part 14: Pediatric Advanced Life Support: 2010 American Heart Association Guidelines for Cardiopulmonary Resuscitation and Emergency Cardiovascular. Circulation. 2010 Nov 2;122(18 Suppl 3):S876-908. (PubMed) (pdf)
7.- Luten RC, Wears RL, Broselow J, Zaritsky A, Barnett TM, Lee T, Bailey A, Vally R, Brown R, Rosenthal B. Length-based endotracheal tube and emergency equipment in pediatrics. Ann Emerg Med. 1992 Aug;21(8):900-4. (PubMed)
8.- Sagarin MJ, Chiang V, Sakles JC, Barton ED, Wolfe RE, Vissers RJ, Walls RM. Rapid sequence intubation for pediatric emergency airway management. Pediatr Emerg Care. 2002;18:417““423. (PubMed)
9.- Carrillo A, López-Herce J. Canalización intraósea. An Pediatr Contin 2003;1(1):38-41. (pdf)
10.- Melé Olivé J , Nogué Bou R. La vía intraósea en situaciones de emergencia: Revisión bibliográfica. emergencias 2006;18:344-353. (pdf)
11.- Cincinnati Children’s Hospital Medical Center. Single Ventricle Anomalies and Fontan Circulation. (html) (video)
12.- Ranucci M, Isgrí² G, De la Torre T, Romitti F, Conti D, Carlucci C. Near-infrared spectroscopy correlates with continuous superior vena cava oxygen saturation in pediatric cardiac surgery patients. Paediatr Anaesth. 2008 Dec;18(12):1163-9. (PubMed)
13.- Cripes. The Frank Murphy Memorial Lecture 2008 – Fontan Physiology.Dept Of Anesthesiology & Critical Care, University Of Pennsylvania School Of Medicine, 19AGO2008. (html)
… para entender mejor los niveles de evidencia y grados de recomendación (pdf)
1 Eugenio Martínez Hurtado Médico Residente 2 Sara Hervilla Ezquerra Médico Adjunto Servicio de Anestesiología y Reanimación Hospital Universitario Fundación Alcorcón (Madrid)En algunas circunstancias, como pobre complianza pulmonar, alta resistencia de la vía aérea o fuga a nivel dela glotis, tanto la AHA como el ERC recomiendan un TET con balón (Clase IIa, LOE 2).
En cuanto al tamaño del TET, debería ser seleccionado mediante la aplicación de una fórmula validada. En aquellos niños que pesen más de 35 kg la elección del TET en función de la altura es más adecuada que mediante fórmulas, incluso en niños de corta estatura. Independientemente del tipo de TET que se vaya a usar, hay que tener preparados tubos con un DI 0,5 mm superior e inferior al estimado.
Durante la intubación, si el TET encuentra resistencia hay que usar el siguiente más pequeño. Por el contrario, si la fuga de aire a través de la glotis es tan importante que interfiere en la oxigenación o en la ventilación, hay que considerar cambiar el TET por el siguiente más grande o, si se usó un TET sin balón, cambiarlo por uno con balón del mismo número.
Para la AHA 2010, si usamos un TET sin balón en niños < 1 año puede usarse un tubo de 3,5 mm DI y de 4 mm DI entre 1 y 2 años. Por encima de los 2 años el tamaño del TET se estimará con la fórmula (años/4)+4.
Por otro lado, si usamos un TET con balón en niños < 1 año puede usarse un tubo de 3,0 mm DI. En niños de 1 a 2 años puede usarse un tubo de 3,5 mm DI (Clase IIa, LOE 2). Por encima de los 2 años puede calcularse el TET con balón mediante la fórmula (años/4)+3,5 (Clase IIa, LOE 2). Si al introducirlo se encuentra resistencia deberá usarse un tubo con un DI 0,5 mm menor. Y, si no hay fuga con el balón desinchado, puede ser beneficioso reintubar con un TET sin balón de un DI 0,5 mm menor cuando el niño esté estable.
EL ERC 2010, por su parte, recomienda que para niños menores de 1 año se empleen tubos sin balón de 3,5 a 4 mm DI o con balón de 3 a 3,5 mm DI, para niños de 1 a 2 años sin balón de 4 a 4,5 mm DI o con balón de 3,5 a 4 mm DI, y para mayores de 2 años se empleen según la fórmula: sin balón (años/4)+4, o con balón (años/4)+3,5. Sin embargo, indican que la elección del TET en función de la longitud del cuerpo del niño es más adecuada que el empleo de una fórmula (http://www.ncbi.nlm.nih.gov/pubmed/1497153).
Presión cricoidea durante la intubación traqueal
No hay suficiente evidencia para recomendar el uso de la presión cricoidea como método para prevenir la aspiración durante la intubación traqueal en niños. Por tanto, la aplicación de presión sobre el cricoides se debe modificar o suspender si interfiere con la ventilación o si complica la intubación (Clase III, LOE 3).
Por otro lado, la AHA 2010 recomienda aplicar la presión cricoidea en aquellas victimas que no respondan para reducir la entrada de aire al estómago durante la reanimación (Clase IIa, LOE 2). Esto podría requerir la presencia de un tercer reanimador si la presión cricoidea no la puede aplicar el mismo que está aplicando la mascarilla a la cara. En caso de aplicarla, hay que evitar que la presión sea excesiva y obstruya la traquea (Clase III, LOE 2).
Secuencia de intubación rápida (SIR)
La AHA recomienda que sólo aquellos reanimadores con entrenamiento, experiencia en el uso de medicación y competencia en el manejo de la vía aérea infantil, y a fin de facilitar la intubación de urgencia y reducir la incidencia de complicaciones, pueden usar sedantes, bloqueantes neuromusculares y otras medicaciones para realizar una SIR en el paciente pediátrico (Sagarin MJ, Chiang V, Sakles JC, Barton ED, Wolfe RE, Vissers RJ, Walls RM. Rapid sequence intubation for pediatric emergency airway management. Pediatr Emerg Care. 2002;18:417““423). En caso de que se use la SIR debe tenerse preparado un plan secundario para manejar la vía aérea en caso de no poder llevar a cabo la intubación.
La ERC, por otro lado, dice que en los niños en parada cardíaca o coma no se necesita sedación o analgesia para intubar. En los demás casos la intubación debe ir precedida de oxigenación, sedación rápida, analgesia y el empleo de bloqueantes neuromusculares para minimizar las complicaciones y/o fallos, y el reanimador que intube debe poseer la experiencia y estar familiarizado con las drogas que se emplean en la SIR (Sagarin MJ, Chiang V, Sakles JC, Barton ED, Wolfe RE, Vissers RJ, Walls RM. Rapid sequence intubation for pediatric emergency airway management. Pediatr Emerg Care. 2002;18:417““423).
Monitorización de dióxido de carbono espirado (CO2), idealmente por capnografía
La monitorización de dióxido de carbono espirado (CO2), idealmente por capnografía, es útil para confirmar la posición correcta del tubo traqueal y recomendable durante la RCP para ayudar a evaluar y optimizar su calidad en cualquier situación (Clase I, LOE 3), incluido el transporte (Clase IIb, LOE 3). Durante la parada cardíaca, si no se detecta CO2 espirado debe confirmarse la posición del TET con una laringoscopia directa (Clase IIa, LOE 3).
Sin embargo, no hay ninguna técnica que por si sola asegure al 100% la correcta colocación del TET (Clase I, LOE 2).
Limitación del oxígeno a los niveles normales tras la reanimación
Para la AHA 2010, una vez restablecida la circulación, se debe monitorizar la SaO2. Cuando se disponga del equipo apropiado, puede ser razonable ajustar la administración de oxígeno para mantener la SaO2 a un valor igual o superior al 94%, con el fin de evitar la hiperoxia y garantizar una administración adecuada de oxígeno. Dado que una SaO2 del 100% puede equivaler a una PaO2 de entre 80 y 500 mm Hg aprox., por lo general es apropiado disminuir la FiO2 si la SaO2 llega al 100%, siempre que se pueda mantener la saturación a un valor igual o superior al 94% (Clase IIb, LOE 3).
El ERC 2010 por su parte recomienda aplicar oxígeno a alta concentración (FiO2 del 100%) durante la fase inicial de la reanimación y, una vez restaurada la circulación, disminuir la FiO2 para mantener una SaO2 entre el 94““98%.
Ventilación y Oxigenación a través de Cateteres Transtraqueales
Se debe considerar esta posibilidad en pacientes con una obstrucción severa de la vía aérea por encima del cartílago cricoides si los métodos tradicionales no han tenido éxito y el reanimador tiene experiencia en su uso y el material adecuado. Dado que la ventilación transtraqueal resulta insuficiente para lavar eficazmente el CO2, debe considerarse como una técnica temporal mientras se asegura correctamente la vía aérea (Clase IIb, LOE 3).
Manejo Cardiocirculatorio
Debe monitorizarse inmediatamente al niño. El EKG diferenciará entre ritmos normales y anómalos, además de servir de ayuda para comprobar la respuesta a la medicación y los cambios clínicos.
El ecocardiograma no ha demostrado suficiente evidencia para ser empleado de forma rutinaria en la parada cardíaca infantil, pero en manos de personal entrenado puede ser de ayuda para identificar pacientes con causas de parada potencialmente tratable, en especial el taponamiento cardíaco o el llenado ventricular insuficiente (Clase IIb, LOE 3).
La monitorización de dióxido de carbono espirado (ETCO2) mediante capnografía continua o capnometría, si están disponibles, pueden ser de ayuda durante la reanimación, sobre todo para confirmar la efectividad de las compresiones torácicas (Clase IIa, LOE 3), como comentamos en el SVBP.
Fluídos, drogas y accesos vasculares
Tanto la AHA 2010 como el ERC 2010 coinciden en la importancia de obtener un acceso vascular para administrar medicación y tomar muestras de sangre. Dado que en niños el acceso venoso periférico (IV) puede ser dificultoso durante una urgencia, por lo que debe evitarse el perder tiempo para canalizar un acceso IV (el ERC 2010 considera un máximo de 1 minuto). En ese caso, se intentará el acceso intraóseo (IO), que suele lograrse con rapidez y mínimas complicaciones (http://www.apcontinuada.com/contenidos/pdf/v1n1a8pdf001.pdf).
Acceso IO
El acceso IO es rápido, seguro y efectivo, y puede usarse como acceso vascular inicial en la parada cardíaca (Clase I, LOE 3). Pueden emplearse todas las medicaciones intravenosas sin peligro con la misma eficacia que un acceso venoso central, además de poder usarse para obtener muestras analíticas. Sin embargo, las gasometrías no serán fiables tras la administración de bicarbonato sódico (http://www.semes.org/revista/vol18_6/4.pdf).
Tras la administración de la medicación debe administrarse un bolo de Suero Salino 0,9% para lograr una distribución de la medicación a la circulación central más rápida.
Acceso Venoso
Como ya se ha comentado, los accesos venosos periféricos (IVP) son útiles pero complicados en niños, por lo que no se debe realizar más de 3 intentos.
Los accesos venosos centrales (IVC) son más seguros a largo plazo, pero requieren entrenamiento y experiencia, su canalización lleva tiempo, y no ofrecen grandes ventajas durante la reanimación en comparación con el IO o el IVP, por lo que no se recomiendan como acceso inicial.
En caso de disponer de accesos periféricos y centrales, usaremos preferentemente el acceso central, dado que hay medicación que resulta más efectiva cuando se administra cerca del corazón (p.ej. adenosina) y otra que puede resultar irritante cuando se infunde en una vena periférica (p.ej. calcio, Amiodarona, etc.).
Medicación Intratraqueal
Si el acceso vascular no es posible, los medicamentos liposolubes (como la Lidocaína, Epinefrina, Atropina y Naloxona [LEAN]) pueden usarse por vía Intratraqueal a través del TET. Para ello se deben cesar las compresiones, se administrará la medicación diluida en 5 ml de SSF 0,9% y realizaran 5 ventilaciones.
Sin embargo, los efectos no serán iguales a los obtenidos por vía intravenosa. Además, las dosis óptimas intratraqueales son desconocidas a causa de la gran variabilidad de la absorción alveolar. Los expertos de la AHA recomiendan doblar o triplicar la dosis de lidocaína, atropina o naloxona cuando se administran a través del TET. La epinefrina se administrará a dosis 10 veces superiores a las intravenosas (0,1 mg/kg, o 0,1 ml/kg a una concentración de 1:1.000). Tabla 1
El ERC recomienda:
No debe emplearse esta vía para administrar medicación no liposolube (p.ej. glucosa, bicarbonato sódico, calcio, etc.), puesto que pueden dañar la mucosa de la vía aérea.
TABLA 1














Por favor necesito que me envien a mi correo el articulo de RCP Pediatrico