 Mª Isabel Rodríguez Macías.
Mª Isabel Rodríguez Macías.
Aránzazu Fernández Rodríguez.
Artículo original: Illman HL, Laurila P, Antila H, Meretoja OA, Alahuhta S, Olkkola KT. The duration of residual neuromuscular block after administration of neostigmine or sugammadex at two visible twitches during train-of-four monitoring. Anesth Analg. 2011 Jan;112(1):63-8. Epub 2010 Oct 26 (PubMed)
Cómo citar este artículo: Rodríguez Macías, M. I., & Fernández Rodríguez, A. (2011). Bloqueo neuromuscular residual tras administración de rocuronio: comparación sugammadex-neostigmina: : Illman HL, Laurila P, Antila H, Meretoja OA, Alahuhta S, Olkkola KT. The duration of residual neuromuscular block after administration of neostigmine or sugammadex at two visible twitches during train-of-four monitoring. Anesth Analg. 2011 Jan;112(1):63-8. Epub 2010 Oct 26. Revista Electrónica AnestesiaR, 3(6), 3. https://doi.org/10.30445/rear.v3i6.450
Introducción
En la recuperación anestésica es imperativa una adecuada recuperación del bloqueo neuromuscular (BNM) para que el paciente tenga un control completo sobre los músculos faríngeos y respiratorios. Se necesita una TOF ratio de al menos 0,9 para excluir bloqueo residual postoperatorio clínicamente significativo.
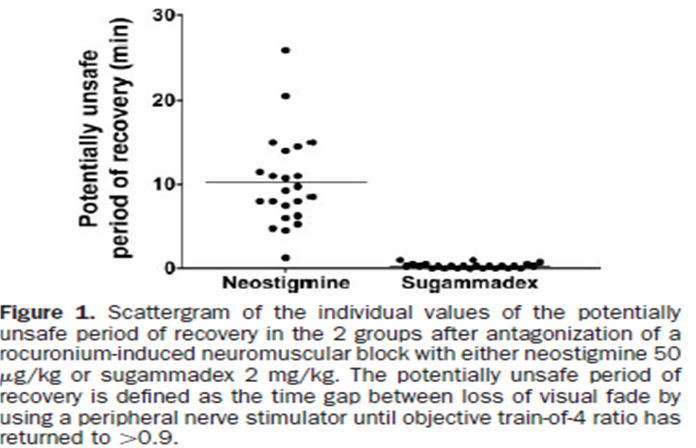
La amortiguación de la respuesta del Tren de Cuatro (TOF) puede no ser detectada fiablemente con un estimulador de nervio periférico (PNS), hasta con un TOF ratio de 0,4. El lapso de tiempo entre la pérdida visual de la amortiguación usando un PNS hasta que el TOF ratio medido objetivamente es de 0,9, es considerado por los autores como el“ período de recuperación potencialmente inseguro“, durante el cual el paciente está expuesto a una serie de riesgos como pueden ser eventos respiratorios críticos.
La neostigmina antagoniza el BNM por inhibición de la acetilcolinesterasa, lo cual aumenta la cantidad de acetilcolina en la unión neuromuscular, pero no tiene efecto en la tasa de eliminación del fármaco bloqueante. Además su inicio de acción es relativamente lento y debido a su efecto techo, no puede antagonizar niveles profundos de BNM. La nueva droga reversora sugammmadex es, debido a la encapsulación del rocuronio que ocurre primariamente en el plasma, capaz de revertir incluso un profundo o intenso BNM administrando la dosis necesaria en relación a la cantidad de rocuronio en el organismo.
De acuerdo a la hipótesis de los autores, la duración de este período podría ser significativamente más corta con sugammadex que con neostigmina.
Resumen
Se realiza un ensayo clínico aleatorizado (ECA) a doble ciego con pacientes anestesiados y con BNM inducido con rocuronio, monitorizados objetivamente mediante TOF-Watch, aunque los anestesiólogos sólo realizaron evaluación visual de las respuestas del TOF, siendo distribuidos en dos grupos (según secuencia aleatoria) para recibir, al finalizar la intervención, neostigmina o sugammadex una vez detectadas dos respuestas del TOF tras la última dosis de rocuronio.
Método
Se incluyeron 50 pacientes programados para cirugía electiva requiriendo anestesia general. Los pacientes eran hombres o mujeres, de edades entre 18 y 70 años y con ASA entre I-IV. La inducción de la anestesia general se realizó con propofol y un opioide de acuerdo con la rutina del centro del estudio. Dependiendo de la duración estimada de la anestesia y otros factores clínicos, se utilizó rocuronio entre 0,6-1 mg/kg para facilitar la intubación endotraqueal. El mantenimiento se realizó con un anestésico volátil (sevofluorado o desfluorano) junto con opioides. El grado de BNM fue medido con un monitor pero con dos métodos: la monitorización objetiva aplicando la aceleromiografía fue usado en paralelo con la evaluación visual de la respuesta. El modo TOF de estimulación fue aplicado (2Hz, 0,2 ms) a intervalos de 15 segundos durante el procedimiento.
El anestesiólogo a cargo del paciente no conocía el objetivo de las mediciones y cuantificó el grado de BNM sólo por la evaluación visual de la respuesta muscular. Las medidas objetivas fueron transferidas desde el TOF-Watch a un ordenador para su procesamiento. La administración de rocuronio adicional y momento de administración de neostigmina o sugammadex, fueron por lo tanto basados sólo en la evaluación visual de las respuestas del TOF. Al final de la cirugía, los pacientes anestesiados fueron aleatoriamente asignados a dos grupos. La aleatorización fue realizada utilizando sobres sellados generados por ordenador para determinar qué fármaco reversor debía recibir cada paciente. El sobre contenía instrucciones escritas para preparar neostigmina 50mcg/kg + glicopirrolato 10 mcg/kg ó sugammadex 2 mg/kg para revertir el BNM. El anestesiólogo tampoco conocía el fármaco reversor utilizado.
Resultados
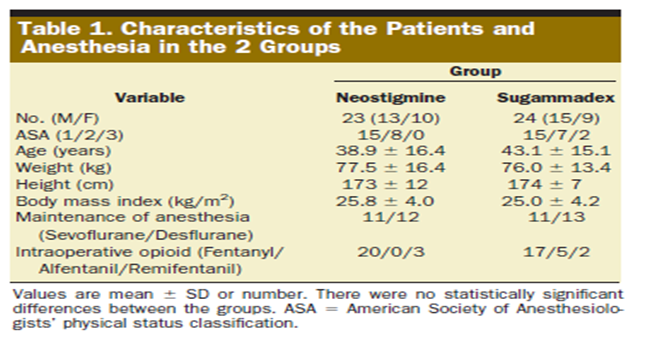
Las características de los pacientes y la anestesia se presentan en la tabla 1.
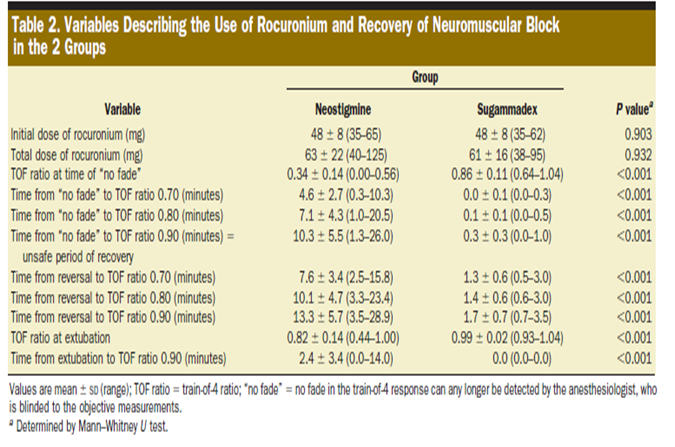
Los pacientes eran similares y no había diferencias significativas en la conducta de la anestesia en los dos grupos. Los principales resultados del estudio se muestran en la tabla 2 y la figura 1.
El período de recuperación potencialmente inseguro, el tiempo transcurrido desde la pérdida visual de la amortiguación de la respuesta hasta el retorno al TOF ratio de 0,9, fue 10,3+5,5 minutos en el grupo de la neostigmina y 0,3+0,3 minutos para el del sugammadex.
Conclusiones
Los autores concluyen que sus resultados corroboran los de estudios anteriores donde se mostraba que la neostigmina actuaba más lentamente que el sugammadex para la reversión del BNM inducido por rocuronio y, además, aportan información clínicamente importante sobre los riesgos potenciales si el clínico se basa únicamente en la estimación visual del BNM usando un estimulador de nervio periférico.
Comentario
Este artículo aborda un tema ya tratado con anterioridad1,2, pero demuestra específicamente en un estudio controlado y aleatorizado que el uso de neostigmina en combinación con evaluación visual de la respuesta muscular a la estimulación del nervio periférico puede aumentar el riesgo de parálisis residual postoperatoria.
Se ha demostrado que el bloqueo neuromuscular residual posoperatorio y la debilidad muscular resultante causada por los BNM no despolarizantes se asocian con mayor mortalidad y morbilidad. El bloqueo neuromuscular residual puede dar lugar a complicaciones pulmonares, por ejemplo respiración laboriosa, bajos niveles de oxígeno en la sangre, infección pulmonar e ingreso del contenido gástrico en los pulmones.3,4,5 Además, puede producir una disminución posoperatoria en la fuerza muscular con complicaciones asociadas, como dificultades visuales, recuperación y momento del alta retardados.3
Se ha indicado sugammadex para la reversión habitual del bloqueo neuromuscular inducido por rocuronio. En este sentido, todos los ensayos incluidos en una amplia revisión sistemática6 han utilizado la reaparición a nivel de T2 como el tiempo de administración de sugammadex. La dosis óptima de sugammadex (≥ 2 mg/kg) administrada en este momento revirtió con éxito el bloqueo neuromuscular dentro de los 3 min. y 16 veces más rápido que la neostigmina.
Hay un consenso generalizado entre los expertos de que los métodos objetivos de monitorización son mucho más seguros y fiables que la evaluación táctil o visual de la respuesta de contracción muscular tras estimulación con PNS. Este estudio muestra que la adecuada recuperación del bloqueo con rocuronio no puede asegurarse empleando evaluación visual del BNM, especialmente cuando el fármaco reversor es la neostigmina y que la monitorización objetiva es necesaria para excluir la parálisis residual.
Bibliografía
1.- de Boer HD, Driessen JJ, Marcus MA, Kerkkamp H, Heeringa M, Klimek M. Reversal of rocuronium-induced (1.2 mg/kg) profound neuromuscular block by sugammadex: a multicenter, dose-finding and safety study. Anesthesiology 2007;107:239““44. (PubMed) (pdf) (epub)
2.- Jones RK, Caldwell JE, Brull SJ, Soto RG. Reversal of profound rocuronium-induced blockade with sugammadex: a randomized comparison with neostigmine. Anesthesiology. 2008 Nov;109(5):816-24. (PubMed) (pdf) (epub)
3.- Murphy GS. Residual neuromuscular blockade: incidence, assessment, and relevance in the postoperative period. Minerva Anestesiologica 2006; 72: 97-109. (PubMed) (pdf)
4.- Sundman E, Witt H, Olsson R, Ekberg O, Kuylenstierna R, Eriksson LI. The incidence and mechanisms of pharyngeal and upper oesophageal dysfunction in partially paralysed humans. Pharyngeal video radiography and simultaneous manometry after atracurium. Anesthesiology 2000; 92: 977-84. (PubMed) (pdf) (epub)
5.- Murphy GS, Szokol JW, Marymont JH, Greenberg SB, Avram MJ, Vender JS. Residual neuromuscular blockade and critical respiratory events in the postanesthesia care unit. Anesth Analg 2008;107:130““7. (PubMed) (pdf)
6.- Amir Abrishami, Joyce Ho, Jean Wong, Ling Yin, Frances Chung. Sugammadex: fármaco de reversión selectiva para la prevención del bloqueo neuromuscular residual posoperatorio (Revision Cochrane traducida). En: Biblioteca Cochrane Plus 2009 Número 4. (html)
Mª Isabel Rodríguez Macías.
Servicio de Anestesiología, Reanimación y Terapéutica del Dolor. H.U. San Cecilio de Granada.
Aránzazu Fernández Rodríguez.
Servicio de Anestesiología, Reanimación y Terapéutica del Dolor. H.U. Virgen de las Nieves de Granada.





Escribe un Conocido experto en el tema: «Thus, even after the introduction of sugammadex,
neuromuscular monitoring will be useful, allowing the right dose to be
chosen. The alternative would be to give a large sugammadex dose
for all cases, a more expensive course of action than monitoring»
-Donati F. Sugammadex: an opportunity for more thinking or more cookbook
medicine? Can J Anesth 2007; 54: 9:689″695…
Donati tiene razón, a la sazón es revisor adjunto del CJA….pero lamentablemente (según la segunda alternativa del parráfo de arriba) la población de anestesiologos han convertido la reversión de un BNM inducido por rocuronio en la administración de una dosis fija de sugammadex sin utilizar un monitor como guía. Peor todavía, ni lo refieren en la hoja de anestesia.
Joaquin,
Ésa es la gran victoria del marketing. Sería una desgracia que esa actitud se impusiese. Pero es verdad que llegan comentarios de hospitales donde su uso se ha extendido de esa forma.
En nuestro hospital, sin embargo, su uso sigue limitado a unas indicaciones muy concretas y lo más curioso, quizá, es que se cumplen.
Es poco frecuente que se administre sin una razón (no por el mero hecho de no haber prestado atención a la dosificación correcta del roruronio) y cuando se hace, después de un incidente crítico en el que se tuvo que reintervenir un paciente que habia recibido sugammadex y que no se había transmitido la información correctamente, con lo que en la segunda inducción el rocuronio no le hacía efecto, ahora no sólo se escribe en todas las hojas de anestesia, sino que se avisa especialmente con una pegatina de color llamativo.
Estoy de acuerdo contigo en que el uso indiscriminado del fármaco puede ser una mera irresponsabilidad ética, pero el no reflejarlo en la hoja de anestesia en caso de reintervención urgente puede ser peligroso.