Miguel García Bellón. Complejo Hospitalario de Toledo.
Carmen Soria Bretones. Hospital Virgen de la Luz. Cuenca.
Cómo citar este artículo: García Bellón, M., & Soria Bretones, C. (2013). Electroencefalografía en Cuidados Críticos. Revista Electrónica AnestesiaR, 5(2), 3. https://doi.org/10.30445/rear.v5i2.284
Introducción
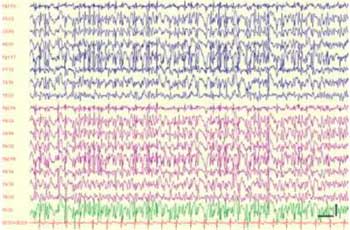 La electroencefalografía es la ciencia que estudia mediante un registro gráfico, en papel o digital, la actividad eléctrica generada por el córtex cerebral, en tiempo real (1,2), presentando una resolución temporal entre 2-4 mseg. (3). Se registra mediante electrodos colocados en cuero cabelludo. Normalmente se utiliza el sistema internacional 10-20 para obtener una adecuada localización topográfica de las señales generadas en el córtex.
La electroencefalografía es la ciencia que estudia mediante un registro gráfico, en papel o digital, la actividad eléctrica generada por el córtex cerebral, en tiempo real (1,2), presentando una resolución temporal entre 2-4 mseg. (3). Se registra mediante electrodos colocados en cuero cabelludo. Normalmente se utiliza el sistema internacional 10-20 para obtener una adecuada localización topográfica de las señales generadas en el córtex.
La señal obtenida, corresponde a la suma de los potenciales de acción postsinápticos de las neuronas piramidales de la corteza cerebral. Esta señal es amplificada por diversos equipos informáticos, y tiene una correlación espacial dada por los distintos electrodos.
Mediante el EEG, se puede obtener información localizada, y en tiempo real de distintos procesos que alteran la función normal de la corteza cerebral, ya sean focos epileptógenos, lesiones focales, procesos isquémicos o metabólicos.
Además permite evaluar el nivel de consciencia, y sus distintas fluctuaciones, la reactividad cortical a diversos estímulos. Tiene un valor pronóstico en función de los distintos patrones registrados y permite evaluar el ciclo vigilia-sueño.
Sitema Internacional 10-20
Es un sistema estandarizado de colocación de los electrodos sobre el cuero cabelludo (Figura 1). Sigue estando vigente en la mayoría de los laboratorios de electroencefalografía.
La numeración par corresponde al hemicráneo derecho, y la impar al izquierdo.
Las letras representan areas frontales (Fp y F), temporales (T), parietales (P), centrales (C) y occipitales (O); además de dos electrodos de referencia en orejas (A).
La letra z corresponde a electrodos de línea media.
Tipos de monitorizacion EEG
Registros puntuales
Valoran en un preciso momento la función cerebral. Está sujeto a variaciones y fluctuaciones en el nivel de consciencia. En este tipo de registro, deben de darse unas mínimas condiciones de reposo, además de realizar maniobras de fotoestimulación, hiperventilación, para ver la reactividad ante distintos estímulos.
Registro estándar 20 -30 minutos: Un único registro puede ser normal y no detectar anomalías. Tras un segundo registro, aumenta la sensibilidad y especificidad de la prueba. Las maniobras de hiperventilación y fotoestimulación favorecen la aparición de grafoelementos epileptiformes. En pacientes ingresados en UCI, la capacidad de detectar actividad crítica, es del 11% (4).
Registro de 45 minutos: Pueden detectar mejor las distintas alteraciones epileptiformes que puedan surgir a lo largo del registro. A mayor duración del registro, mayor posibilidad de encontrar anomalías. Se pueden hacer tras privación de sueño, lo que induce con gran frecuencia alteraciones irritativas corticales y subcorticales subyacentes.
Registro tras privación de sueño: Se realiza el registro tras un mínimo de 6 horas de privación de sueño espontáneo nocturno, dependiendo de la tolerancia del paciente. Pone de manifiesto y acentúa posibles anomalías corticales y subcorticales. Sobre todo durante las fases superficiales de sueño I y II.
Registro EEG Continuo
El registro EEG continuo consiste en la monitorización continua de la actividad cerebral durante largos periodos de tiempo, variables entre 24-72 horas. Actualmente, los sistemas modernos permiten la integración en tiempo real de la señal de vídeo. Si hay alteración funcional, en registros largos de 24-48 horas, se pondrán de manifiesto. En algunos estudios, el registro EEG continuo, muestra una sensibilidad para detectar crisis del 28% (4, 5).
Principales ritmos corticales en el EEG adulto
Ritmos Beta: Actividad rápida entre 14-50 Hz. Localización en regiones frontales y temporales anteriores. Frecuente en estados de vigilia concentrado, o nerviosismo. Hay un porcentaje de población que presenta este patrón EEG de forma basal. También se observa ritmo beta secundario a inteferencia medicamentosa, sobre todo benzodiacepinas (Figura 2).
Ritmos Alfa: Actividad entre 8-12 Hz. Localización en regiones occipitales. Ritmo predominante en vigilia relajada. Reactivo a apertura y cierre palpebral.
Hay que ser cauto en su valoración en niños y ancianos. Su frecuencia se enlentece por encefalopatías tóxico-metabólicas, hipoxia, hipocapnia, múltiples fármacos, y en los estados de demencia (Figura 3).
Ritmos Theta: Activiad lenta entre 4-8 Hz. Patológico en vigilia. Pone de manifiesto alteraciones corticales y subcorticales. Muy frecuente en estadios iniciales de demencia. Frecuente encontrarlo en lesiones focales de origen vascular.
OJO: Fisiológico en registros de sueño y en niños menores de 18-20 años (Figura 4).
Ritmos Delta: Actividad muy lenta a 1-4 Hz. Patológico en vigilia. Pone de manifiesto alteraciones corticales y subcorticales. Se puede observar en demencias muy avanzadas, encefalopatías metabólicas y tóxicas. Patrón en brote-supresión. Patrón de ondas trifásicas (típicas de encefalopatía hepática). Estos ritmos aparecen de manera precoz en procesos isquémicos agudos (Figura 5).
Principales grafoelementos de carácter patológico en el EEG
Punta: Es un aumento transitorio y bien definido de la actividad eléctrica de base, de morfología picuda, y duración entre 20 y 70 milisegundos. La amplitud es variable. Corresponden a descargas neuronales hipersincrónicas y simultáneas. Si aparece en un único electrodo, sospechar que se trate de un artefacto (Figura 6).
Ondas agudas: Aumento transitorio y bien definido de la actividad eléctrica de base, de y morfología picuda, y duración entre 70 y 200 milisegundos (Figura 7).
Estos grafoelementos son altamente sugestivos de trastornos epilépticos, aunque también pueden verse en pacientes sin antecedentes de epilepsia.
La agrupación de estos principales grafoelementos dan lugar a otros gafoelementos compuestos:
– Punta onda: Esta formada por una punta seguida de una onda, lenta, que aparece con distribución focal o generalizada (Figura 8).
– Polipunta: Compuesta por varias puntas en ráfaga, que pueden ir seguidas de onda lenta o no (Figura 9).
– Polipunta-onda: Es igual que la punta onda, pero con dos o más puntas (Figura 10).
– Onda aguda lenta: Onda aguda que dura más de 200 milisegundos (Figura 11).
Indicaciones de la monitorización EEG en el paciente crítico
La interpretación y valoración del registro electroencefalográfico ha de ser realizada por un especialista en neurofisiología clínica.
Imprescindible
Status Epiléptico
Según la Epilepsy Foundation of America Working Group, y varios estudios recientes, el status epiléptico se define como cualquier crisis comicial que dure 30 minutos o más, o varias crisis comiciales intermitentes durante más de 30 minutos, tras las cuales, el paciente no recupera la consciencia (Fig.12).
La mortalidad del Status epiléptico varía entre el 17 y 23 % (6).
Se debería hacer un EEG urgente en las siguientes situaciones:
– Arreactividad prolongada y severa tras ictus. El EEG podrá diferenciar entre patrones de coma, en los que no hay actividad epileptiforme, y patrones típicos de Status epiléptico.
– Pacientes que hayan recibido relajantes musculares y/o sedantes, en los que es difícil diferenciar e identificar signos clínicos de actividad comicial.
– Pacientes con signos clínicos atípicos, para diferenciarlos de pseudocrisis.
– Status epiléptico refractario a tratamiento con benzodiacepinas y anticomiciales.
Muy Recomendable
Monitorización de actividad comicial no convulsiva, o status epiléptico no convlusivo (SENC)
No hay una definición clara de status epiléptico no convulsivo (SENC). El diagnóstico lo dan los cambios clínicos, sobre todo fluctuaciones del nivel de consciencia, y las alteraciones en el EEG.
Maganti et al lo definieron como «condición con estado prolongado de alteración del nivel de conciencia asociado a actividad paroxística continua o descargas eléctricas en el EEG» (7).
El EEG es la herramienta imprescindible para el diagnóstico del SENC (8).
Hay varios patrones EEG en el SENC (9,10):
– Generalizado: Indican una afectación global de toda la corteza cerebral.
* Presencia de puntas y polipuntas generalizadas, registrados en todos los canales, presentan cierta periodicidad y frecuencia, sobre todo a 2-3 Hz (Figura 13).
* Ondas trifásicas, típicas de encefalopatías, de predominio en regiones frontotemporales anteriores (Figura 14).
* Patrones de brote-supresión (Figura 15).
– Lateralizado: Indican afectación de una o varias regiones corticales:
* Presencia de puntas y polipuntas focales, en una región en concreto.
* Presencia de actividad intercrítica, con periodicidad (PLEDS) (Figura 16).
Pacientes con riesgo de isquemia cerebral
La isquemia cerebral provoca cambios en el EEG, incluso sin evidencia de infarto. Las capas corticales 3 y 5 son especialmente sensibles a los déficits de oxígeno (9).
– Hemorragias subaracnoideas. Se ha utlizado el EEG continuo en el paciente crítico para detectar el vasoespasmo secundario a la hemorragia subaracnoidea (10, 11).
– Esta monitorización es muy útil en el seguimiento de pacientes con AIT (sobre todo durante el sueño, cuando no pueden manifestar síntomas).
Los cambios en el EEG, pueden preceder al deterioro clínico hasta 2 días (12).
Patrones EEG en Alteraciones de la Perfusión Cerebral
PROCESOS ISQUÉMICOS: Enlentecimiento de la actividad eléctrica cerebral, focal, abarcando todo un hemisferio, según la magnitud del territorio afecto.
Disminución del voltaje, lentificación del trazado. Aparición de ritmos Theta-Delta (Figura 17).
Vigilar, valorar y cuantificar sobre todo la asimetría interhemisférica. Hay una correlación muy cercana en la alteración EEG y la lesión. Además, su ajustada resolución temporal, lo hace muy adecuado para detectar procesos isquémicos incipientes. Pacientes con AIT ya resueltos y asintomáticos, pueden presentar alteraciones en el EEG, por lo que el EEG es una herramienta útil para detectar isquemias tardías. Lesiones isquémicas incipientes, y áreas con compromiso vascular, pero asintomáticas, presentan alteraciones durante las maniobras de hiperventilación.
Lesiones isquémicas establecidas, presentan brotes de actividad Theta-Delta de manera continua en la región implicada.
PROCESOSO HEMORRíGICOS: Tienen una mayor tendencia a presentar actividad irritativa y grafoelementos de tipo punta-onda y ondas agudas que las lesiones isquémicas. Escasa repercusión EEG si la lesión es en regiones subcorticales profundas, en bulbo o mesencéfalo (aunque pueden observarse brotes de actividad Delta).
Trauma Craneal Agudo
El EEG es muy útil para la detección precoz de crisis comiciales inmediatas al TCE (Figura 18). En caso de necesitar sedación profunda, permite determinar grado de profundidad según los distintos trazados EEG (patrón brote-supresión) (13,14). Esto evitará dejar al paciente con registro EEG isoeléctrico (Figura 19).
El EEG valora las anomalías EEG críticas e intercríticas. Lo más frecuente es registrar grafoelementos de tipo punta-onda, polipunta-onda y ondas agudas.
Durante las crisis comiciales, estos grafoelementos tienen una ritmicidad, y una atenuación del voltaje posterior, conocida como silencio postcrítico (Figura 20).
Diagnóstico y Pronóstico del Coma
Es muy importante diagnosticar a estos pacientes. El incremento metabólico y del flujo sanguíneo que se produce secundariamente a la actividad comicial, puede comprometer todavía más el tejido cerebral (15).
Los cambios en el EEG pueden correlacionarse con marcadores bioquímicos de daño neuronal específico, como la enolasa específica neuronal (16).
Patrones electroencefalograficos indicativos de mal pronóstico en pacientes en coma:
– Frecuencias lentas. Sobre todo actividad Delta, con poca variabilidad.
– Dismincuión de la reactividad a estímulos: Tactiles, dolorosos, auditivos, luminosos, etc…
– Desaparición de los grafoelementos del sueño, como los complejos K, o los husos de sueño, implican disfunción de estructuras subcorticales.
– Patrón de Coma Alfa: La presencia de ritmos en la frecuencia alfa, generalizados, y sin reactividad, implica un pronóstico ominioso, en el cual la tendencia es la muerte en escasos días, o el estado vegetativo persistente (17) (Figura 21).
– Patrón de brote-supresión: Se intercalan brotes de actividad Delta, seguidos de un periodo de atenuación de voltaje, de varios segundos o minutos de duración. Aparecen cuando el flujo cerebral está comprometido. Muy mal pronóstico. Es típico de la encefalopatía anóxico isquémica, en la que toda la corteza cerebral ha sufrido una isquemia global y mantenida. Estos patrones pueden observarse tras la administración de anestésicos, como propofol, y sevoflurano.
Recomendable
– Diagnóstico de muerte cerebral: Registro electroencefalográfico isoeléctrico y arreactivo en todas las derivaciones. El trazado EEG no se modifica tras las maniobras de estimulación (Figura 22).
– Evaluación de la función cerebral en pacientes que no pueden manifestar síntomas: Síndrome del cautiverio, Síndrome de Guillen-Barré con afectación de pares craneales altos, botulismos, etc…
– Diagnóstico de encefalopatías metabólicas en pacientes con fluctuaciones del nivel de consciencia. Encefalopatía hepática. Encefalopatía urémica: Características ondas trifásicas de predominio en regiones fronto-temporales (Figura 23).
– Encefalitis: patrón de enlentecimiento muy específico, con actividad Delta generalizada entre 2-4 Hz.
– Encefalitis herpética: Alteraciones EEG previas a desarrollo de lesión. Brotes de actividad Theta-Delta en regiones temporales, y frecuentes grafoelementos agudos (Figura 24).
– Encefalopatía de Creutfeld Jacob: Patrón EEG casi patognomónico (18) (Figura 25).
– Pacientes agitados o desorientados que no recuperan su situación basal previa.
– Pacientes arreactivos. Descritos casos de mutismo acinético.
Beneficios de la monitorización EEG del paciente crítico
– Rápida identificación de alteración funcional cortical, permitiendo una rápida actuación.
– Detección de isquemia tardía.
– Identificación de status epiléptico y tratamiento, además de su respuesta al tratamiento.
– Identificación del Status no convulsivo.
– Determinar grado de reactividad cerebral, mediante las distintas maniobras de activación.
– Identificar patrones electroencefalográficos de mal pronóstico.
– Determinar grado de profundidad de la sedación.
Limitaciones de la monitorizacion del paciente crítico
– Necesidad de personal entrenado y experimentado. El registro debe ser informado por un médico especialista en neurofisiología clínica
– Necesita espacio físico.
– Fluctuaciones individuales a lo largo del tiempo. El individuo puede variar en su grado de lucidez a lo largo del día, dependiendo de múltiples factores. Fármacos, somnolencia, grado de perfusión cerebral, cifras de presión arterial…
– Variaciones interobservador; e incluso en el mismo observador.
– No diferencia bien causas hipóxico-isquémicas o metabólicas.
Aspectos a tener en cuenta en la monitorizacion EEG en pacientes críticos
Efectos de los distintos Fármacos en El EEG:
1.- Medicacion Anestesica Y Sedacion:
SEVOFLURANO: Deprime la actividad EEG, dependiendo de la concentración empleada, pudiendo llegar a registrase patrones de brote-supresión.
Además, en individuos susceptibles, como niños y ancianos, y en pacientes con antecedentes epilépticos, pueden observarse registros con grafoelementos epileptiformes, aunque la mayor parte de ellos sin crisis comiciales clínicas.
Es por ello conveniente evitar las dosis altas de sevoflurano en esta población, manteniendo una CAM<1,5 durante el mantenimiento en estos pacientes y monitorizar al menos la profundidad anestésica con los medios disponibles (BIS o EEG).
OXIDO NITRICO: Los cambios EEG varían dependiendo de la concentración. Concentraciones entre el 30““40% provocan una fragmentación de los ritmos alfa en regiones posteriores. Concentraciones en torno al 50%, producen incremento de la actividad Beta. Los ritmos lentos Theta, aparecen en concentraciones del 70-80%. El EEG tarda una hora en normalizarse tras la supresión del NO.
PROPOFOL: Deprime la actividad EEG, de manera dosis-dependiente. Dosis entre 40-200 mg, producen patrón de brote-supresión. Su administración provoca cambios en el EEG muy similares a los registrados durante el sueño fisiológico.
ETOMIDATO: Derivado imidazólico. Actúa directamente sobre los receptores GABA. Tiene efectos proconvulsivantes por varios mecanismos: Inhibición de las interneuronas inhibitorias, y mediante excitación directa. De hecho, hay estudios que utilizan el etomidato como método de activación EEG para detectar anomalías epileptiformes (19).
BENZODIACEPINAS: Aumentan los ritmos beta. Ritmos beta de origen medicamentoso. A pesar que el paciente está relajado. Duración de estos efectos hasta 2 semanas (Figura 26).
Es importante distinguir entre benzodiacepinas de uso ansiolítico y de inducción anestésica.
Tener en cuenta si hay perfusión continua o dosis repetitivas de benzodiacepinas, que alteran la estructura normal del sueño, disminuyendo la cantidad de sueño profundo, las fases III y IV.
BARBITURICOS:. Dependiendo de la dosis empleada. Dosis pequeñas, producen ritmos rápidos en el rango beta en regiones frontales. Dosis mayores, provocan fragmentación del ritmo alfa, y registros de sueño superficial y profundo.
El tiopental, produce rápidamente un patrón de brote-supresión, en relación con su capacidad de depresión metabólica cerebral (20).
KETAMINA: Respuesta EEG dosis dependiente. Provoca brotes de actividad Theta, persistentes en el tiempo.
OPIíCEOS. Escaso efecto en el EEG. Discreto enlentecimiento del ritmo alfa. Facilita la inducción del sueño espontáneo.
2.- ANTIBIÓTICOS:
BETA-LACTíMICOS:
– Carbamenem: pueden inducir crisis comiciales, con una frecuencia variable entre un 3-33%. La potencia epileptogénica está en relación con el la estructura anillada del beta-lactamico, que se une a los receptores gabaérgicos. Pacientes con insuficiencia renal, altas dosis de fármacos, y antecedentes de lesión del sistema nervioso central, presentan crisis comiciales con mayor frecuencia.
– Cefalosporinas: Ceftriaxona, ceftacidima (3ª generación), y Cefepime (4ª generación). Hay descritos casos de status no convulsivos en relación con esta medicación en pacientes en insuficiencia renal (21).
QUINOLONAS: Levofloxacino y ciprofloxacino: Hay descritos casos de crisis comiciales, asociadas a altas dosis de medicamento, edad avanzada, alteraciones hidroelectrolíticas, y fármacos asociados, como teofilinas, metoclopramida, y mirtazapina (estas últimas por interacciones con citocromo CYP1A2 (22).
Las manifestaciones clínicas de la neurotoxicidad por antibióticos varían, siendo frecuentes los cuadros de estupor, encefalopatía, asterixis, crisis comiciales. Todos ellos muy variables y de difícil interpretación. Las alteraciones EEG que provocan varían desde discretos grafoelementos epileptiformes de tipo punta-onda y ondas agudas, hasta la presencia de estatus no convulsivos, incluyendo el patrón de ondas trifásicas típico de encefalopatías.
Medidas Preventivas ante Crisis Comiciales de Origen Farmacológico
– Evitar en la medida de lo posible sevoflurano y etomidato.
– Considerar profilaxis de las crisis empleando agonistas Gabaérgicos (benzodiacepinas, sobre todo Midazolam).
– Realizar al menos un electroencefalograma para detectar anomalías corticales o grafoelementos epileptógenos.
Artefactos del EEG
Son múltiples y variados los artefactos que se producen en el entorno del paciente. Es esencial identificarlos y saber interpretarlos, para realizar una correcta lectura del electroencefalograma (23,24,25).
Pueden llegar al punto de hacer un registro no valorable.
Artefactos Del Entorno
Corriente alterna: Provocado por la corriente eléctrica de 50Hz, generada por infinidad de aparatos: Bombas de infusión, cama eléctrica, manta de calor, respirador, máquina de diálisis.
Colocar bien los electrodos, preparar la piel del cuero cabelludo, disminuir en lo posible las impedancias, y colocar una toma de tierra, disminuirá la incidencia de este molesto artefacto. Colocar siempre el filtro de corriente alterna para minimizarlo (Figura 27).
Mal contacto de electrodos: Provoca inestabilidad en las impedancias, dando lugar a ondas muy agudas, que confluyen en el trazado en la región correspondiente al electrodo mal colocado. Recolocando el electrodo se corrige con facilidad (Figura 28).
Marcapasos: Da lugar a ondas agudas, rítmicas, cuando la derivación electrocardiográfica del EEG se sitúa cerca del marcapasos.
Artefactos Biológicos
Artefacto electromiográfico: Es el artefacto biológico más frecuente. Secundario a la contracción de los músculos del cuero cabelludo, frontal, facial, masetero, y cuello. La contracción de maseteros, pueden hacer un registro indescifrable.
Estos artefactos se pueden atenuar desfrunciendo el ceño, abriendo la boca, y si es secundario a dolor o nerviosismo, pautando analgesia o sedación leve ( valorar el tipo de sedante, por el efecto de los ritmos beta medicamentosos de las BZD) (Figura 29).
Artefacto de movimientos musculares involuntarios: Muy frecuentes en el paciente crítico la existencia de mioclonías, temblor, o actividad tónico-clónica.
Artefactos de parpadeo: Fácilmente identificables. De elevada amplitud, se transmite a regiones frontales (Figura 30).
Artefacto glosocinético: El movimiento de la lengua, provoca un artefacto que puede interpretarse como un brote de actividad lenta generalizado, de máxima amplitud en regiones centrales. ,
Artefacto glosofaríngeo: El movimiento realizado al tragar, activa la lengua, musculatura faríngea, y esfenopalatina, que se transmite como brotes de actividad lenta en regiones centrales.
Sudor: Importantes oscilaciones muy lentas en todos los canales, sobre todo en los frontales. Disminución de la temperatura, o abanicar al enfermo pueden eliminarlo o atenuarlo.
Artefacto Arterial: Los electrodos situados cerca de las arterias temporales, o en arteriolas, generan una onda con morfología de punta pulsátil, rítmica. Se corrige cambiando el electrodo de posición.
Artefacto electrocardiográfico: El potencial de acción generado por el corazón, se transmite hasta el cuero cabelludo, dando lugar a puntas rítmicas, que pueden ser confundidas con crisis comiciales.
Balistocardiográfico: El propio movimiento del corazón transmite fluctuaciones que se registran en cuero cabelludo.
EEG durante el sueño en pacientes Críticos
Los pacientes críticos, presentan un importante número de alteraciones del sueño.
Hay un importantísima desestructuración de la arquitectura normal del sueño, con frecuentes despertares, disminución de las fases profundas, tanto Fases III y IV, como REM, además de frecuentes alteraciones del ciclo vigilia-sueño.
Las causas más frecuentes son el propio entorno, el elevado nivel de estrés, las frecuentes interrupciones por medicación y maniobras médicas, cambios posturales, la ventilación mecánica, etc.
Esta alteración de la arquitectura normal del sueño, puede enlentecer la recuperación de los pacientes. La disminución de las fases profundas de sueño, da lugar a una disminución de la síntesis proteica de múltiples hormonas y neurotransmisores. Además, la privación de sueño por sí misma, activa y facilita la aparición de grafoelementos epileptiformes en pacientes susceptibles (26,27).

Bibliografía
1.- Hans-Christian Hansen, Jan Claassen. EEG and Evoked Potentials in Neuroanesthesia, Intraoperative Neurological Monitoring, and Neurointensive Care; Niedermeyer, Ernst; da Silva, Fernando Lopes Da Silva. Electroencephalography, basic principles, clinical applications, and related fields. 5th Edition. (googlebooks)
2.- Gil-Nagel A, Parra J, Iriarte J, Kanner A M. Manual de electroencefalografía. (googlebooks)
3.- Scheuer ML.Continuous EEG monitoring in the intensive care unit. Epilepsia. 2002;43 Suppl 3:114-27. (PubMed)
4.- Pandian JD, Cascino GD, So EL, Manno E, Fulgham JR. Digital video-electroencephalographic monitoring in the neurologicalneurosurgical intensive care unit: clinical features and outcome. Arch Neurol 2004;61:1090““4. (PubMed) (pdf)
5.- Friedman D, Claassen J, Hirsch LJ. Continuous electroencephalogram monitoring in the intensive care unit. Anesth Analg. 2009 Aug;109(2):506-23. (PubMed) (pdf)
6.- Claassen J, Lokin JK, Fitzsimmons BF, Mendelsohn FA, Mayer SA. Predictors of functional disability and mortality after status epilepticus. Neurology. 2002 Jan 8;58(1):139-42. (PubMed)
7.- Maganti R, Gerber P, Drees C, Chung S. Nonconvulsive status epilepticus. Epilepsy Behav. 2008 May;12(4):572-86. Epub 2008 Jan 11. Review. (PubMed)
8.- Bauer G, Trinka E. Nonconvulsive status epilepticus and coma. Epilepsia. 2010 Feb;51(2):177-90. Epub 2009 Sep 10. (PubMed)
9.- Fernández-Torre JL. Nonconvulsive status epilepticus in comatose adults. Rev Neurol. 2010 Mar 1;50(5):300-8. (PubMed)
10.- Hirsch LJ, Claassen J, Mayer SA, Emerson RG. Stimulus-induced rhythmic, periodic, or ictal discharges (SIRPIDs): a common EEG phenomenon in the critically ill. Epilepsia. 2004 Feb;45(2):109-23. (PubMed)
11.- Jordan KG. Continuous EEG monitoring in the neuroscience intensive care unit and emergency department. J Clin Neurophysiol. 1999 Jan;16(1):14-39. (PubMed)
12.- Claassen J, Hirsch LJ, Kreiter KT, Du EY, Connolly ES, Emerson RG, Mayer SA. Quantitative continuous EEG for detecting delayed cerebral ischemia in patients with poor-grade subarachnoid hemorrhage. Clin Neurophysiol. 2004 Dec;115(12):2699-710. (PubMed)
13.- Rodríguez García PL, Rodríguez Pupo LR, Rodríguez García D. [Diagnosis of delayed cerebral ischaemia and cerebral vasospasm in subarachnoid haemorrhage]. Neurologia. 2010 Jun;25(5):322-30. (PubMed) (pdf)
14. Vespa PM, O’Phelan K, Shah M, Mirabelli J, Starkman S, Kidwell C, Saver J, Nuwer MR, Frazee JG, McArthur DA, Martin NA. Acute seizures after intracerebral hemorrhage: a factor in progressive midline shift and outcome. Neurology. 2003 May 13;60(9):1441-6. (PubMed)
15. Theilen HJ, Ragaller M, Tschí¶ U, May SA, Schackert G, Albrecht MD. Electroencephalogram silence ratio for early outcome prognosis in severe head trauma. Crit Care Med. 2000 Oct;28(10):3522-9. (PubMed)
16. Berkhoff M, Donati F, Bassetti C. Postanoxic alpha (theta) coma: a reappraisal of its prognostic significance. Clin Neurophysiol. 2000 Feb;111(2):297-304. (PubMed)
17. Rossetti AO, Carrera E, Oddo M. Early EEG correlates of neuronal injury after brain anoxia. Neurology. 2012 Mar 13;78(11):796-802. Epub 2012 Feb 8. (PubMed)
18. Ortega-Albás JJ, Serrano-García AL. Neurophysiology in Creutzfeldt-Jakob disease. Rev Neurol. 2003 Feb 15-28;36(4):376-80. (PubMed)
19. Herrera-Peco I, Ortega GJ, Hernando-Requejo V, Sola RG, Pastor J. Voltage sources in mesial temporal area induced by etomidate. Rev Neurol. 2010 Sep 1;51(5):263-70. (PubMed)
20. Voss LJ, Sleigh JW, Barnard JP, Kirsch HE. The howling cortex: seizures and general anesthetic drugs. Anesth Analg. 2008 Nov;107(5):1689-703. (PubMed)
21. Martínez-Rodríguez JE, Barriga FJ, Santamaria J, Iranzo A, Pareja JA, Revilla M, dela Rosa CR. Nonconvulsive status epilepticus associated with cephalosporins in patients with renal failure. Am J Med. 2001 Aug;111(2):115-9. (PubMed)
22. Bellon A, Perez-Garcia G, Coverdale JH, Chacko RC. Seizures associated with levofloxacin: case presentation and literature review. Eur J Clin Pharmacol. 2009 Oct;65(10):959-62. Epub 2009 Aug 26. (PubMed)
23. White DM, Van Cott AC. EEG artifacts in the intensive care unit setting. Am J Electroneurodiagnostic Technol. 2010 Mar;50(1):8-25. (PubMed)
24. Tatum WO, Dworetzky BA, Freeman WD, Schomer DL. Artifact: recording EEG in special care units. J Clin Neurophysiol. 2011 Jun;28(3):264-77. (PubMed)
25. McMenamin BW, Shackman AJ, Greischar LL, Davidson RJ. Electromyogenic Artifacts and Electroencephalographic Inferences Revisited. Neuroimage. 2011 Jan 1;54(1):4-9. Epub 2010 Aug 2. (PubMed) (pdf)
26. Hardin KA. Sleep in the ICU: potential mechanisms and clinical implications. Chest. 2009 Jul;136(1):284-94. (PubMed) (pdf)
27. Bourne RS, Minelli C, Mills GH, Kandler R. Clinical review: Sleep measurement in critical care patients: research and clinical implications. Crit Care. 2007;11(4):226. (PubMed) (pdf)
García Bellón, MiguelEspecialista en Neurofisiología clínica. MIR Anestesiología y Reanimación. Complejo Hospitalario de Toledo.
Soria Bretones Carmen
Especialista en Neurofisiología clínica. Hospital Virgen de la Luz. Cuenca















Buena revision, saludos
Excelente
Excelente