López Herrero R (1), Sánchez Quirós B (1), Lorenzo López M (2)
(1) MIR Anestesia y Reanimación. Hospital Clínico Universitario de Valladolid.
(2) Adjunto Anestesia y Reanimación. Hospital Clínico Universitario de Valladolid.
Artículo original: Papazian L, Aubron C, Brochard L, Chiche JD, Combes A, Dreyfuss D et al. Formal guidelines: management of acute respiratory distress syndrome. Ann. Intensive Care. 2019 Jun 13;9(1):69. doi: 10.1186/s13613-019-0540-9. (Pubmed) (PDF)
Cómo citar este artículo: López Herrero, R., Sánchez Quirós, B., & Lorenzo López, M. (2020). Manejo del Síndrome de Distrés Respiratorio Agudo (SDRA). ¿Qué hay de nuevo?. Revista Electrónica AnestesiaR, 12(8), 3. https://doi.org/10.30445/rear.v12i8.848
Introducción
El síndrome de Distrés respiratorio agudo (SDRA) es una enfermedad pulmonar inflamatoria aguda y difusa que tiene como consecuencia un aumento de la permeabilidad vascular pulmonar y una disminución del tejido pulmonar aireado. Se caracteriza por presentar hipoxemia, disminución de la compliance, aumento del shunt intrapulmonar y del espacio muerto fisiológico (1). Presenta una incidencia del 10,4% en los pacientes ingresados en unidades de cuidados intensivos y una mortalidad del 63% (2). Debida a la incidencia, a la elevada mortalidad y a la disparidad de opiniones sobre el manejo de esta patología, es necesario disponer de guías de práctica clínica donde se organicen las estrategias de tratamiento de acuerdo a la mejor evidencia científica.
Resumen de las Guías
Objetivos
Realizamos una revisión de la guía clínica para el manejo del Distrés respiratorio agudo publicada en Annals of Intensive Care en Junio de 2019.
Material y métodos
Esta guía fue desarrollada por un grupo de trabajo de expertos designados por el SRLF (Société de Réanimation de Langue Française). Los expertos formularon directrices de acuerdo con la metodología GRADE (Grading of Recommendations, Assessment, Development and Evaluation) (Tabla 1).
| NIVEL EVIDENCIA | RECOMENDACIÓN | GRADO |
| Alto | Fuerte recomendación “…debería hacerse…” | Grado 1+ |
| Moderado | Recomendación opcional “…probablemente debería hacerse…” | Grado 2+ |
| Insuficiente | Recomendación por parte de comité de expertos | Opinión de expertos |
| Moderado | Recomendación opcional “…probablemente NO debería hacerse…” | Grado 2- |
| Alto | Recomendación fuerte “…NO debería hacerse…” | Grado 1- |
| Insuficiente | No se recomienda |
Tabla 1. Recomendaciones de acuerdo a la metodología GRADE.
Para aprobar una recomendación sobre un criterio, al menos el 50% de los expertos tenían que estar de acuerdo y menos del 20% tenían que estar en desacuerdo. Para un convenio sólido, al menos el 70% de los expertos tenían que estar conformes. En ausencia de pacto firme, las recomendaciones fueron reformuladas y calificadas nuevamente, con el fin de llegar a un consenso.
En esta guía se emitieron quince recomendaciones (cuatro de ellas de evidencia alta, cuatro de evidencia moderada, siete presentaron un nivel que no permitía el uso de la clasificación GRADE, tratándose de opiniones de expertos y tres no podrían ser recomendadas con el conocimiento actual).
Estas guías están limitadas a pacientes adultos, en fase temprana de la enfermedad y sometidos a ventilación mecánica invasiva.
Resultados
Un resumen de las recomendaciones traducidas en esta guía se presenta en la tabla 2.
| RECOMENDACIÓN | GRADO DE EVIDENCIA | |
| EVALUACIÓN | Evaluación al menos cada 24 horas | Opinión de expertos |
| VOLUMEN TIDAL | Volumen corriente de 6 ml/kg de peso ideal corporal | Grado 1+ |
| PRESIÓN PLATEAU | No debe exceder los 30 cm H20 para reducir la mortalidad | Grado 1+ |
| PRESIÓN POSITIVA AL FINAL DE LA ESPIRACIÓN (PEEP) | Valor superior a 5 cmH20 en todos los pacientes con SDRA | Opinión de experto |
| MANIOBRAS DE RECLUTAMIENTO | Probablemente no deberían de ser utilizadas | Grado 2- |
| DRIVING PRESSURE | No hacer recomendaciones basadas únicamente en la limitación de la driving pressure | No recomendación |
| VENTILACIÓN OSCILATORIA DE ALTA FRECUENCIA | No debería de ser utilizada | Grado 1- |
| DECÚBITO PRONO | Debe usarse en paciente con SDRA con PaO2/FiO2<150 mmHg | Grado 1+ |
| ECMO | Podría considerarse en pacientes con PaO2/FiO2 <80 mmHg | Grado 2+ |
| BLOQUEO NEUROMUSCULAR TEMPRANO Y CORTO | Considerarse en pacientes con SDRA con PaO2/FiO2 ≤150 para reducir la mortalidad. | Grado 2+ |
| VENTILACIÓN ESPONTANEA DE MANERA PRECOZ | No recomendación | |
| SISTEMAS DE EXTRACCIÓN DE CO2 EXTRACORPOREO DE BAJO FLUJO | No recomendación | |
| ÓXIDO NÍTRICO INHALADO | Usarse en hipoxemia profunda a pesar de estrategia de ventilación mecánica protectora y posición en prono y antes de utilizar ECMO venovenosa | Opinión de expertos |
Tabla 2: Resumen de las recomendaciones presentes en la guía.
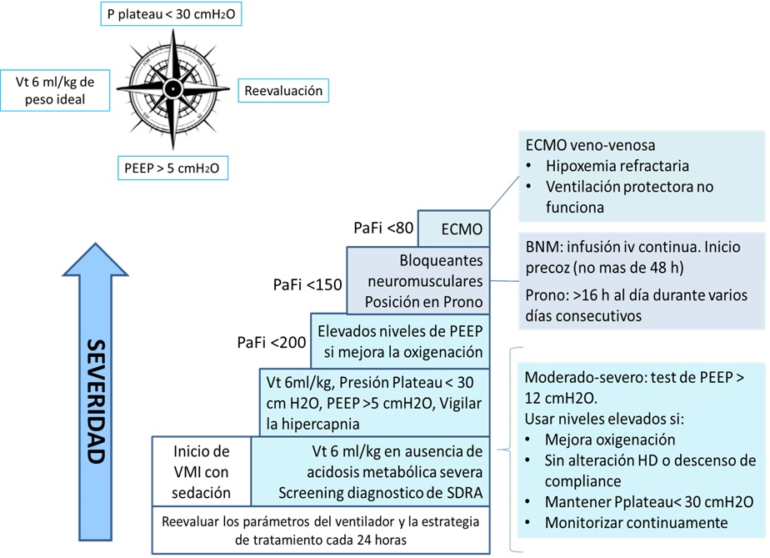
La decisión de iniciar algunos tratamientos se toma tras una fase de estabilización que incluye la optimización de la ventilación mecánica como primer paso del tratamiento. La indicación para algunos tratamientos depende de la gravedad del SDRA (que se evalúa según la relación PaO2/FiO2) y estos solo se establecen cuando haya una respuesta insuficiente a los tratamientos de primera línea. (Figura 1)
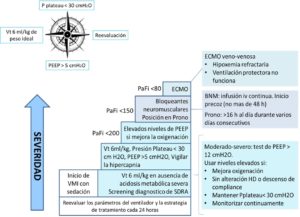
Comentario
En esta guía, no solo se abarcan estrategias de ventilación mecánica, como en la mayoría de las guías previas (3), sino que también se tratan otras estrategias terapéuticas importantes como la utilización de relajantes musculares o de óxido nítrico inhalado.
Como novedad estas guías recomiendan una reevaluación de los parámetros ventilatorios y del manejo terapéutico de los pacientes al menos una vez cada 24 horas. Esta reevaluación es importante para saber si las estrategias terapéuticas que estamos utilizando son efectivas y modificar las que no lo sean. Es difícil definir con qué frecuencia evaluar los parámetros de ventilación y tratamiento, parece que una frecuencia similar a la propuesta para la evaluación de los criterios para el destete del ventilador (es decir, diariamente) es razonable (4). En algunos casos una evaluación más frecuente podía ser necesaria.
En cuanto a la ventilación mecánica no hay nuevas aportaciones respecto a las recomendaciones sugeridas previamente por la ARDS Network (5). El uso de ventilación mecánica protectora está muy aceptado en los pacientes con SDRA, en los que se limita el Volumen corriente a 6 ml/kg de peso ideal y la presión Plateau a < 30 cmH20. Estas técnicas han demostrado una disminución de la mortalidad. Como novedad los expertos aconsejan utilizar estas tácticas en la mayor parte de los pacientes sometidos a ventilación mecánica y sedación en las unidades de cuidados intensivos debido al elevado riesgo de fallo en el reconocimiento de pacientes con SDRA.
Respecto a los niveles de PEEP tampoco existen cambios importantes. Los expertos sugieren la utilización de niveles por encima de 5 cmH2O en todos los pacientes con SDRA, utilizando valores elevados solamente en aquellos que presenten SDRA moderado o grave. En estas guías no se discute cual es el mejor método para obtener la PEEP óptima. En cualquier caso, la PEEP debería individualizarse en cada caso.
Según la opinión de los expertos las maniobras de reclutamiento alveolar probablemente no deberían realizarse. Se podrían tener en cuenta en casos de desreclutamiento (aspiración endotraqueal, desconexión accidental entre otros) y en pacientes con PaO2/FiO2 <100 mmHg a pesar de una adecuada terapia. Todavía no se recomienda una maniobra de reclutamiento, ya que no se ha comprobado que una sea superior a otra (6). Lo autores aconsejan que el procedimiento no dure más de 10-20 segundos y la presión de la vía aérea no exceda de los 30-40 cmH2O. La maniobra de reclutamiento debe realizarse con cuidado y debe interrumpirse si el paciente presenta alteraciones hemodinámicas importantes. Actualmente se están realizando estudios en los que se indicarán maniobras de reclutamiento según los hallazgos obtenidos en un TC (Tomografía computarizada) de tórax (afectación difusa o focal) (7).
Recientemente han surgido nuevos estudios sobre la asociación de niveles elevados de driving pressure y la mortalidad en el SDRA (8). Actualmente se están realizando diferentes ensayos clínicos sobre el tema. Estas guías no recomiendan utilizar únicamente una maniobra basada en limitar la driving pressure y tampoco establecen un valor límite.
La ventilación oscilatoria de alta frecuencia ha quedado relegada no recomendándose la utilización de la misma en pacientes con Distrés.
Respecto al decúbito prono no hay cambios respecto a guías anteriores. Se aconseja su utilización en pacientes con PaO2/FiO2< 150 mmHg durante sesiones de al menos 16 horas consecutivas (9).
Los autores de la guía consideran que la utilización de oxigenación de membrana extracorpórea (ECMO venovenosa) probablemente debería realizarse en pacientes con PaO2/FiO2 <80mmHg en los que han fracasado todas las estrategias. Si decidimos utilizar ECMO deberíamos contactar con un centro de referencia y hacerlo de manera precoz. Hay que tener en cuenta que la utilización de ECMO presenta múltiples complicaciones y que no ha demostrado un aumento de la supervivencia (10).
Como novedad, estas guías sugieren administrar bloqueantes neuromusculares en pacientes con PaO2/FiO2 <150 mmHg ya que han demostrado reducir la mortalidad. Se recomienda la administración mediante infusión continua en las primeras 48 horas del manejo y no deberíamos utilizar los fármacos durante más de 48 horas. No hay evidencia sobre el agente que hay que utilizar para realizar el bloqueo neuromuscular (11).
Respecto a otras guías, los autores no recomiendan la utilización de sistemas de extracción de CO2 extracorpóreo.
Los expertos sugieren la utilización de óxido nítrico inhalado en casos de SDRA con hipoxemia profunda (PaO2/FiO2 <100 mmHg) a pesar de la utilización de maniobras de ventilación mecánica protectora y posicionamiento en prono y antes de la utilización de ECMO venovenosa. La utilización de óxido nítrico inhalado produce una mejora en la oxigenación después de 24 horas de tratamiento, esta mejora suele ser transitoria. La utilización de óxido nítrico inhalado no ha demostrado aumentar la supervivencia en los pacientes con SDRA. Se recomienda no utilizar concentraciones superiores a 10 ppm, ya que en ocasiones se asocian con un empeoramiento de la PaO2/FiO2, posiblemente debido a la difusión de óxido nítrico hacia áreas no ventiladas. Los diferentes estudios sugieren que el óxido nítrico inhalado tiene un buen perfil de seguridad y que sus posibles efectos adversos (metahemoglobinemia, inhibición de la agregación plaquetaria, insuficiencia renal, producción de NO2) no son clínicamente significativos si se tiene algunas precauciones de seguridad (usos de sistemas de administración que permitan la inhalación sincronizada con el flujo inspiratorio, no utilizar niveles elevados de óxido nítrico inhalado durante periodos prolongados de tiempo, reevaluar la dosis requerida diariamente, monitorizar la función plaquetaria, los tiempos de coagulación y la función renal, no administrarlo en pacientes con déficit de metahemoglobinreductasa). Además, el destete debe ser progresivo para limitar el riesgo de un aumento repentino de la presión arterial pulmonar (12).
En estas guías se echa en falta recomendaciones sobre el uso de ventilación mecánica no invasiva, oxigenoterapia con gafas de alto flujo, la utilización de diferentes modalidades respiratorias (como por ejemplo, ventilación con índice I:E invertido, ventilación con liberación de presión en la vía aérea), intervenciones farmacológicas como el uso de corticoides sistémicos, así como un adecuado soporte nutricional o un manejo conservado de los líquidos.
Para concluir consideramos que estas guías son necesarias, ya que constituyen un estándar mínimo en la práctica clínica, pero creemos que el manejo de cada paciente debe ser individualizado y adaptarse a sus características clínicas y evolución, así como a las competencias del profesional que le atiende.
Bibliografía
- De Luis Cabezón N, Sánchez Castro I, Bengoetxea Uriarte UX, Rodrigo Casanova MP, García Peña JM, Aguilera Celorrio L. Síndrome de Distrés respiratorio agudo: revisión a propósito de la definición de Berlin. Rev Esp Anestesiol Reanim. 2014;61(6):319-327. (Elsevier)
- Bellani G, Laffey JG, Pham T, Fan E, Brochard L, Esteban A, et al. Epidemiology, patterns of care, and mortality for patients with acute respiratory distress syndrome in intensive care units in 50 countries. JAMA. 2016;315(8): 788-800. (PubMed)
- Fan E, Del Sorbo L, Goligher EC, Hodgson CL, Munshi L, Walkey AJ, et al. An Official American Thoracic Society/European Society of Intensive Care Medicine/Society of Critical Care Medicine Clinical Practice Guideline: Mechanical Ventilation in Adult Patients with Acute Respiratory Distress Syndrome. Am J Respir Crit Care Med 2017;195(9):1253-1263. (PubMed)
- Chen L, Chen GQ, Shore K, Shklar O, Martins C, Devenyi B, et al. Implementing a bedside assessment of respiratory mechanics in patients with acute respiratory distress syndrome. Crit Care. 2017;21(1):84. (PubMed)
- Acute Respiratory Distress Syndrome Network, Brower RG, Matthay MA, Morris A, Schoenfeld D, Thompson BT, Wheeler A. Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. N Engl J Med. 2000 May 4;342(18):1301-8. (PubMed)
- Zee and Gommers. Recruitment Maneuvers and Higher PEEP, the So-called open Lung Concept, in patients with ARDS. Critical Care 2019;23:73. (PubMed)
- Jabaudon M, Godet T, Futier E, Bazin JE, Sapin V, Roszyk L, et al. Rationale, study design and analysis plan of the lung imaging morphology for ventilator settings in acute respiratory distress syndrome study (LIVE study): study protocol for a randomised controlled trial. Anaesth Crit Care Pain Med. 2017;36(5):301-6. (PubMed)
- Aoyama H, Pettenuzzo T, Aoyama K, Pinto R, Englesakis M, et al. Association of Driving Pressure With Mortality Among Ventilated Patients With Acute Respiratory Distress Syndrome: A Systematic Review and Meta-Analysis. Crit Care Med. 2018;46(2):300-306. (PubMed)
- Guerin C, Reignier J, Richard JC, Beuret P, Gascouin A, Boulain T et al. Prone Positioning in Severe Acute Respiratory Distress Syndrome. N Engl J Med 2013;368(23):2159-68. (PubMed)
- Richard C, Argaud L, Blet A, Boulain T, Contentin L, Dechartres A et al. Extracorporeal life support for patients with acute respiratory distress syndrome: report of a Consensus Conference. Ann Intensive Care 2014;4:15. (PubMed)
- Papazian L, Forel JM, Gacouin A, Penot-Ragon C, Perrin G , Loundou A, et al. Neuromuscular Blockers in Early Acute Respiratory Distress Syndrome. N Engl J Med. 2010;363(12):1107-15. (PubMed)
- Monsalve-Naharro JA, Domingo-Chiva E, Garcia Castillo S, Cuesta-Montero P, Jiménez-Vizuete JM. Inhaled nitric oxide in adult patients with acute respiratory distress síndrome. Farm Hosp. 2017;41(2):292-312. (PubMed)
Cómo citar: López Herrero, R., Sánchez Quirós, B., & Lorenzo López, M. (2020). Manejo del Síndrome de Distrés Respiratorio Agudo (SDRA). ¿Qué hay de nuevo?. Revista Electrónica AnestesiaR, 12(8), 3. https://doi.org/10.30445/rear.v12i8.848


todo muy bien pero a veces queedan 24 horas
todo muy bien