Eugenio Martínez Hurtado 1, Elena Olivas García 1, Paula Martínez Fariña 1, Marta Bernardino Santos 2, Santiago García del Valle y Manzano 3
Hospital Universitario Fundación de Alcorcón
Cómo citar este artículo: Martínez Hurtado, E., Olivas García, E., Martínez Fariñas, P., Bernardino Santos, M., & García del Valle y Manzano, S. (2012). Traqueotomía Percutánea (II) con seguridad para el paciente crítico: Checklist, ecografía y fibrobroncoscopio. Revista Electrónica AnestesiaR, 4(4), 4. https://doi.org/10.30445/rear.v4i4.369
En 1.998 apareció un set para Traqueotomía Percutánea por Dilatación (TPD) conocido como Ciaglia Blue Rhino®, que esencialmente consiste en una modificación del método de Ciaglia original, y que se caracteriza por presentar un único dilatador curvo con un recubrimiento hidrofílico que reduce el coeficiente de fricción y que permite crear el traqueostoma en un único paso 1.
En una entrada anterior hemos hablado ya de la historia, los distintos métodos y sets para realizar una TPD, las indicaciones, contraindicaciones y complicaciones de la técnica.
En esta entrada:
– Presentaremos el Checklist que hemos confeccionado en nuestro centro y que revisamos antes a la realización de una Traqueotomía Percutánea por Dilatación (TPD) en la Unidad de Reanimación, válido para cualquiera de los modelos existentes en el mercado 2.
– Describiremos la técnica que seguimos en nuestro centro usando el dispositivo Blue Rhino® 3, 4.
CheckList
Técnica Blue Rhino®
1. Revisión del Checklist: Tras comprobar que consentimiento informado está firmado por la familia y en la historia clínica, comprobamos la coagulación, además del número de plaquetas y anti-Xa si procede, así como la última dosis de HBPM.
Comprobamos que el periodo de ayunas (gástrica) sea > 8 horas.
Comprobamos los parámetros del ventilador (FiO2, VTIDAL, FR, PEEP, etc.), ventilando al paciente con una FIO2 del 100% y PEEP 5-10.
Se evalúan los signos vitales y se asegura la hipnosis, analgesia y relajación, usando fentanilo, midazolam y/o propofol en dosis tituladas según la respuesta hemodinámica, y Cisatracurio (0,2 mg./kg.) o Rocuronio (0,6 mg./kg.).
Comprobamos que que hay personal suficiente y que todo el material necesario está disponible y funciona.
2. Colocación correcta del paciente: Una vez retirada la almohada se optimiza la posición del paciente, colocando un rodillo bajo los hombros para lograr una hiperextensión cervical que permite que se expongan más fácilmente las estructuras anatómicas.
 |
 |
Se identifican los anillos traqueales por palpación. Se debe identificar también las estructuras anatómicas de referencia (tiroides, cricoides, etc.).
 |
 |
3. Realización de ecografía cervical para confirmar la posición de los primeros anillos traqueales y descartar que no hay masas, vasos, pleura pulmonar, etc., en la zona de la punción 5,6.
 |
 |
 |
Guiado por ecografía, se marca el lugar de abordaje para la TPD, idealmente entre el 2º y 3er anillos (en su defecto, entre el 1º y 2º).
 |
 |
4. Retirada del tubo endotraqueal (TET), deshinchando el balón, hasta las cuerdas vocales mediante laringoscopia directa por el anestesista que manejará el fibrobroncoscopio. Se vuelve entonces a hinchar el balón.
5. Introducción del fibroscopio flexible por la luz del TET sin interrumpir la ventilación mecánica (VM). El fibroscopio está conectado a un monitor, de forma que las imágenes son visible en todo momento por todo el equipo.Si se atenúa la luz ambiental es posible ver la luz del fibrobroncoscopio a traves de la piel en el punto donde se hará la punción.
 |
 |
 |
|
6. Colocación del resto del equipo: El médico que realizará la traqueotomía se coloca a la izquierda del paciente (si es diestro), y con su mano no dominante sujeta firmemente la tráquea del paciente entre el índice y el pulgar hasta finalizar la técnica. El anestesista que le ayuda se coloca al otro lado de la cama del paciente.
7. Se punciona entre el 2º y 3er anillos traqueales (o, si no es posible, entre el 1º y 2º), perpendiculares a piel con un angulo de aprox. 45º en dirección a los pies del paciente, hasta obtener pérdida de la resistencia.
 |
 |
La imagen fibroscópica muestra la correcta entrada del catéter en la luz traqueal en la línea media. Se aspira con la jeringa, confirmando la aspiración de aire en la columna de líquido.
8. Una vez en la luz traqueal, se retiran la jeringa y la aguja metálica, dejando el catéter de plástico. Siguiendo la técnica de Seldinger, se pasa la guía de alambre con punta atraumática a través del catéter. Debe progresar sin resistencia.
Luego se usará esta guía para pasar el dilatador corto de 14 Fr. El movimiento debe ser ligeramente rotatorio. A continuación se retira el dilatador corto de 14 Fr dejando la guía de alambre en su sitio.
Todo el proceso es guiado por visión fibroscópica viendo primero la progresión hacia carina de la guía de alambre y posteriormente la entrada en la luz traqueal del dilatador corto.
 |
 |
 |
Control con fibroscopio Control con Ascope |
9. Previamente a introducir el dilatador Blue Rhino®, hacer una pequeña incisión en la piel que facilite el paso del mismo.
Tras sumergir el dilatador Blue Rhino® en agua estéril o solución salina para activar el recubrimiento hidrofílico, se introduce sobre el catéter guía, que a su vez se introduce sobre la guía metálica. Realizando movimientos firmes, avanzamos hasta que se llega a la marca de posicionamiento del dilatador.
La posición del dilatador Blue Rhino® debe estar perfectamente alineada con respecto a la tráquea del paciente, que debemos sujetar firmemente en todo momento, para evitar traumatismos en la pared traqueal posterior durante la introducción.
No se debe sobrepasar esta marca para evitar lesiones en la carina (sobre todo en pacientes con peso de 50 kg. o menos, y 120 cm. o menos de altura).
 |
 |
10. Tras retirar el dilatador Blue Rhino® se introduce la cánula de traqueostomía no fenestrada lubricada, ensamblada previamente en el dilatador de carga sobre el catéter guía, con el balón completamente desinflado (previamente comprobado).
El sistema cánula/dilatador de carga ensamblados debe dirigirse perpendicular al eje de la traquea durante la introducción para la dilatación entre los cartílagos sea uniforme. Una vez que la cánula de traqueotomía esté dentro de la luz traqueal, el sistema ensamblado puede dirigirse en dirección caudal.
Tras esto se podrá retirar el dilatador, el catéter guía y la guía metálica, avanzando la cánula de traqueotomía.
 |
11. Se confirma la adecuada posición de la cánula y la ausencia de sangrado con el fibroscopio a través de la luz del TET. Se infla entonces el balón de la cánula de traqueostomía, y se conecta al respirador con sonda de capnografía.
La aparición de la curva de capnografía confirma la correcta ventilación del paciente. A continuación se retira el TET y se fija la cánula al cuello.
 |
Videos
Simulación
Uso del Blue Rhino
Control ecográfico del cuello
Entre las posibles contraindicaciones de la TPD están la existencia de un tiroides de gran tamaño, la existencia de anomalías o variantesanatómicas que compliquen la técnica, incluída la existencia de vasos sanguíneos anómalos que puedan ocasionar un sangrado importante o incluso peligroso, la desviación de la tráquea, cuellos muy gruesos, con poca o nula movilidad, etc.
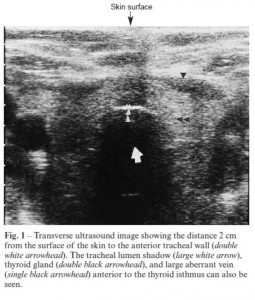
Para solventar todos estos problemas, Muhammad et al. analizaron en 1.999 si el uso de los ultrasonidos tenía indicación en la realización de TPD en pacientes críticos 5. Aunque sólo expusieron 4 casos, concluyeron que el ecógrafo ayudaba al diagnóstico de posibles problemas (como la localización ecográfica de una vena anómala pretraqueal, en la imágen) y, por tanto, parecía una herramienta útil y beneficiosa.
Posteriormente, en 2.011 Rajajee et al. analizaron el uso del ecográfo a pie de cama durante la realización de la TPD en 13 pacientes, de los cuales 3 eran obesos mórbidos, 2 tenían lesiones de columna cervical y 1 una traqueotomía previa 6.
Aunque el estudio contaba sólo con 13 pacientes, y en palabras de sus autores estaba limitado por ser sólo una demostración preliminar, concluyeron que los ultrasonidos son útiles para prevenir el sangrado de las estructuras vasculares pretraqueales.
Además, el ecógrafo permite localizar y delimitar los anillos traqueales, de forma que se evita el riesgo de punción por encima del 1er anillo, especialmente en aquellos pacientes en los que no puede localizarse claramente mediante palpación manual (p.ej. obesos mórbidos) o en los que no puede lograrse la extensión de cuello (p.ej. lesiones cervicales).
Fibrobroncoscopia de control
En 1.990 Marelli et al. analizaron la viabilidad de la aplicación generalizada de la TPD guiada por fibrobroncoscopia en 61 pacientes. Además de encontrar una reducción de los costes generales del 50% repecto a la traqueotomía quirúrgica, concluyeron que la guía con el fibro parecía aumentar la seguridad del procedimiento, ayudando a prevenir las complicaciones como neumotórax, enfisema subcutáneo o el paso paratraqueal a través de una falsa vía notificados con métodos percutáneos ciegos 7. Varios autores posteriormente recomendaron su uso dado que aumentaba la seguridad de la punción traqueal, permitiendo además la corrección durante el procedimiento de las punciones paramediales 8,9,10,11,12.
Sin embargo, la inserción de un broncoscopio en la vía aérea de un paciente en VM no está exenta de riesgos, y puede generar una obstrucción al flujo de aire que determine la hipoventilación del paciente, pudiendo dar lugar a una hipoventilación iatrogénica oculta con hipercapnia 13. Por este motivo hay que mantener la monitorización durante todo el procedimiento.
Por otro lado, diversos trabajos han analizado los efectos que la fibrobroncoscopia genera sobre la presión intracraneal (PIC) en los pacientes con traumatismo craneoencefálico (TCE) grave, encontrando que, aunque aumenta la PIC, la presión arterial media (PAM) también aumenta, manteniéndose una adecuada presión de perfusión cerebral (PPC). Además, la PIC vuelve a sus niveles basales después del procedimiento, de modo que cuando se realiza correctamente, la fibrobroncoscopia no parece afectar negativamente al estado neurológico en pacientes con TCE grave 14,15,16.
Eugenio Martínez Hurtado 1 Elena Olivas García 1 Paula Martínez Fariña 1 1.- Residente de Anestesiología, Reanimación y Dolor Marta Bernardino Santos 2 2.- FEA Anestesiología y Reanimación Santiago García del Valle y Manzano 3 3.- Jefe de la Unidad de Anestesiología y Reanimación Hospital Universitario Fundación de Alcorcón (Madrid)Bibliografía
1.- Byhahn C, Lischke V, Scheifler G, Westphal K. Ciaglia blue rhino: a modified technique for percutaneous dilatation tracheostomy. Technique and early clinical results. Anaesthesist. 2000 Mar;49(3):202-6. (PubMed)
2.- Pablo Jorge Monjas, César Aldecoa-ílvarez Santullano. Dispositivos de Abordaje Percutáneo. Documentos ESRA. (pdf)
3.- Rakesh Bhandary, Niraj Niranjan. Anaesthesia Tutorial of the Week (ATOTW). TRACHEOSTOMY. ANAESTHESIA TUTORIAL OF THE WEEK 241, 17TH OCTOBER 2011. World Federation of Societies of Anaesthesiologists (WFSA) (pdf)
4.- Susarla SM,Peacock ZS,Alam HB. Percutaneous Dilatational Tracheostomy: Review of Technique and Evidence for Its Use. J Oral Maxillofac Surg.2011 Aug 4. [Epub ahead of print]. (PubMed), (pdf)
5.- Muhammad JK, Patton DW, Evans RM, Major E. Percutaneous dilatational tracheostomy under ultrasound guidance. Br J Oral Maxillofac Surg. 1999 Aug;37(4):309-11. (PubMed), (pdf)
6.- (Rajajee V, Fletcher JJ, Rochlen LR, Jacobs TL. Real-time ultrasound-guided percutaneous dilatational tracheostomy: a feasibility study. Crit Care. 2011;15(1):R67. Epub 2011 Feb 22. (PubMed), (pdf)
7.- Marelli D, Paul A, Manolidis S, Walsh G, Odim JN, Burdon TA, Shennib H, Vestweber KH, Fleiszer DM, Mulder DS: Endoscopic guided percutaneous tracheostomy:early results of a consecutive trial. J Trauma 1990,30:433-435. (PubMed)
8.- Winkler WB, Karnik R, Seelmann O, Havlicek J, Slany J. Bedside percutaneous dilational tracheostomy with endoscopic guidance: experience with 71 ICU patients. Intensive Care Med. 1994 Aug;20(7):476-9. (PubMed)
9.- Barba CA, Angood PB, Kauder DR, Latenser B, Martin K, McGonigal MD, Phillips GR, Rotondo MF, Schwab CW: Bronchoscopic guidance makes percutaneous tracheostomy a safe, cost-effective, and easy-to-teach procedure. Surgery 1995, 118:879-883. (PubMed)
10.- Fernandez L, Norwood S, Roettger R, Gass D, Wilkins H 3rd. Bedside percutaneous tracheostomy with bronchoscopic guidance in critically ill patients. Arch Surg. 1996 Feb;131(2):129-32. (PubMed)
11.- Hinerman R, Alvarez F, Keller CA. Outcome of bedside percutaneous tracheostomy with bronchoscopic guidance. Intensive Care Med. 2000 Dec;26(12):1850-6. (PubMed)
12.- Kost KM. Endoscopic percutaneous dilatational tracheotomy: a prospective evaluation of 500 consecutive cases. Laryngoscope. 2005 Oct;115(10 Pt 2):1-30. (PubMed)
13.- Reilly PM, Anderson HL III, Sing RF, Schwab CW, Bartlett RH: Occult hypercarbia. An unrecognized phenomenon during percutaneous endoscopic tracheostomy. Chest 1995, 107:1760-1763. (PubMed), (pdf)
14.- Peerless JR, Snow N, Likavec MJ, Pinchak AC, Malangoni MA. The effect of fiberoptic bronchoscopy on cerebral hemodynamics in patients with severe head injury. Chest. 1995 Oct;108(4):962-5. (PubMed), (pdf)
15.- Kerwin AJ, Croce MA, Timmons SD, Maxwell RA, Malhotra AK, Fabian TC. Effects of fiberoptic bronchoscopy on intracranial pressure in patients with brain injury: a prospective clinical study. J Trauma. 2000 May;48(5):878-82; discussion 882-3. (PubMed)
16.- Kocaeli H, Korfali E, TaÅŸkapilioÄŸlu O, Ozcan T. Analysis of intracranial pressure changes during early versus late percutaneous tracheostomy in a neuro-intensive care unit. Acta Neurochir (Wien). 2008 Dec;150(12):1263-7; discussion 1267. Epub 2008 Nov 11. (PubMed)









Solicito informacion para poderme contactar con el especialista de linea para que de a conocer el set de traqueostomia percutanea en la unidad de cuidados intensivos MEINTEGRAL en CHAPARRAL DEPARTAMENTO DEL TOLIMA COLOMBIA (yo ya lo conozco pero mis compañeros no).
Agradecimientos,
SANDRA PATRICIA PEí‘A ROMERO
Buenos dias
vivo en Mexico, Distroto Federal, donde puedo conseguier la canula de traqueostomia percutanea.
gracias.
Hola me intwresa comprar un set para la traqueostomia percutanea en Mexico cdmx gracias urgente conseguir