Martin Orejas M (1), Martin Mora V (2)
(1) Residente de Anestesiología y Reanimación. Hospital Universitario Vall d’Hebron de Barcelona.
(2) Adjunto del Servicio de Anestesiología y Reanimación. Hospital Universitario Vall d’Hebron de Barcelona.
Cómo citar este artículo: Martín Orejas, M., & Martín Mora, V. (2020). AT-121, ¿el opioide perfecto?. Revista Electrónica AnestesiaR, 12(7), 4. https://doi.org/10.30445/rear.v12i7.862

Históricamente está documentado el uso de opio en distintas civilizaciones y épocas de la historia. Los egipcios utilizaron el opio para tratar las cefaleas del dios Ra. Galeno lo empezó a usar en el siglo II d.C. como analgésico y contra la disentería, y Paracelso creó el láudano en 1522 y lo llamó “piedra de la inmortalidad”. En 1805, Sertumer logró la purificación de la morfina. Durante la Segunda Guerra Mundial, Ehrhart y Bockmühl desarrollaron la metadona. Más tarde apareció la heroína, en los años 70, junto con las primeras teorías sobre receptores opioides y ligandos endógenos.

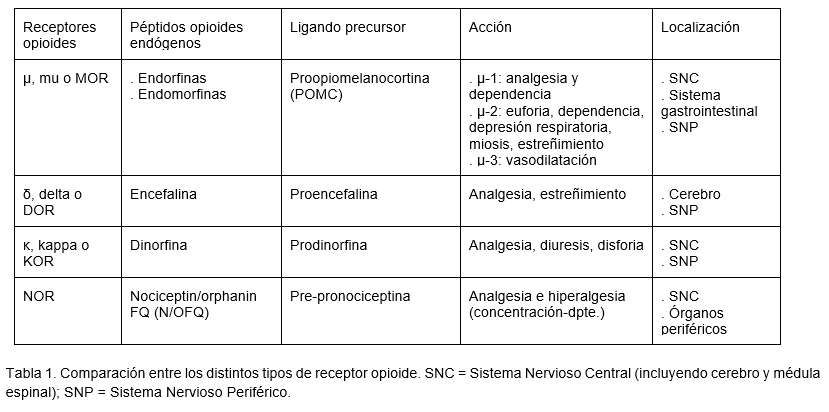
Los opioides son los analgésicos más potentes y efectivos disponibles en la actualidad. La mayoría de ellos son agonistas del receptor mu (MOR, de las siglas en inglés Mu Opioid Receptor) (Tabla 1.). La activación de MOR, no solo posee efectos antinociceptivos, también aumenta la disponibilidad sináptica de dopamina, principal neurotransmisor en la creación de circuitos de recompensa. Este refuerzo positivo explica la epidemia mundial de adicción y abuso de opioides sintéticos, que afecta especialmente a los Estados Unidos.
En 1994, Mollereau et al. clonaron un cuarto tipo de receptor opioide con actividad homóloga a los receptores ya conocidos, el receptor del péptido nociceptina/orfanina (NOP, de las siglas en inglés Nociceptin/Orphanin Peptide). El receptor NOR y su ligando endógeno N/OFQ se expresan en el mismo circuito neuronal que el resto de receptores y ligandos opioides. A diferencia de éstos, NOR-N/OFQ inhibe la liberación de dopamina. Si no hay efecto recompensa, no se genera adicción: éste podría ser un aspecto clave en el tratamiento del dolor crónico y el manejo del abuso a opioides.
Existen diferencias importantes en la farmacocinética y farmacodinamia del sistema NOR-N/OFQ entre las distintas especies estudiadas (roedores, primates y humanos). En los estudios en roedores se ha relacionado este sistema con la aparición de hiperalgesia y efectos anti-opioides a nivel supraespinal, aunque a nivel espinal puede producir analgesia. En primates no humanos, los agonistas selectivos de los receptores de NOP producen un efecto analgésico comparable al de la morfina, tanto a nivel central (espinal y supraespinal) como periférico, sin producir depresión respiratoria, ni hiperalgesia y tampoco “efecto recompensa” (potencial de abuso).
AT-121
Ding H, et al. demostraron en primates que, el patrón de abuso tras la administración repetida de AT-121 era diferente del que se presenta con otras sustancias (Fig. 1A y 1B). La evolución hacia la tolerancia y la dependencia podría ser más lenta con AT-121 que, con otros opiáceos, ya que atenúa el efecto recompensa (tanto de la propia molécula como de los mórficos), disminuyendo la necesidad del consumo. No se encontraron datos de hiperalgesia inducida por esta sustancia.
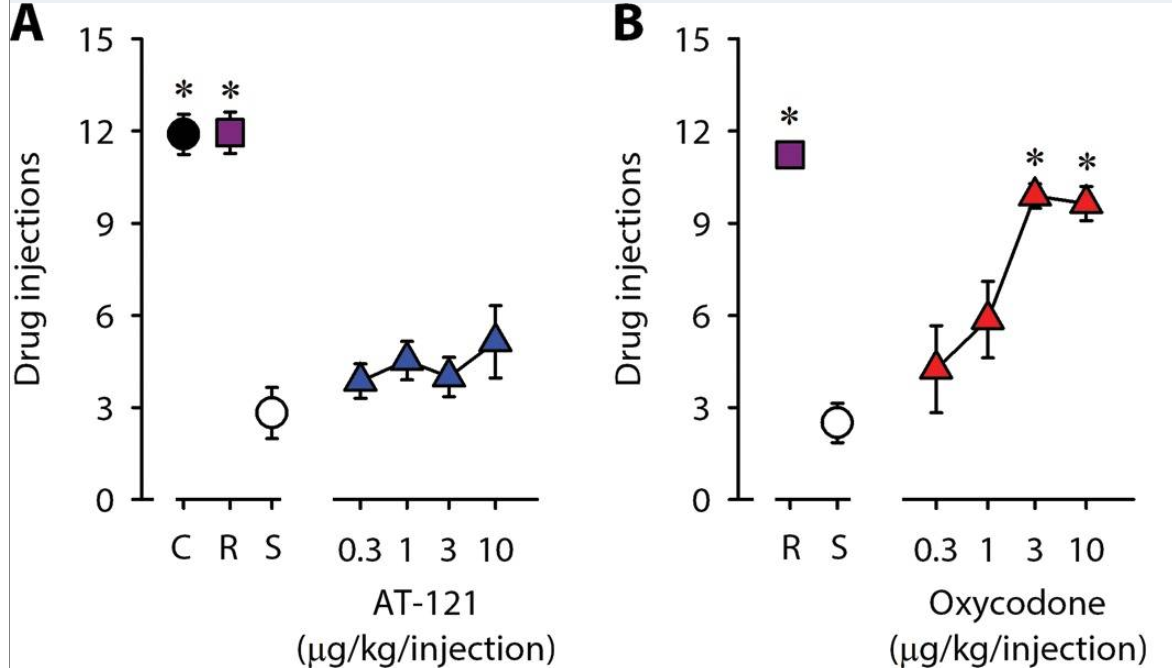
Comparación del “efecto recompensa” tras administración de diversos opioides: número de veces que el mono se inyecta el fármaco tras una primera exposición. Evaluación del potencial de abuso. Cocaína a 0,03 mg/kg/dosis, remifentanilo a 0,3 mcg/kg/dosis, solución salina a ~0,14 ml/kg/dosis), AT-121 a 0,3-10 mg/kg/dosis u oxicodona 0,3-10 mg/kg/dosis. AT-121 y oxicodona: efectos diferentes en función de la dosis administrada.
Todas estas características podrían hacer de AT-121 un fármaco clave en el manejo de pacientes con dolor crónico.
Norikazu Kiguchi et al. describieron un agonista parcial de MOP/NOP denominado BU10038, con unas propiedades farmacocinéticas y farmacodinámicas similares a AT-121.
En los últimos años se han investigado distintos agonistas bifuncionales de NOP/MOP como AT-201, AT-212, cebranopadol o GRT6005, BU08028, etc. Los datos actuales indican que AT-121 es un fármaco seguro: en primates una dosis de 0.03 mg/kg produce analgesia completa sin alterar la función respiratoria o la hemodinamia y sin variación del nivel de conciencia.
A la espera de futuras investigaciones en humanos, los resultados obtenidos hasta la fecha son esperanzadores.
BIBLIOGRAFÍA
- Ding et al., A bifunctional nociceptin and mu opioid receptor agonist is analgesic without opioid side effects in nonhuman primates. Sci Transl Med. 2018 Aug 29; 10(456): eaar3483. (HTLM)
- Ding et al., A novel orvinol analog, BU08028, as a safe opioid analgesic without abuse liability in primates. PNAS September 13, 2016 113 (37) E5511-E5518. (HTLM)
- Kiguchi et al., BU10038 as a safe opioid analgesic with fewer side-effects after systemic and intrathecal administration in primates. Br J Anaesth 2019 Jun;122(6):e146-e156. (PubMed)
- Nurulain T. The Nociceptin Opioid Receptor (NOP) as a Therapeutic Target: Progress in Translation from Preclinical Research to Clinical Utility. J Med Chem. 2016 Aug 11; 59(15): 7011–7028 (HTML)
PEARLTREES GATIV
Cómo citar: Martín Orejas, M., & Martín Mora, V. (2020). AT-121, ¿el opioide perfecto?. Revista Electrónica AnestesiaR, 12(7), 4. https://doi.org/10.30445/rear.v12i7.862




Excelentes artículos médicos!
A falta de efedrina en mi país, he estado combinando en subaracnoideo, lidocaína 2%, Ropivacaína 7.5% y Glucosa 50%.
Excelentes resultados, sin hipotensión. Sin Síndromes supinos obstétricos.
Inicio rápido, duración de 3.5 hs hasta 4.
La he usado en obstetricia (cesáreas, histerectomías, legrados y Lápara Ginecólogica.
En Cirugía General, hernias y apendicectomías. Laparotomías infraumbilicales.
En trauma, cirugía de cadera, rodilla, etc.
Hemos aprendido a sobrevivir sin el simpaticomimético.
Saludos!